Nature:淋巴瘤中CARD11-PIK3R3突变,让CAR-T细胞抗癌能力提高百倍
时间:2024-03-08 10:02:10 来源 网络 作者:网络
CAR-T细胞疗法是一种革命性的癌症治疗新技术,自2017年以来,美国FDA已经批准了六种CAR-T细胞疗法用于治疗恶性血液类癌症,并展现了令人印象深刻的治疗效果。
然而,CAR-T细胞疗法对血液类癌症效果突出,但对占据癌症总数90%的实体瘤的治疗效果却差强人意。因此,如何提高CAR-T细胞疗法在实体瘤中的治疗效果,是一个亟待解决的难题。
2024年2月7日,西北大学的 Jaehyuk Choi 团队和加州大学旧金山分校的 Kole Roybal 团队在 Nature 期刊发表了题为:Naturally occurring T cell mutations enhance engineered T cell therapies(自然发生的T细胞突变增强了工程化T细胞疗法)的研究论文。
该研究采取了“师夷长技以制夷”的策略,通过研究导致淋巴瘤的恶性T细胞基因突变,并将编码这种天然存在的、独特的突变基因整合到CAR-T细胞,使它们杀死癌细胞的能力提高了100倍以上,而且不存在毒副作用和促癌风险,这为CAR-T细胞疗法在实体瘤上的治疗应用打开了新的大门!

CAR-T细胞疗法已经彻底改变了血液类癌症的治疗格局,但在实体瘤和耐药血液恶性肿瘤中,这一新兴前沿疗法还是受到多种因素的限制,包括体内持久性差、免疫抑制环境因素和T细胞耗竭等等。
有趣的是,虽然人工改造的CAR-T细胞持续战斗能力很差,但导致淋巴瘤的恶性T细胞却能在体内持续存在。常言道,“师夷长技以制夷”,恶性T细胞很可能存在一种特殊的基因突变使其拥有强大的生命力,如果能将这种基因代码写入到CAR-T细胞中,是否就能做到“取癌症之长,治癌症之乱”?
为了印证这一想法,研究团队对T细胞肿瘤中发生的适应性突变进行筛选,生成了一个包含71个突变和45个野生型对照的基因文库。紧接着,他们将这些突变整合到人类和小鼠的T细胞中,进而筛选和评估它们对体外和体内T细胞表型的影响。

在体外和体内筛选确定T细胞突变,重新编程CAR信号和功能输出
研究团队在CD4+皮肤T细胞淋巴瘤中发现了一种独特的基因融合——CARD11和PIK3R3的融合——称为CARD11-PIK3R3。携带这一基因突变的CAR-T细胞显著增加了AP-1和NF-κB信号转导、白细胞介素-2(IL-2)的产生和体内外肿瘤杀伤作用。
进一步研究表明,CARD11-PIK3R3以抗原依赖的方式增强了CARD11-BCL10-MALT1复合物信号通路,促进CAR-T细胞在几种对免疫疗法不敏感的肿瘤模型中的抗肿瘤疗效,并具有持久的肿瘤杀伤活性。
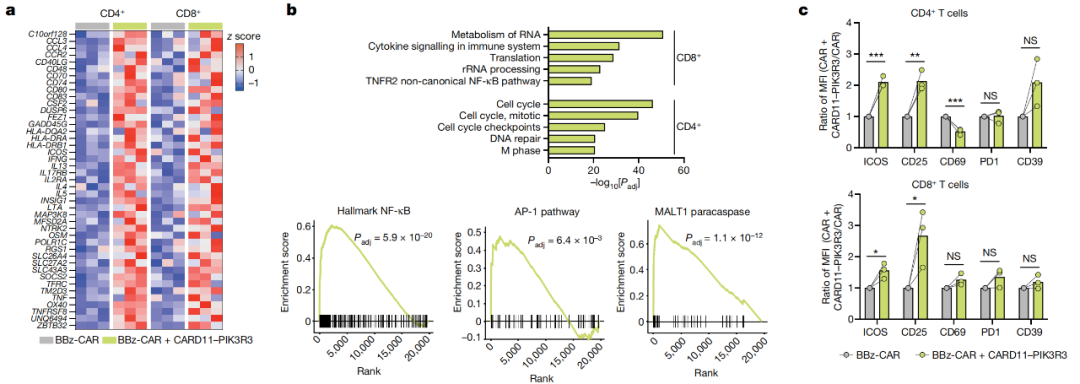
CARD11-PIK3R3的表达导致原代人类CD8+T细胞的信号转导、转录和功能增强
不仅如此,CARD11-PIK3R3还可以大幅降低CAR-T细胞的治疗剂量,在常规CAR-T疗法中,通常需要使用上百万个CAR-T细胞来治疗癌症小鼠,但在整合了CARD11-PIK3R3基因突变之后,仅需2万个新型CAR-T细胞就足以消灭肿瘤。换而言之,CARD11-PIK3R3使CAR-T细胞杀死癌细胞的能力提高了100倍。

CARD11-PIK3R3提高了人和小鼠CAR-T细胞在体内的治疗效果
因此,得益于如此强大的抗肿瘤杀伤作用,这一新技术降低了对CAR-T细胞剂量的需求,并减轻对苛刻的淋巴细胞耗竭预处理的要求。更重要的是,在注射治疗418天后,表达CARD11-PIK3R3的CAR-T细胞没有出现恶性转化的表征,证明了这一新技术在体内的安全性。

CARD11-PIK3R3增强了小鼠和人TCR-T细胞在体内的治疗效果
结 语
总而言之,这项发表在 Nature 的研究表明,存在于淋巴瘤中的基因突变——CARD11-PIK3R3,让CAR-T细胞对实肿瘤的杀伤作用提高百倍。这一研究结果也提示我们,合理利用自然发生的基因突变可能是改良T细胞免疫疗法的新方向。
参考文献:
https://www.nature.com/articles/s41586-024-07018-7 https://www.nature.com/articles/d41586-024-00305-3

