近年来,中枢神经系统肿瘤的诊断已从基于显微镜形态学的诊断模式,转变为以识别肿瘤细胞体细胞基因变异为主导的诊断模式。这一转变需要采用截然不同的检测方法,而这就必须配备相应的培训与资金资源。加拿大神经病理学家协会(CANP)基于科学文献与共识制定了脑和脊髓肿瘤分子检测建议,旨在平衡两方面需求:一是获得对治疗具有决定意义的精准诊断的需求,二是向新诊断模式过渡过程中固有的当前局限性。CANP下属的专业事务委员会负责执行此项任务。CANP全体大会期间对建议草案进行了讨论,同时邀请了已应用分子检测技术的团队以及依赖外部实验室开展检测的团队进行报告。专业事务委员会总结了共识内容,并将建议提交至CANP执行委员会。最终报告在CANP网站上公示一个月,供所有成员提出意见。以下建议适用于中枢神经系统原发性肿瘤,不包括转移性肿瘤或由神经系统外侵犯至神经系统的肿瘤。这些建议具有临床相关性,因为检测结果会对患者治疗产生直接影响——无论是通过靶向治疗的应用,还是通过经临床试验证实的放疗和/或化疗的最佳应用方案。
研究背景
以下建议概述了截至2024年中枢神经系统特定肿瘤诊断中的最佳实践,涉及弥漫性和局限性胶质瘤、神经节神经胶质瘤、室管膜瘤及髓母细胞瘤。这些建议已通过CANP的全国性审核与批准。随着科学研究的持续推进和临床经验的不断积累,本文档内容预计将逐步更新完善。
本文档还明确了加拿大诊断实验室为实现世界卫生组织(WHO)当前标准下的脑肿瘤诊断所需达到的最低要求,包括下文详述的免疫组化检测、分子检测及细胞基因学检测。为实现最优工作流程和及时的患者诊疗,建议在可能的情况下尽量增加分散式检测;但甲基化谱分析可能需要采用更集中化的检测模式。
弥漫性胶质瘤
弥漫性胶质瘤分为成人型和儿童型肿瘤。成人型弥漫性胶质瘤包括:(1)IDH突变型星形细胞瘤与少突胶质细胞瘤;(2)IDH野生型胶质母细胞瘤。儿童型弥漫性胶质瘤分为:(3)低级别(主要特征为MAPK通路基因或MYB/MYBL1基因存在变异);(4)高级别(主要特征为组蛋白、错配修复、受体酪氨酸激酶等多种变异)。从组织学角度来看,弥漫性胶质瘤通常不具备显著特征,因此需谨慎结合免疫组化检测与分子检测,以实现整合诊断。
在成人患者中,成人型分子变异占主导。需区分IDH突变型胶质瘤与IDH野生型胶质瘤,后者预后显著更差。对于年轻成人患者,应考虑存在儿童型分子变异的可能。
弥漫性胶质瘤的调整后诊断流程图请参见图1。
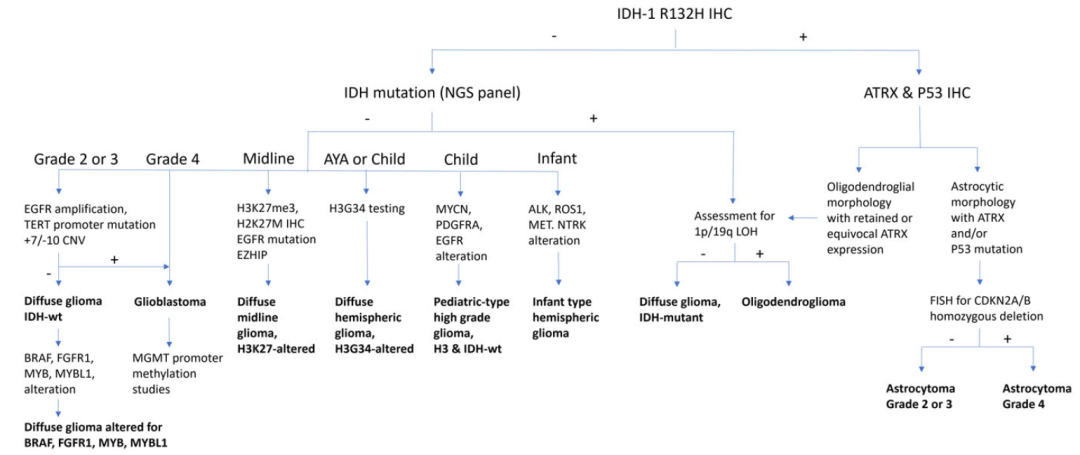

图1
1. IDH1基因最常见的突变类型(IDH1 p.R132H突变)可通过免疫组化(IHC)检测。该检测可联合ATRX±p53的免疫组化检测。在存在IDH突变的前提下,ATRX蛋白缺失(通常伴随p53蛋白异常表达)可作为星形细胞瘤的诊断依据;反之,若ATRX蛋白表达保留,则应进一步检测1p/19q共缺失,该变异可作为少突胶质细胞瘤的诊断依据。对于组织学表现为低级别且存在IDH突变的星形细胞瘤,可通过检测CDKN2A/B基因的拷贝数状态辅助分级。CDKN2A/B纯合缺失已被证实与患者生存期缩短相关,同时也可作为少突胶质细胞瘤3级的分子标志物。
2. 对于IDH1 p.R132H突变检测阴性的肿瘤,需结合临床背景进一步评估:
i. 年龄>55岁且肿瘤组织学表现符合胶质母细胞瘤特征的患者,通常无需进一步诊断检测,可直接诊断为IDH野生型胶质母细胞瘤;
ii. 年龄<55岁和/或肿瘤组织学表现为低级别特征的患者,需进一步检测IDH1和IDH2基因的“非经典型”突变;同时,应根据情况考虑检测与IDH野生型胶质母细胞瘤相关的分子变异和/或儿童型分子变异。
3. 对于组织学表现为低级别且IDH野生型的弥漫性胶质瘤(尤其发生于中老年患者的肿瘤),应检测IDH野生型胶质母细胞瘤的特征性分子变异,包括:7号染色体获得与10号染色体缺失同时存在、EGFR扩增和/或TERT启动子突变。
4. 所有IDH野生型胶质母细胞瘤均需检测MGMT启动子甲基化状态;目前尚不清楚IDH突变型星形细胞瘤患者是否能从该检测中获益。对于儿童和年轻成人患者,其弥漫性胶质瘤应检测儿童型分子变异。在儿童和年轻成人患者中,儿童型分子变异较为常见,且这类变异适用于靶向治疗;对于青少年及以上患者,应考虑存在成人型分子变异(IDH1、IDH2基因突变)的可能性。肿瘤发生部位(半球型vs中线型)对检测方向的选择也具有重要指导意义。
5. 半球型弥漫性低级别胶质瘤应检测以下变异:MAPK通路基因(包括FGFR1、FGFR2、FGFR3、KRAS、NF1、BRAF)、MYB基因和MYBL1基因的单核苷酸变异(SNVs)、插入/缺失(indels)及融合;也可纳入对NTRK1、NTRK2、NTRK3、MAP2K1和MET基因少见变异的检测。同时,应考虑检测成人型分子变异。BRAF p.V600E突变可通过免疫组化检测;对于存在BRAF p.V600E突变的肿瘤,需检测CDKN2A/B基因的拷贝数状态。若存在CDKN2A/B纯合缺失和/或TERT基因变异和/或ATRX基因变异,则应考虑其他诊断可能性(参见下文“局限性胶质瘤与神经节神经胶质瘤”建议2)。
6. 半球型弥漫性高级别胶质瘤应检测以下内容:H3-3A基因突变(用于诊断H3G34突变型弥漫性半球胶质瘤)、EGFR和PDGFRA基因的SNVs与扩增、癌症易感综合征相关基因(错配修复和复制修复相关基因:MLH1、MSH2、MSH6、PMS2、POLE、POLD1,以及TP53基因)的变异,以及MYCN基因扩增;同时,应考虑检测成人型分子变异。该类肿瘤的组织学表现可能与目前归类为“局限性”的肿瘤存在重叠(参见下文“局限性胶质瘤与神经节神经胶质瘤”建议2),此时可通过DNA甲基化谱分析区分分子特征重叠的肿瘤实体。H3 p.G34R突变和错配修复(MMR)状态可通过免疫组化检测。对于婴儿患者,需检测涉及受体酪氨酸激酶(包括ALK、ROS1、NTRK1、NTRK2、NTRK3、MET)的融合变异(用于诊断婴儿型半球胶质瘤)。
7. 对于所有年龄段患者的中线部位(丘脑、脑干、小脑、脊髓)弥漫性胶质瘤,应通过免疫组化检测H3K27三甲基化(H3K27me3)状态,并检测H3-3A基因(或较少见的H3C2、H3C3、H3C14基因)的变异。H3 p.K28M(K27M)突变可通过免疫组化检测。BRAF或FGFR1的继发变异也可纳入。对于H3野生型病例,应检测EGFR扩增状态和zeste增强子抑制蛋白(EZHIP)的过表达情况(IHC)。
局限性胶质瘤与神经节神经胶质瘤
大多数局限性胶质瘤与神经节神经胶质瘤以MAPK通路变异(SNVs、indels、融合)为特征。在特定肿瘤类型中,CDKN2A/B基因的拷贝数变异以及端粒维持相关基因(ATRX、TERT)的变异,是重要的额外分子特征。
这一类别的罕见肿瘤具有特定的分子变异特征。
1. 毛细胞型星形细胞瘤应检测MAPK通路变异,包括BRAF基因(SNVs、融合)、FGFR1基因(SNVs、融合、内部串联重复)及NF1基因变异;也可纳入对KRAS、PTPN11、RAF1等少见变异基因的检测。
2. 具有毛细胞样特征的高级别星形细胞瘤(HGAP)与多形性黄色星形细胞瘤(PXA),除需检测MAPK通路变异(BRAF、FGFR1、NF1)外,还应检测CDKN2A/B基因(拷贝数缺失)及ATRX和/或TERT基因变异。匹配的DNA甲基化谱是HGAP的必需诊断标准,对PXA的诊断也具有参考价值。若肿瘤存在RAS/MAPK通路变异,且同时伴有ATRX缺失和/或CDKN2A/B纯合缺失,则高度提示HGAP可能;但目前HGAP的确诊仍需依赖甲基化谱分析。
3. 神经节胶质瘤应检测BRAF基因变异,其中BRAF p.V600E突变可通过IHC检测;也可纳入对RAF1、KRAS、NF1等其他MAPK通路少见变异基因的检测。该肿瘤不应存在CDKN2A/B纯合缺失。
4. 多种罕见局限性胶质瘤与神经节神经胶质瘤的诊断,可通过检测特定分子变异或特定DNA甲基化谱得以确认。在这类情况下,下一代测序(NGS)优于甲基化谱分析,因为前者可提供特定治疗靶点。
-
胚胎发育不良性神经上皮肿瘤:FGFR1 SNVs、融合、内部串联重复(ITD);
-
乳头状胶质神经元肿瘤:PRKCA融合;
-
形成菊形团的胶质神经元肿瘤:FGFR1、NF1和/或PIK3CA变异;
-
黏液样胶质神经元肿瘤:PDGFRA SNVs;
-
弥漫性软脑膜肿瘤:BRAF融合,伴1p缺失±19q缺失±1q获得;
-
多结节空泡状神经元肿瘤:MAP2K1 SNVs;
-
脑室外神经细胞瘤:FGFR1融合;
-
促纤维增生性婴儿神经节胶质瘤/星形细胞瘤:BRAF、RAF1、FGFR1变异;
-
具有少突胶质细胞瘤样特征及核簇的弥漫性胶质神经元肿瘤:特异性DNA甲基化谱;
-
星形母细胞瘤:MN1融合;
-
脊索样胶质瘤:PRKCA SNVs。
室管膜瘤
1.后颅窝室管膜瘤应通过免疫组化检测H3K27me3缺失情况;若条件允许,还应同时通过免疫组化检测EZHIP表达情况,以区分后颅窝A型(PFA)与后颅窝B型(PFB)室管膜瘤。DNA甲基化谱分析是替代检测方法,在成人病例中(需鉴别PFB与甲基化分类中的亚室管膜瘤时)可能有帮助。PFA室管膜瘤应检测1q与6q的拷贝数变异;甲基化分类中的亚室管膜瘤应检测TERT启动子突变与6号染色体缺失情况。
2. 幕上室管膜瘤应检测ZFTA与YAP1基因融合;对于存在ZFTA融合的肿瘤,还应检测CDKN2A/B基因的拷贝数状态。
3. 组织学表现为高级别的脊髓室管膜瘤,应检测MYCN基因扩增情况。
髓母细胞瘤
1. 所有髓母细胞瘤均应进行分子检测以明确分子亚组。DNA 甲基化分析和/或纳米串分析是适用的技术手段。根据不同亚组需求,可能还需检测拷贝数变异(如3组髓母细胞瘤中的MYC基因扩增)。
2. 儿童期 SHH激活型髓母细胞瘤,应检测TP53变异。
表格汇总了以下内容:分子变异(表1)、关键免疫组化染色(表2)以及WHO将DNA甲基化谱列为“必需”诊断标准的肿瘤类型(表3)。在表3中,作者用星号标注了仅能通过甲基化谱分析确诊的肿瘤类型;对于该表中的其他所有肿瘤类型,NGS可作为替代检测方法。此外,任何未明确诊断的病例均可能从甲基化分析中获益。表4汇总了胶质瘤与神经节神经胶质瘤的特征性分子变异。
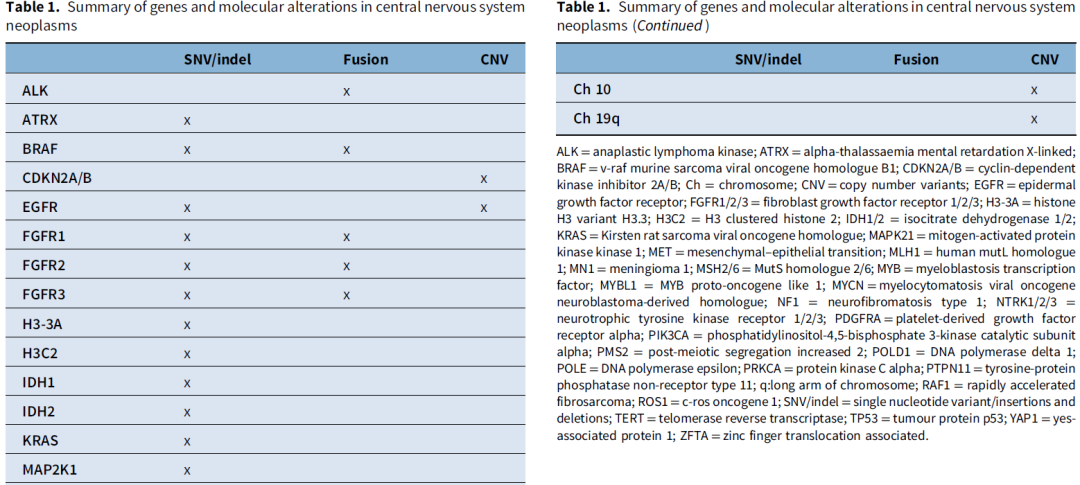
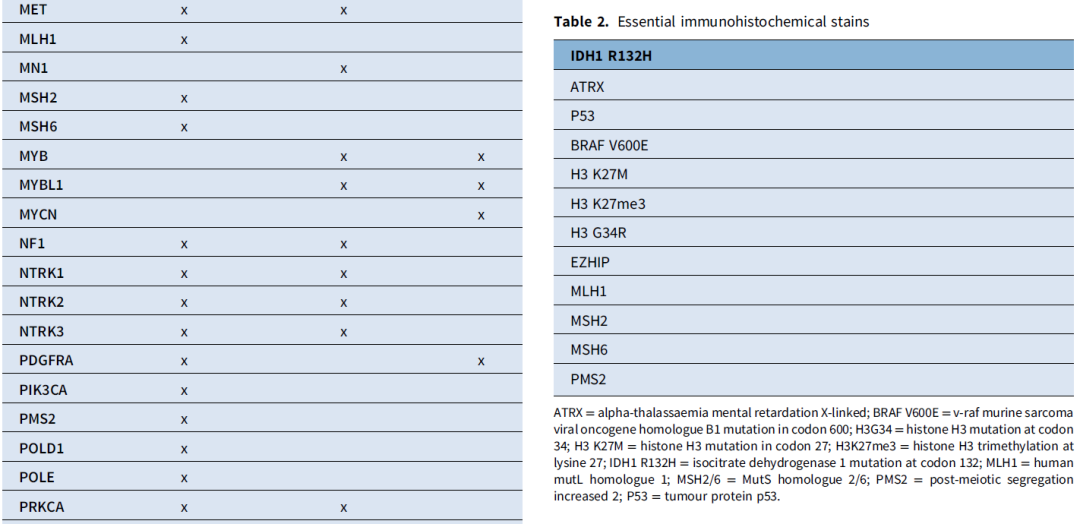
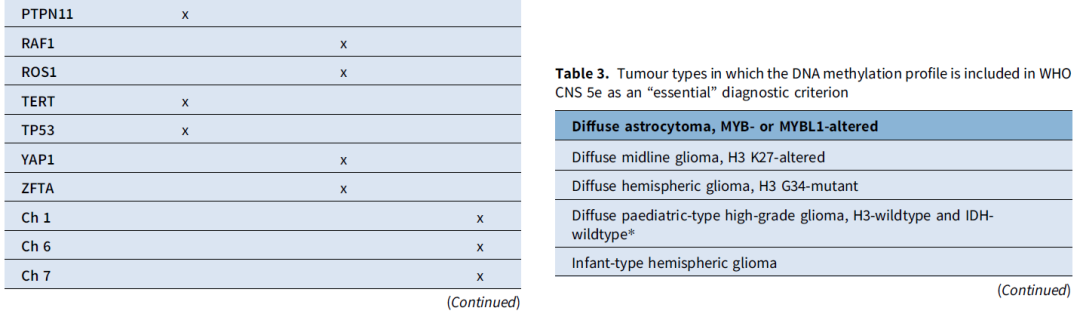
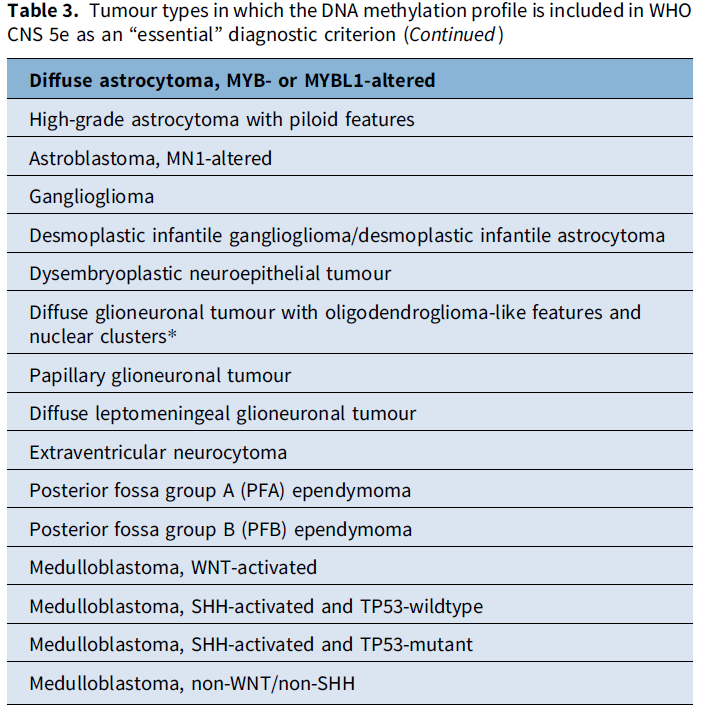
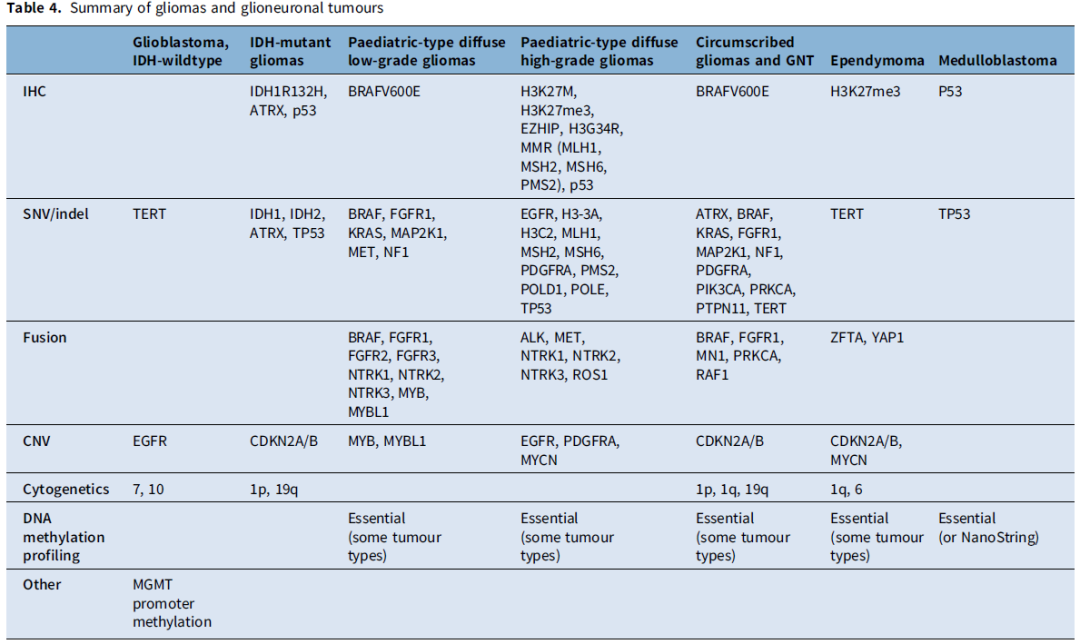
表1、2、3、4
参考文献:
Munoz, David G et al. “Molecular Testing of Central Nervous System Tumours: Recommendations of the Canadian Association of Neuropathologists.” The Canadian journal of neurological sciences. Le journal canadien des sciences neurologiques, 1-6. 28 Oct. 2024, doi:10.1017/cjn.2024.332