引言
在生命科学的前沿领域,研究人员正努力揭开人体组织与细胞的复杂面纱,而单细胞测序技术(Single-Cell Sequencing)的飞速发展为我们提供了前所未有的工具。通过单细胞技术,研究人员可以在单个细胞水平上对基因表达、调控机制和细胞异质性进行深度解析,这让我们能够全面理解生命在健康与疾病状态下的微观世界。然而,单个研究往往受限于样本量、技术偏差和个体差异,难以提供全面的细胞全景图。因此,整合多个单细胞数据集并构建具有高精度和通用性的单细胞参考图谱(Single-Cell Reference Atlas),成为当前生物医学领域的重要方向。
单细胞图谱如同生命的“细胞地图”,通过将分散的单细胞数据整合到统一的平台中,它能够更全面地展示组织内不同细胞的分布、功能和相互作用。这一图谱不仅能克服单一研究的技术与数据偏差,还能通过跨实验室、跨物种和跨技术平台的数据整合,实现对细胞异质性和组织结构的更精准刻画。例如,人类细胞图谱(Human Cell Atlas,HCA)和人类生物分子图谱项目(HuBMAP)等大型国际项目,正致力于构建全面的人体细胞图谱,为全球研究人员提供一个共享的生物学参考资源。
12月13日Nature Methods的综述 “Considerations for building and using integrated single-cell atlases”,讨论了构建和应用单细胞参考图谱的关键步骤与挑战,包括数据准备、预处理、批次效应消除、元数据整合及图谱评估与共享等方面。研究人员指出,单细胞图谱的构建不仅依赖于高质量的数据,还需要科学的整合方法和严格的质量控制,以确保图谱的准确性和可用性。此外,图谱的共享与持续更新,也将推动其成为一个不断演进的资源,为新数据提供参考、为疾病研究提供新的视角。
从绘制健康组织的细胞分布,到揭示疾病状态下细胞的动态变化,单细胞图谱将成为理解生命系统复杂性的关键工具。它不仅能够帮助研究者解析细胞类型与基因调控之间的关系,还将推动新一代疾病诊断与治疗方法的发展,为精准医学提供有力支撑。

我们的身体究竟是如何由千亿个细胞精密协作而运作的?每一个细胞,仿佛是微观世界里的“精密工匠”,通过基因的表达和分子信号的调控,共同维持着生命的平衡。然而,传统的研究方法将成千上万个细胞的平均数据汇总分析,掩盖了单个细胞的独特性,难以揭示隐藏在细胞群体背后的“个性”与“多样性”。
单细胞测序技术(Single-Cell Sequencing) 的问世,打破了这一局限。这项技术如同高倍显微镜一般,将我们带入单个细胞的世界,使研究人员能够逐一解析每个细胞的基因表达、调控机制以及细胞间的差异。单细胞技术让我们能够在单一细胞层面上观察细胞的“个体差异”,真正捕捉生命系统的复杂性。例如,通过单细胞RNA测序(scRNA-seq),研究人员能够识别组织中的稀有细胞群体,描绘细胞分化的轨迹,甚至发现疾病状态下的细胞变化。
然而,单个研究由于样本量有限、实验设计差异以及技术偏差,往往只能窥探细胞世界的一角。为了解决这一问题,研究人员提出了构建单细胞参考图谱(Single-Cell Reference Atlas) 的概念。单细胞图谱通过整合多个实验室、多个研究的单细胞数据,形成一个覆盖广泛细胞类型、组织状态和个体差异的“细胞地图”,为生命科学和医学研究提供了全新的工具。例如,人类细胞图谱(Human Cell Atlas, HCA) 项目正致力于绘制人体所有细胞的全景图,试图全面解析细胞在健康与疾病状态下的功能与相互作用。
这一“细胞地图”的诞生意义非凡。它不仅可以帮助研究人员深入了解器官发育、细胞分化和疾病发生的机制,还能为精准医学提供重要的基准,推动个体化诊断与治疗的发展。
从数据到图谱:如何拼凑细胞的全景图?
构建单细胞参考图谱,就像拼凑一幅复杂的“细胞全景图”,每一块拼图都是来自不同实验室、不同个体和不同组织的单细胞数据。为了让这幅图准确、全面且具有实用性,研究人员必须从一开始就精心设计与筛选,确保每一步都精准无误。
第一步:明确图谱的目标
图谱的构建并非“万能拼图”,而是要根据特定的科学问题来确定研究焦点。例如,如果目标是研究衰老过程中的细胞变化,那么数据选择时就需要覆盖从年轻到老年各个年龄段的样本。如果目标是疾病状态下的细胞功能异常,就需要纳入健康对照组与患者组的数据。因此,目标设定决定了图谱的应用范围和价值。
第二步:数据的精挑细选
优质的数据是构建高质量图谱的基础。研究人员在数据选择时会重点考量几个关键因素:
数据多样性:确保数据来源于不同个体、不同组织,甚至不同技术平台,尽可能覆盖广泛的细胞群体和生物学差异。
元数据的完整性:如年龄、性别、健康状态等样本信息,为后续分析提供重要背景支撑。
数据质量:数据中的细胞数量、测序深度以及低质量细胞的比例都会影响整合的结果。
研究人员强调,数据的技术差异(如实验室操作、样本处理和测序技术)是无法避免的,但通过合理的批次效应控制和数据标准化,这些技术偏差可以被有效消除,保留真正的生物学信号。
第三步:数据质量的严格把控
在数据进入图谱之前,必须经过质量控制和预处理。例如,会剔除测序深度不足、污染严重或标注不完整的细胞数据。这一环节不仅保障了数据的可用性,还为后续的整合和分析提供了可靠的基础。
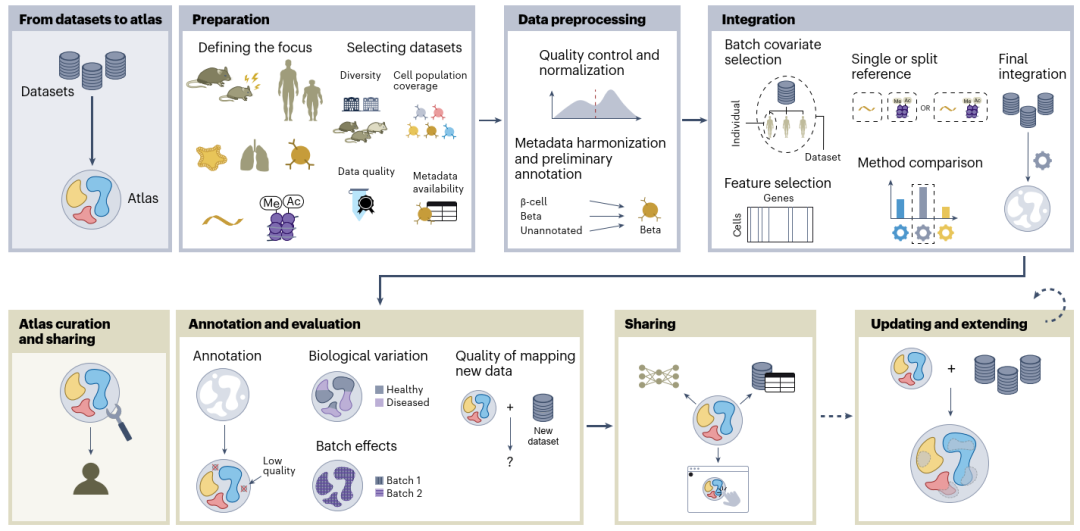
构建参考图谱的工作流程(Credit: Nature Methods)
图谱构建阶段(From datasets to atlas)
数据准备(Preparation):明确图谱的目标和研究重点,例如是否针对特定器官、细胞类型或疾病状态。精选符合目标的数据集,确保数据的多样性、质量和元数据(Metadata)完整性。
数据预处理(Data Preprocessing):包括元数据协调(Metadata Harmonization)和初步数据注释,保证不同数据集之间的格式和命名规则一致。对原始数据进行质量控制(如去除低质量细胞)和标准化处理,确保数据具备可整合性。
数据整合(Integration):通过选择合适的批次协变量(Batch Covariate),去除批次效应,保留生物学变异。筛选关键特征(基因),并应用整合算法,将不同来源的数据集统一投射到共享的空间中,生成最终的整合图谱。
图谱管理与共享阶段(Atlas curation and sharing)
图谱注释与评估(Annotation and Evaluation):对整合后的图谱进行高质量的细胞标注,确保标注的准确性和一致性。通过生物学验证评估图谱质量,检查残余批次效应,确保数据整合的可靠性。
图谱共享(Sharing):将构建好的参考图谱通过共享平台(如CELLxGENE、Single Cell Portal)发布,方便全球研究者访问和使用。数据共享包括原始数据、元数据及整合模型等,使图谱易于下载、查询和分析。
图谱更新与扩展(Updating and Extending):新的数据集可以通过Query-to-Reference Mapping快速映射到现有图谱上,扩展图谱的覆盖范围。当积累足够的新数据时,图谱可以被重新整合,以保持其与时俱进,反映最新的生物学信息。
数据的磨合与整合:如何克服批次效应这道坎?
想象一幅画,由不同的艺术家使用不同的画布、颜料和技巧创作而成。如果将这些作品拼接在一起,可能会出现色调不一、风格迥异的问题。对于单细胞参考图谱的构建而言,这种“差异”就是批次效应(Batch Effects)。批次效应是指由于技术、实验室操作、样本来源等因素导致的数据间非生物学差异,它严重干扰了数据的整合,掩盖了真正的生物学信息。
批次效应的来源:无法回避的技术差异
批次效应的产生有多种原因:
技术因素:不同实验室可能使用不同的单细胞测序平台和流程,导致数据偏差。
样本处理:如组织获取方法(活体采样、手术切片或尸检)和细胞解离技术的不同,会影响细胞存活率和捕获效率。
个体差异:样本来源于不同个体,健康状态、年龄、性别等生物学差异也可能被误认为批次效应。
研究人员指出,数据整合的目标是除这些技术性噪音,同时保留真实的生物学变异。这一过程既充满挑战,也需要科学的策略。
方法选择:如何找到最佳“磨合剂”?
研究人员通常会通过以下手段解决批次效应:
批次协变量选择:定义哪些变量是需要消除的批次效应,比如样本批次或测序平台。通过调整整合方法,可以在去除技术偏差的同时保留生物学差异。
特征筛选:在整合之前,筛选出对生物学信号最有价值的基因(如“高变异基因”),去掉那些受到批次影响的无关基因。
数据标准化:采用先进的算法(如Harmony、scVI等),对数据进行归一化处理,最大限度地去除批次效应,使不同来源的数据“说同一种语言”。
实现数据的无缝整合
通过这些方法,研究人员成功地将不同来源、不同条件下产生的单细胞数据整合到统一的坐标空间中。这就像一支训练有素的合唱团,消除了不和谐的音符,呈现出流畅的“生物学交响乐”。
克服批次效应不仅让单细胞参考图谱更加精准可靠,也使其具备了更广泛的应用价值。
一张图谱胜千言:单细胞图谱如何改变医学研究?
揭示细胞异质性:健康组织的微观全景
每个组织看似均一,实则由多种细胞协同运作,这种“异质性”对维持健康至关重要。单细胞图谱通过解析成千上万个细胞的基因表达,将不同类型、不同状态的细胞精确分类,绘制出组织内的“细胞生态”。例如,图谱构建揭示了不同年龄阶段或器官特定的细胞群体,提供了关于组织发育和稳态维持的宝贵信息。这些数据不仅让研究人员能够识别稀有的细胞群体,还能探究细胞之间的相互作用和功能分工。
发现疾病中的细胞状态:揭开病理变化的面纱
疾病的发生往往伴随着细胞的异常变化,而单细胞图谱正是捕捉这些变化的利器。在肿瘤研究中,研究人员发现某些癌症特有的细胞状态和免疫逃逸机制;在慢性炎症或纤维化疾病中,细胞图谱揭示了特定细胞类型的增殖或功能失调。例如,通过对健康与疾病样本进行对比分析,研究人员能够确定哪些基因表达的改变是疾病标志,从而找到潜在的生物标志物(Biomarkers)。这些标志物不仅可以用于早期诊断,还能帮助筛选出新的治疗靶点。
助力精准医学:量身定制的治疗方案
单细胞图谱还为个体化医疗奠定了基础。通过整合大规模患者数据,研究人员可以根据细胞特征将患者进行分组,实现疾病的分子分型。这种分型有助于医生为每位患者制定量身定制的治疗方案。例如,在免疫治疗中,单细胞图谱可以帮助识别反应良好的患者群体,提高治疗效果,减少不必要的副作用。
不断更新的细胞蓝图:共享与扩展,让图谱“活起来”
单细胞参考图谱(Single-Cell Reference Atlas)并非一成不变的静态资源,而是一幅不断扩展、持续进化的“细胞蓝图”。它的价值不仅体现在整合已有数据,更在于通过数据共享和动态更新,持续吸收新发现,成为全球的共同资源,推动生命科学的前行。
数据共享:开放平台的力量
共享,是单细胞图谱得以“活起来”的关键。研究人员认识到,单一研究的局限性无法满足揭示复杂生物学规律的需求,因此,全球合作与数据开放变得尤为重要。目前,已有多个数据共享平台崭露头角,如人类细胞图谱(HCA) 数据库、CELLxGENE 和Single Cell Portal 等。这些平台为研究者提供了直观的数据访问和下载功能,方便进行图谱的查询、分析和重用。
研究指出,数据共享的标准化至关重要。例如,使用统一的元数据命名规则和生物学术语(如标准的细胞类型命名)不仅能提高数据的一致性,还能确保跨研究间的数据整合更加顺畅。通过这些开放的平台,研究人员可以随时将新数据映射到已有的图谱中,填补细胞类型、个体差异或疾病状态的空白。
动态更新:让图谱与时俱进
新数据的不断涌现推动着单细胞图谱的扩展与更新。研究人员可以通过两种方式来让图谱“成长”:
映射新数据:新单细胞数据可被快速映射到现有图谱上,通过Query-to-Reference Mapping技术,研究人员可以在图谱框架中识别新细胞类型或状态。
重新整合与扩展:当积累了足够的新数据时,可以重新整合所有数据,更新图谱的结构,确保其覆盖更广泛的生物学条件。
这种持续更新的特性,使单细胞图谱具备了“生命力”。例如,加入不同人群的样本数据(如年龄、性别、遗传背景的多样性)可以让图谱更具普适性,进而揭示更复杂的生物学现象。同时,新的疾病状态、细胞标记物或多组学数据的引入,也让图谱的应用范围不断拓展。
全球共建,共享未来
单细胞图谱的共享与更新,标志着科学研究正在迈向开放与协作的新时代。它不仅帮助研究人员节省了数据采集和分析的时间,更推动了跨学科、跨领域的创新。每一位研究者都可以是图谱的“建设者”,也可以是图谱的“使用者”,共同推动生命科学与医学的突破。
单细胞图谱正在让精准医学从愿景走向现实。从精准诊断到靶向治疗,再到个体化医疗,这张不断完善的“细胞地图”,将引领我们走向一个更健康、更精准的医学新时代。每一个细胞的真相,都将照亮生命科学的未来。
参考文献
Hrovatin, K., Sikkema, L., Shitov, V.A. et al. Considerations for building and using integrated single-cell atlases. Nat Methods (2024). https://doi.org/10.1038/s41592-024-02532-y.