实际上,我们通常讲的肺癌是原发于肺的恶性肿瘤,主要分为两大类:非小细胞肺癌和小细胞肺癌。然而,肺部肿瘤并非只有这两种,还可进一步细分为多种不同类型(见下表),其治疗方法有很大差异。病理诊断作为肿瘤诊断的“金标准”,可以通过免疫组化、分子病理检测等方式对其进行精准区分,帮助临床医生对症治疗。
肺部肿瘤第5版WHO分类


肺部肿瘤相关免疫组化指标
一、肺腺癌常用免疫标记物
TTF-1
-
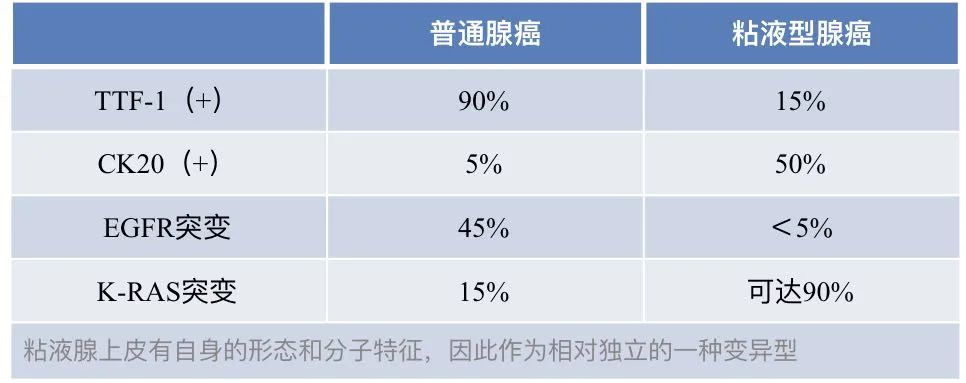
TTF-1(甲状腺转录因子-1)表达于甲状腺滤泡上皮和肺泡上皮细胞的细胞核中。与肿瘤分化程度正相关,分化越差(如浸润性粘液腺癌、胶样腺癌)则越可能表达缺失;
-
75%-85%肺腺癌表达;
-
TTF-1也表达于肺神经内分泌肿瘤(NETs),包括类癌(典型类癌TC、非典型类癌AC)、50%的大细胞神经内分泌癌(LCNEC)及90%的小细胞肺癌(SCLC);
-
鳞癌通常不表达TTF-1(故TTF-1主要用于腺癌、鳞癌鉴别,不能鉴别肺腺癌和NETs);
-
在肺的转移性腺癌中,除了甲状腺癌几乎全表达外,少量子宫内膜、子宫颈、卵巢、乳腺和结直肠的腺癌也表达。所有类型肾细胞癌均不表达。
Napsin A
-
Napsin A(新天冬氨酸蛋白酶 A)在正常肺泡 II 型上皮细胞和近端与远端肾小管中表达,70%-90%的肺腺癌表达,其敏感度和特异度均优于TTF-1;
-
与TTF-1相似,Napsin A在肺腺癌中表达也与组织学类型、分化程度具有相关性;
-
约 3% 的肺鳞癌阳性,肺神经内分泌肿瘤阴性(可用于肺腺癌和NETs鉴别);
-
部分转移性肺癌,如肾细胞癌、少部分甲状腺乳头状癌、子宫内膜腺癌、卵巢腺癌、胆管细胞癌等TTF-1和Napsin A是目前诊断肺腺癌最优秀的抗体组合之一。
CK7(cytokeratin-7)
-
敏感性高,几乎100%肺腺癌表达;
-
特异性差,30%-70%肺鳞癌阳性;
-
广泛表达于乳腺、胃、卵巢、胰腺、子宫、尿路上皮等多种器官和部位发生的腺癌;
-
肺腺癌鉴别诊断时,需与TTF-1、NapsinA联合应用。
肺泡表面糖蛋白(SP-A、SP-B)
-
主要见于分化程度较高的具有Ⅱ型肺泡上皮细胞/Calar细胞分化特征的腺癌(分化较好);
-
在分化差的肺腺癌中,常常表达缺失。
Cam5.2(CK8、CK18)
-
几乎100%的肺腺癌(+);
-
约35%的肺鳞癌和20%大细胞肺癌(+);
-
特异性低,人体几乎所有类型的腺癌均表达。
二、肺鳞癌常用免疫标记物
p63/p40
p63
-
超过 90% 的肺鳞癌细胞核强阳性,但有 10%-33% 的肺腺癌呈局灶性低水平表达;
-
在内分泌肺癌中:类癌<6%,大细胞肺癌13.5-18%,小细胞肺癌22%。
p40
-
P40是P63蛋白的亚型之一,阳性定位在细胞核。其被认为是特异性和敏感性最高的鳞癌标志物;
-
敏感性类似p63,>96.8%鳞癌(+);
-
特异性优于p63,腺癌基本不表达(3-5%),且常局灶表达;
-
内分泌肿瘤中,类癌不表达,大细胞肺癌3.6%;
-
2.4%间皮瘤表达。
CK5/6、DSG3
CK5/6
-
CK5/6正常时主要表达于鳞状上皮细胞、导管上皮基底细胞、肌上皮细胞和间皮细胞中;
-
75%~100%的肺鳞癌有表达,且与分化、分级无关;
-
2%~33%的肺腺癌可表达CK5/6,但常呈局灶性低水平表达;
-
75%~100%的胸膜上皮样恶性间皮瘤也表达。
DSG3
-
DSG3(桥粒芯糖蛋白)在85%~90%的肺鳞癌表达;
-
肺腺癌几乎不表达(<2%)。
92.6%鳞癌可通过CK5/6、DSG3组合诊断
>85%肺腺癌、鳞癌可通过DSG3和Napsin A区别
三、神经内分泌癌的常用免疫标记物
CgA、Syn和CD56
神经内分泌肿瘤包括典型类癌,非典型类癌、大细胞癌及小细胞癌;大细胞癌的诊断常需要结合免疫标志物,其余主要依靠形态学特征。CgA、Syn和CD56是最常用的神经内分泌标志物组合,其中CgA特异性最强,CD56最为敏感但缺乏特异性。
CgA
-
CgA(嗜铬素A)是人类肾上腺髓质中含量最高的一种可溶性酸性蛋白,其广泛存在于神经元、神经内分泌细胞及其肿瘤细胞中;
-
其主要用于标记神经内分泌肿瘤,如垂体肿瘤、胰岛细胞瘤、嗜铬细胞瘤、甲状腺髓样癌、类癌等。
Syn
-
Syn(突触素)主要存在于神经元突触前囊泡膜、肾上腺髓质、颈动脉体及皮肤和内脏的神经性和上皮性神经内分泌细胞;
-
此抗体主要用于标记神经内分泌细胞及其肿瘤。
CD56
-
神经细胞黏附分子(NCAM,CD56)表达于 NK 细胞和小部分活化的 T 淋巴细胞及神经外胚层起源的细胞;
-
此抗体是NK细胞淋巴瘤的标志物,也是肺神经内分泌肿瘤首选的特异性标志物。
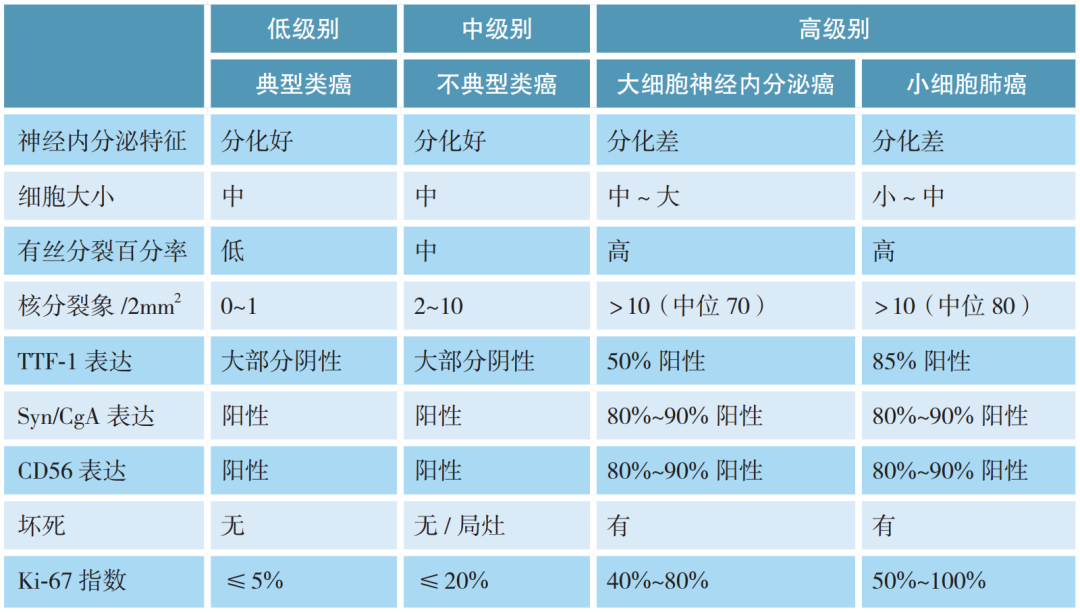
不同类型肺神经内分泌肿瘤特点
Ki-67(增殖指数)
-
Ki-67(增殖指数)是与细胞增殖有关的抗原,其功能与有丝分裂密切相关。Ki-67标记的是处于增殖周期中的细胞,其阳性率越高,肿瘤生长越快,组织分化越差,对化疗也越敏感;
-
Ki-67对肺神经内分泌癌具有诊断和分级双重作用。如典型类癌的Ki-67增殖指数≤5%,属于低级别,非典型类癌为5%~20%,属于中级别,大细胞肺癌通常≥60%,属于高级别。
四、肺腺癌与肺鳞癌的鉴别
1.TTF-1、Napsin A、CK5/6和p63(p40)是目前鉴别肺腺癌和鳞癌最常用的抗体组合。
2.大多数情况下,TTF-1/P63组合基本可以满足对肺鳞癌和肺腺癌的鉴别,其在腺癌和鳞癌均是一个阳性一个阴性。
特殊情况下:
(1)如果TTF-1/p63均阳性,倾向于诊断腺癌,因为p63可以在腺癌中表达,而TTF-1几乎不在鳞癌中弥漫性表达(>50%的肿瘤细胞表达);
(2)如果TTF-1/p63均阴性,则仍然怀疑腺癌,因为TTF-1在差分化腺癌中缺失表达的现象较常见,而p63在鳞癌中的表达非常稳定。
3.所有鳞癌标志物均不能鉴别转移性鳞癌、上皮癌甚至包括肉瘤和大细胞淋巴癌(P63可阳性)。而p40在上述大细胞淋巴瘤中不表达,因此选择p40代替p63能有效避免将肺或纵隔的大细胞淋巴瘤误诊为鳞癌。
五、肺原发性肿瘤与继发性肿瘤的鉴别
肺原发性腺癌 vs 转移性腺癌
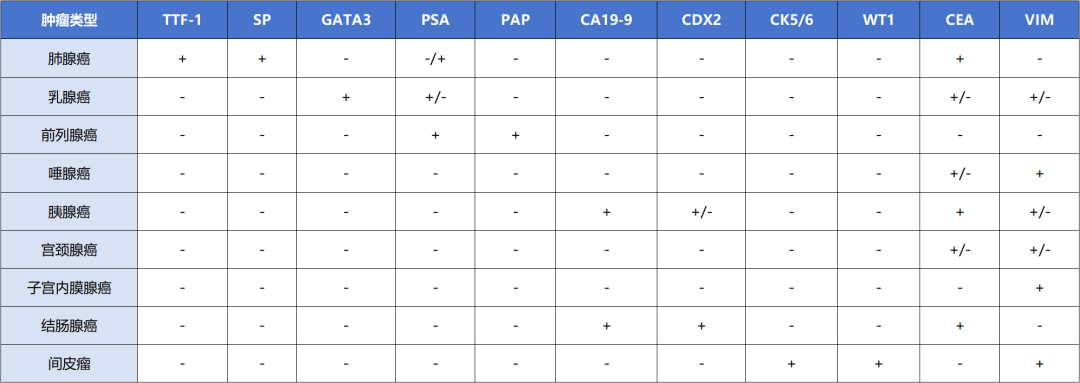
1.腺癌可能来自胃肠道、乳腺、卵巢、子宫内膜和前列腺等器官,未知原发部位的转移性腺癌占所有肺癌的3%~5%。
2.与转移性结直肠腺癌鉴别,利用肺腺癌特异性的标志物如CK7、TTF-1和Napsin A,以及肠癌特异性标志物如CK20、CDX2。
3.GATA-3是乳腺癌的特异性标志物。
4.Pax-8(肺腺癌不表达)、ER和PR表达则支持卵巢浆液性腺癌的诊断。
5.Pax-8、TG表达有助于甲状腺癌的诊断。
6.PAS和PASP表达则强烈支持前列腺癌的诊断。
肺原发性鳞癌 vs 转移性鳞癌鳞癌
可能来自食管、头颈部、皮肤等部位,其他还包括膀胱等泌尿系统的尿路上皮癌。目前尚无有效的标志物(组合)将肺原发性鳞癌与转移性鳞癌鉴别。
六、肺癌与胸膜上皮样恶性间皮瘤的鉴别
1.尚缺乏100%的特异性标志物,因此应至少选择2个间皮和2个上皮标志物。
2.根据抗体的敏感度和特异度,间皮瘤最好的标志物为钙视网膜蛋白(Calretinin)、CK5/6、Wilms肿瘤基因1(Wilms tumour gene-1,WT-1)、MC和D2-40。
七、大细胞肺癌的鉴别
根据WHO定义,大细胞肺癌一种未分化的非小细胞肺癌,其在细胞学和组织结构及免疫表型等方面缺少小细胞癌、腺癌及鳞癌的特征,且必须是手术切除标本才能做出大细胞癌的诊断。免疫组化和粘液染色对诊断大细胞癌是必要的。不难看出,大细胞肺癌是一类排他性诊断,指的是除外小细胞癌、腺癌和鳞癌之后的排除性诊断。
肺部肿瘤分子病理检测
NSCLC推荐检测必检基因为:
EGFR、ALK、ROS1、RET、BRAFV600和MET14外显子跳跃突变、KRAS、NTRK。
EGFR
表皮生长因子受体(EGFR)是一种跨膜酪氨酸激酶受体,在癌细胞的增殖和生长中起着重要作用。经典的EGFR突变包括19号外显子缺失(约占45%)和21号外显子L858R突变(约占40%)。EGFR基因的突变在亚洲人种所患的非小细胞肺癌中最常见,特别是无吸烟史者,如果罹患肺癌,有50-60%都能检测出这种突变,中国患者突变率30-40%,女性患者突变概率更高。
ALK
间性淋巴瘤激酶(ALK)是肺癌发展中的一个重要驱动基因,常被称为“钻石突变”。ALK融合突变与EGFR突变相比,其突变率较低,在肺腺癌患者中的发生率约为5-10%,在中国的非小细胞肺癌中约为5.6%,既往无吸烟史的年轻肺腺癌患者中多见。
ROS1
ROS1基因融合是非小细胞肺癌(NSCLC)中的一个重要驱动基因,并且是当前NSCLC靶向治疗的热点之一。ROS1重排虽然罕见,但ROS1和间变性淋巴瘤激酶(ALK)之间存在同源性、ROS1和ALK阳性NSCLC之间存在相似性,因此ALK抑制剂被重新用于治疗ROS1阳性疾病。
RET
RET基因编码的RET蛋白是一种带有酪氨酸激酶活性的单通道跨膜糖蛋白受体,存在于细胞膜上。RET基因融合在NSCLC患者中的发生率约为1%~2%,属于罕见靶点,但由于我国肺癌患病群体基数较大,因此,这种基因突变在临床中并不算罕见。
BRAF V600
BRAF基因编码丝氨酸/苏氨酸蛋白激酶,属于RAF家族,其在恶性肿瘤中的突变频率为8%。BRAF基因突变的激活通常与EGFR突变或ALK重排相互排斥,对非小细胞肺癌(NSCLC)起到替代致癌驱动因素的作用。BRAF突变是 NSCLC 中的罕见突变,占肺腺癌的 2%。这一变异常见于从不吸烟者、女性和侵袭性组织学类型(微毛细管)。此外,BRAF V600E 突变大多与该肿瘤中存在的大多数药物存在明显的耐药性。
MET14外显子跳跃突变
MET是近年来被认为具有重要靶向治疗价值的致癌驱动基因。MET14外显子跳跃突变是一种能够独立致癌的驱动基因,在NSCLC中,其突变频率在KRAS、EGFR、ALK之后,位列第四,发生率为3%-4%。
KRAS
KRAS突变存在于大约25%的人类癌症中,KRAS突变约占非小细胞肺癌突变的25%,KRAS G12C突变约占非小细胞肺癌突变的13%。与从不吸烟者相比,KRAS G12C突变在有吸烟史的NSCLC患者中更为常见,并且通常伴随更高的肿瘤突变负荷。
NTRK
NTRK表示神经营养受体酪氨酸激酶。NTRK基因家族包括NTRK1、NTRK2和NTRK3,它们分别编码TRK(原肌球蛋白受体激酶)家族的受体蛋白TRKA、TRKB和TRKC,统称为TRK家族蛋白。NTRK基因融合已被确定为泛实体瘤成人和儿童患者的致癌驱动因素。总体而言,具有NTRK基因融合的实体瘤很少见,整体阳性率为0.3%。