免疫检查点抑制剂(ICIs)由于其丰富的淋巴细胞浸润能力而成为治疗肝细胞癌(HCC)的一种有希望的治疗方法。然而,由于肿瘤微环境中存在多种免疫抑制因子,一些HCC患者对ICI治疗反应不佳。
2024年4月12日,天津医科大学李祥春及Yu Jinpu共同通讯在Cell Reports Medicine 在线发表题为“Macrophage-coated tumor cluster aggravates hepatoma invasion and immunotherapy resistance via generating local immune deprivation”的研究论文,该研究证明,巨噬细胞包被肿瘤簇通过产生局部免疫剥夺加重肝癌侵袭和免疫治疗抵抗。
巨噬细胞包被肿瘤集群(MCTC)在HCC中具有独特的空间结构组织,与来自3个内部队列和2个独立外部验证队列的572例HCC患者的无复发生存率和总生存率降低相关。从机制上讲,肿瘤源性巨噬细胞相关凝集素Mac-2结合蛋白(M2BP)诱导MCTC形成,并将免疫能力细胞困在MCTC边缘,诱导肿瘤内细胞毒性T细胞排斥和局部免疫剥夺。用Mac-2拮抗剂阻断M2BP可能是阻止MCTC形成、增强T细胞浸润的有效途径,从而提高HCC中ICI治疗的疗效。

肝细胞癌(HCC)是一种侵袭性很强的肿瘤,术后复发率高虽然酪氨酸激酶抑制剂已被确定用于初级和次级治疗,但它们对总生存期(OS)的改善有限。美国食品和药物管理局(FDA)加快批准免疫检查点抑制剂(ICI),包括PD-1和CTLA-4抗体,有望改变晚期HCC的管理。然而,它在OS方面没有统计学上的显著改善。因此,迫切需要揭示HCC免疫治疗耐药的分子事件,并开发新的策略来提高ICI治疗的疗效。
HCC的ICI耐药是多方面的,但最关键的方面之一涉及肿瘤微环境(TME)内复杂的相互作用。之前的研究表明,肿瘤相关巨噬细胞(TAMs)在HCC TME中普遍存在,并已被证明通过microRNA介导的机制促进HCC细胞的迁移和侵袭。此外,TAMs有助于TME内的免疫抑制环境,正如在各种癌症中所见,较高的TAMs密度与预后不良和ICI耐药性增加相关。
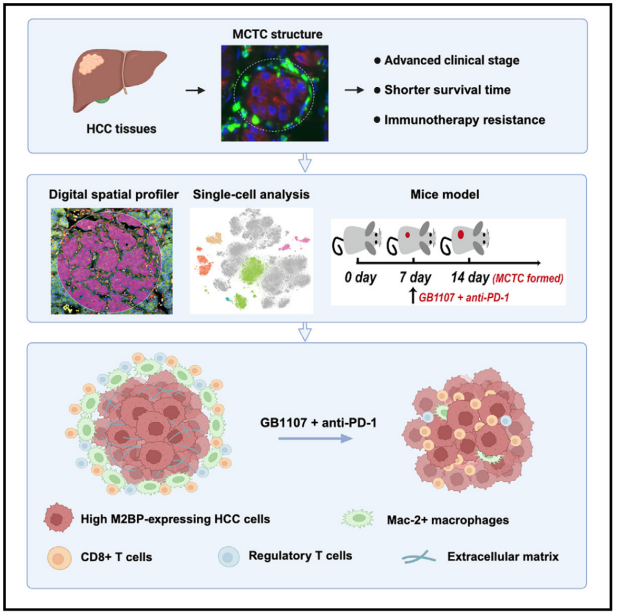
机理模式图(图源自Cell Reports Medicine )
新出现的证据表明,肿瘤内免疫细胞的空间结构对癌症的进展至关重要。例如,癌症相关成纤维细胞和癌细胞之间的结构性相互作用涉及到肺癌细胞的迁移和T细胞的排除。研究人员假设,在HCC中,TAMs的独特空间排列可能通过改变免疫细胞的肿瘤内分布来影响ICI耐药性。
该研究采用先进的高复合体分子谱发现了一种称为巨噬细胞包被肿瘤簇(MCTC)的新型空间结构,它预示着预后差和更具侵袭性的HCC。值得注意的是,尽管MCTC阳性(MCTC+) HCC被定性为“免疫热”肿瘤,但由于排除了肿瘤内的细胞毒性T细胞,因此经常抵抗ICIs。通过使用Mac-2拮抗剂抑制巨噬细胞相关凝集素Mac-2结合蛋白(M2BP),可以阻止MCTC的形成,恢复T细胞的浸润,为提高HCC中ICI的治疗效果提供了一条有希望的途径。
原文链接:
https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(24)00174-5