帕博利珠单抗是一种抗PD-1免疫检查点抑制剂,FDA批准用于治疗经过前期治疗但无法切除或转移的MSI-H/dMMR/TMB-H实体瘤,包括前列腺癌,在前列腺癌患者中,约2-3%的转移性去势抵抗性前列腺癌患者具有MSI-H/dMMR表型,可以观察到临床活性,然而,在未经生物标志物选择的患者中,使用纳武利尤单抗、帕博利珠单抗和阿替利珠单抗的临床获益有限,镭-223是一种放射性药物,可累积在骨骼转移灶,释放α粒子,诱导双链DNA断裂导致肿瘤细胞死亡,α粒子辐射可诱导免疫原性细胞死亡,因此与免疫治疗联合具有潜力,预临床数据显示,与单独使用镭-223相比,镭-223联合CPI可能增强抗肿瘤免疫反应,提高疗效,然而,临床证据显示,单部位放疗联合CPI的效果有限,而多部位放疗可能更有效,该研究旨在评估镭-223联合帕博利珠单抗治疗转移性去势抵抗性前列腺癌患者的疗效。

方法
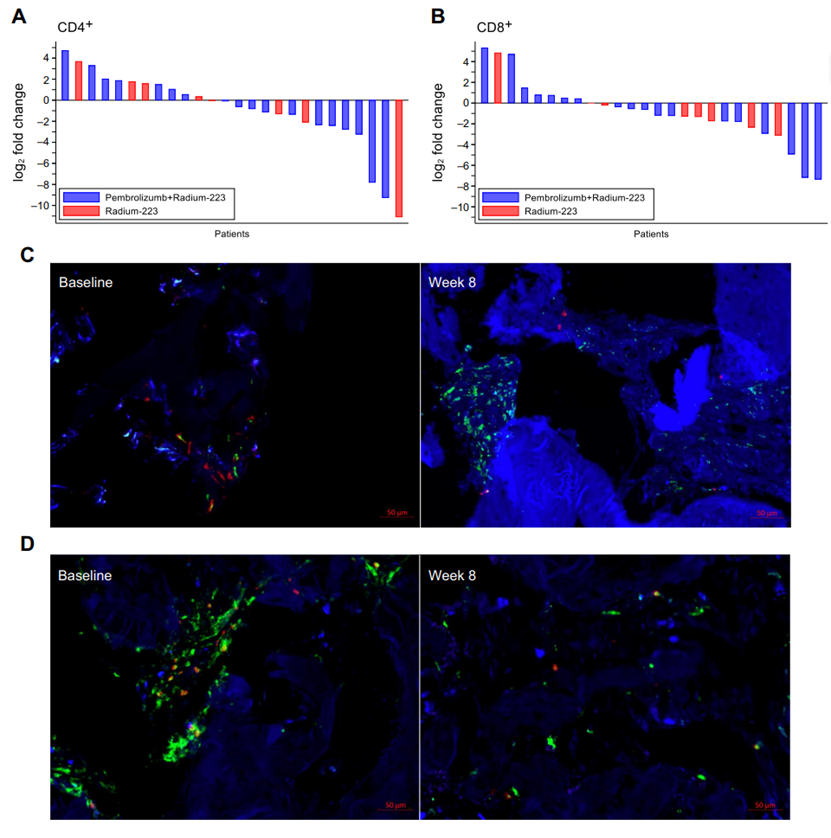
该研究纳入18岁或以上,组织学证实为前列腺腺癌,ECOG评分≤1,有骨转移证据,睾酮水平<50 ng/dL,PSA或骨扫描进展的患者,排除曾接受过radium-223或PD-1/PD-L1/PD-L2阻断治疗的患者,随机分配患者接受镭-223(55 kBq/kg 每4周)+ 帕博利珠单抗(200 mg 每3周)或单独镭-223 (55 kBq/kg 每4周),8周时重复活检,该研究的主要终点是评估治疗8周后与基线相比,两种治疗方案(镭-223加帕博利珠单抗 vs 镭-223单药)对骨转移灶活检标本中CD4+和CD8+ T细胞浸润的差异,次要终点包括安全性、影像学无进展生存期和总生存期。
研究结果
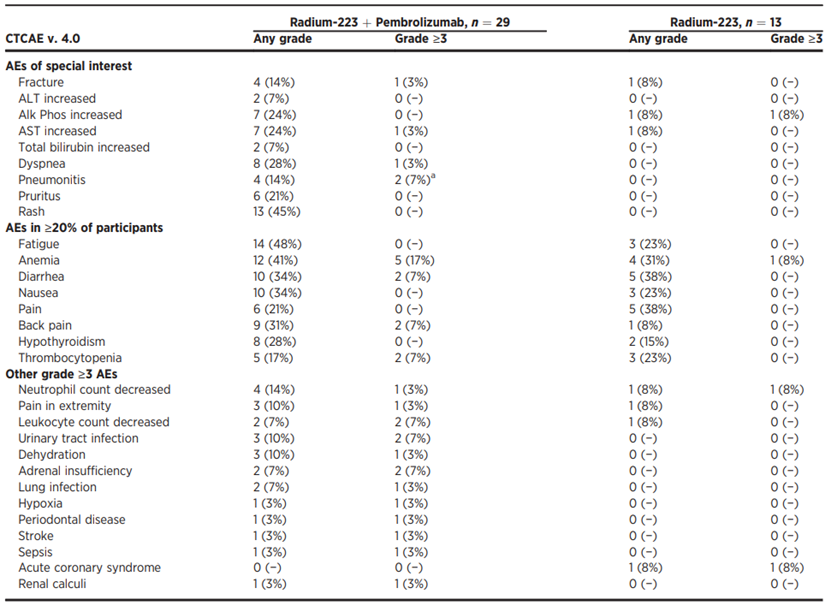
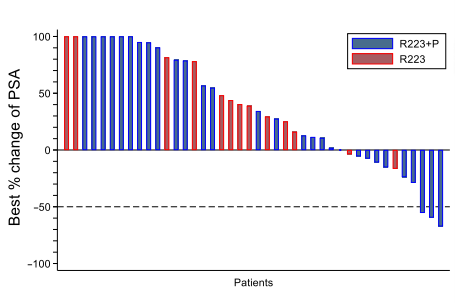
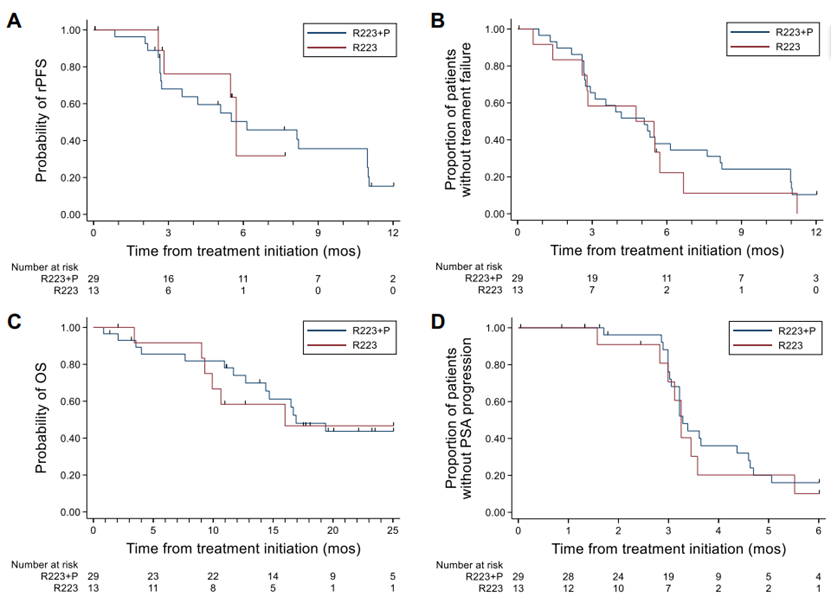
共有42例患者接受治疗并进行分析,其中29例接受R223+P治疗,13例接受R223治疗,在26例可评估患者中,R223+P组和R223组在基线和8周时CD4+和CD8+ T细胞浸润变化无显著差异。R223+P治疗组的rPFS和OS中位数分别为6.1个月和16.9个月,R223组分别为5.7个月和16.0个月,两组间无显著差异。R223+P治疗组的PSA50响应率为10%,R223组无PSA50响应,但两组间rPFS、TTF和OS无显著差异。R223+P治疗可诱导CD4+ T细胞表达CTLA-4,而R223治疗对循环免疫细胞影响有限,尽管R223+P治疗可诱导外周T细胞免疫反应,但并未增加肿瘤微环境中的T细胞浸润,且外周T细胞免疫反应的耗竭可能抑制了联合治疗的临床活性。R223+P治疗整体耐受性良好,未出现预期之外的毒性。
结论
镭-223联合帕博利珠单抗治疗转移性去势抵抗性前列腺癌患者,相较于单独使用镭-223,并没有显示出显著的生存期改善,尽管镭-223联合帕博利珠单抗治疗可诱导外周T细胞免疫反应,但并未增加肿瘤微环境中的T细胞浸润,在镭-223联合帕博利珠单抗治疗的临床应答者中,观察到基线时CD8+ T细胞和髓系细胞频率较低,治疗9周时TIM-3+ T细胞和髓系细胞频率较高,提示治疗后外周T细胞免疫反应的耗竭可能抑制了联合治疗的临床活性,该研究支持了多部位放疗联合免疫治疗可能比单部位放疗更有效的观点,为未来的多模式治疗提供了参考,总体而言,镭-223联合帕博利珠单抗治疗转移性去势抵抗性前列腺癌的疗效有限,尚需进一步优化治疗策略以提高疗效。
原始出处
Atish D. Choudhury, Lucia Kwak, Alexander Cheung, Kathryn M. Allaire, Jaqueline Marquez, David D. Yang, Abhishek Tripathi, Jacqueline M. Kilar, Meredith Flynn, Brianna Maynard, Rebecca Reichel, Amanda F. Pace, Brandon K. Chen, Eliezer M. Van Allen, Kerry Kilbridge, Xiao X. Wei, Bradley A. McGregor, Mark M. Pomerantz, Rupal S. Bhatt, Christopher J. Sweeney, Glenn J. Bubley, Heather A. Jacene, Mary-Ellen Taplin, Franklin W. Huang, Lauren C. Harshman, Lawrence Fong; Randomized Phase II Study Evaluating the Addition of Pembrolizumab to Radium-223 in Metastatic Castration-resistant Prostate Cancer.