与普通人群相比,SLE患者的死亡率仍然较高,特别是心血管疾病(CVD)和感染是导致SLE患者死亡的主要原因。此外,传统的心血管风险评估工具在SLE患者中往往低估了动脉粥样硬化的风险。SLE患者中加速的动脉硬化与传统的心血管风险因素和SLE本身的炎症效应有关。本研究旨在探索SLE患者中动脉硬化发展的新型病理生理机制和代谢途径,这些发现可能揭示新的药物靶点和治疗机会。

本研究通过文献综述的方法,探讨了SLE患者中心血管损伤的代谢途径,特别关注了糖酵解和氧化磷酸化(OXPHOS)在内皮细胞损伤中的作用。研究还分析了特定细胞在血管免疫界面的代谢适应,这些细胞促进了动脉硬化的发展。通过审查相关的动物研究和人类临床数据,进一步验证了这些代谢路径在SLE中的相关性和作用。
研究结果
-
IFN-I的作用: 研究表明,长期的I型干扰素(IFN-I)生产是SLE中导致血管损伤的关键因素。IFN-I通过促进泡沫细胞形成、激活内皮细胞和免疫细胞,以及增强炎症性白细胞在动脉中的招募,加速了动脉硬化的发展。
-
代谢重编程: SLE中的免疫细胞,尤其是单核细胞和巨噬细胞,在炎症微环境中经历代谢重编程,表现为增加的糖酵解和OXPHOS活动,这导致线粒体反应性氧种类(mROS)的增加和炎症代谢物的积累。
-
线粒体功能障碍: SLE患者表现出线粒体功能障碍和修复过程受损。这种情况不仅限于产生能量的TCA循环受损,还包括线粒体DNA(mtDNA)突变导致的原发性动脉硬化。
-
细胞间的相互作用: 在SLE中,IFN-I诱导的代谢改变增强了免疫细胞对内皮细胞的病理作用,包括通过增加scavenger receptor class A (SR-A)的表达来促进泡沫细胞的形成,以及通过影响细胞代谢来加剧内皮细胞的功能障碍和损伤。
-
代谢途径的研究前景: 研究揭示了调节特定细胞(如CD4+ T细胞和单核细胞)的代谢路径可能为预防和治疗SLE患者中的动脉硬化提供新的策略。此外,对这些细胞的代谢特性进行更深入的研究,可能帮助开发新的生物标志物和治疗靶点,以更好地管理SLE和相关的心血管疾病。
-
免疫代谢调控的复杂性: 本研究强调了在炎症相关疾病中,特别是自身免疫性疾病和心血管疾病中,线粒体作为免疫过程中的中央调节器和仲裁者的作用。这种所谓的"mito-inflammation"(线粒体炎症)现象表明,改变线粒体功能可能直接影响炎症过程。
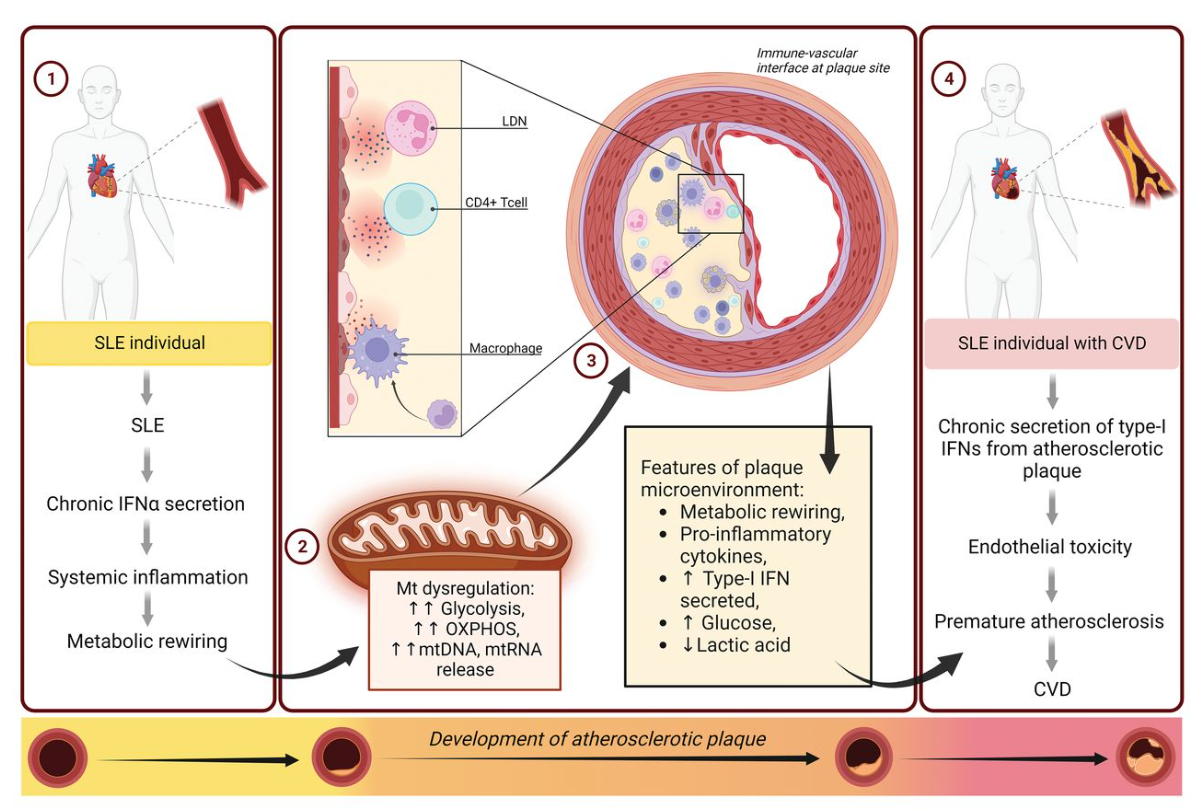
单核细胞/巨噬细胞、LDN 和 CD4+ T 细胞代谢失调对诱导 SLE 患者炎症驱动的内皮损伤的贡献
本研究发现,SLE中的心血管风险增加不完全是由传统的心血管疾病风险因素所解释,而是与深层的免疫调控和代谢紊乱密切相关。未来的研究应当关注如何通过靶向特定的代谢途径来减轻或逆转SLE病理生理过程中的有害效应。这种代谢特征化不仅有助于补充现有的疾病活动性、治疗效果和疾病分型的生物标志物,还可能在临床干预中发挥重要作用,从而为SLE患者提供个性化的治疗策略。
原始出处:
The Link Between Dysregulated Immunometabolism and Vascular Damage: Implications for the Development of Atherosclerosis in Systemic Lupus Erythematosus and Other Rheumatic Diseases. J Rheumatol. 2024 Mar 1;51(3):234-241. doi: 10.3899/jrheum.2023-0833. PMID: 38224981.