导读
为了最大限度地发挥免疫保护作用,记忆CD8+T细胞分化为具有不同监视能力的不同功能群体。这些细胞包括主要在组织中循环的效应记忆T细胞 (TEM),在淋巴器官中充当哨兵的中央记忆T细胞,以及成为全身组织永久资产的组织驻留记忆T细胞 (TRM)。TRM细胞在再感染部位能提供快速和长期的保护。具有TRM细胞特征的肿瘤浸润淋巴细胞能维持增强的效应功能,预测对免疫治疗的良好反应和预后。这些记忆CD8+T细胞亚群所在的不同环境决定了他们的功能和分化,此外细胞代谢所产生的特定的酶和代谢物也可引导记忆CD8+T细胞分化。因此,加深对使T细胞能够驻留组织的代谢策略的理解可以为增强组织和实体瘤免疫反应的新方案提供信息。
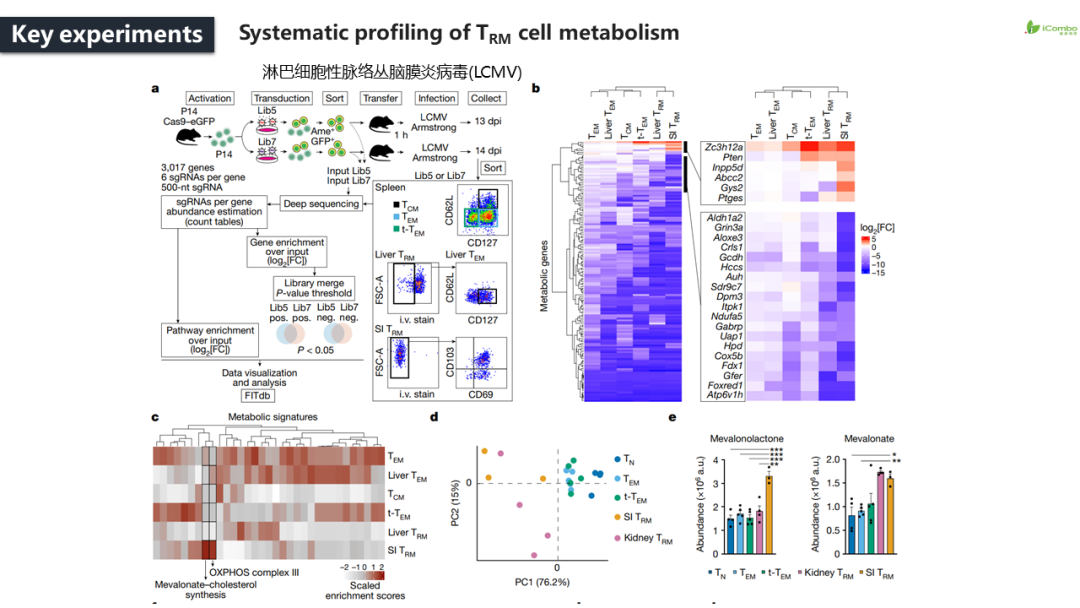
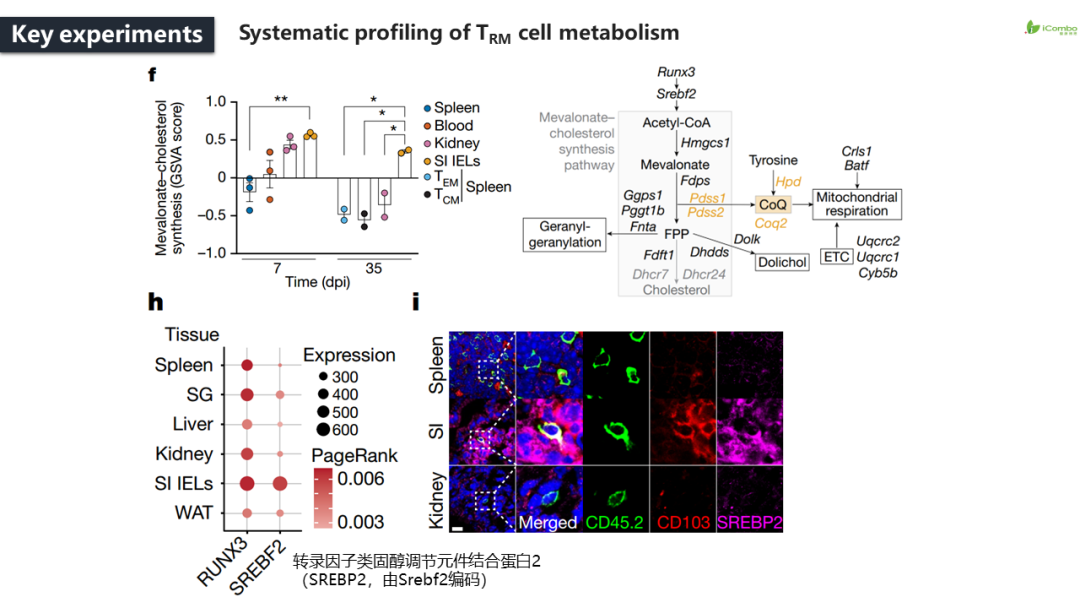
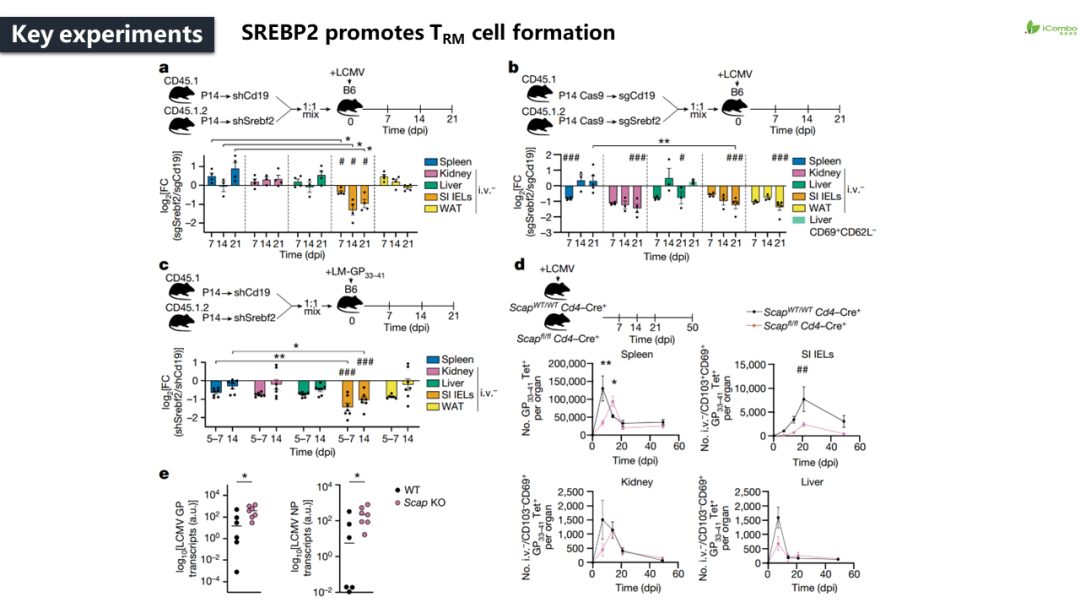
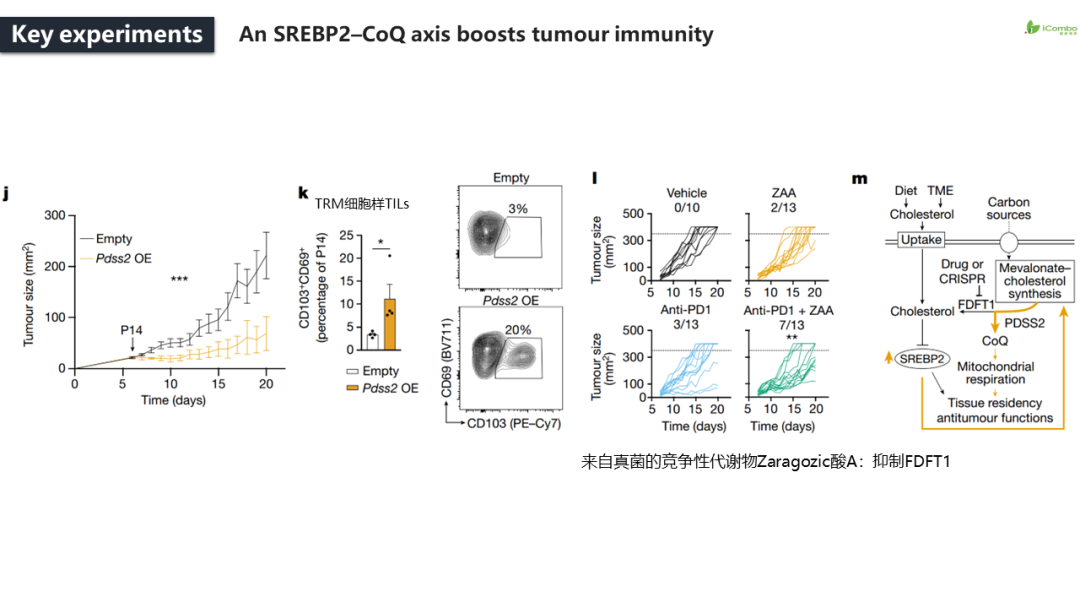
本研究结合代谢依赖性的功能筛选和对循环和驻留的记忆CD8+T细胞亚群的转录和代谢组分析,提供了一种系统的方法来确定新陈代谢如何影响记忆CD8+T细胞的形成,以响应病毒感染。研究发现记忆性CD8+T细胞部署了一系列组织驻留的适应性改变,包括由转录因子SREBP2活性增加驱动的甲羟戊酸-胆固醇途径的非甾体产物,例如辅酶Q。该细胞通过敲除Fdft1或过表达PDSS2来加强合成辅酶Q,促进线粒体呼吸和记忆T细胞的形成,并增强抗肿瘤免疫。总之,通过对TRM细胞代谢的系统探索,研究者揭示了这些程序如何在急性感染的情况下通过促进记忆CD8+T细胞的形成并增强抗肿瘤免疫(Nature.2023 Sep; 621 (7977): 179-187. doi: 10.1038/s41586-023-06483-w)。