CML
无治疗缓解(TFR)是目前慢性髓性白血病(CML)治疗的最终可达到目标,但在酪氨酸激酶抑制剂(TKl)停药后,30%~60%的患者会复发。虽然复发预测因素和TFR的先决标准现在已经得到更精确的定义,但对于不同代TKI之间的差异,特别是在TKI停药后复发的动力学方面,相关研究仍较少。
法国学者开展一项回顾性研究,分析了伊马替尼(IM)、达沙替尼(DAS)和尼洛替尼(NIL)停药后复发的动力学特征并发现,停药后IM患者的复发动力学显著快于二代TKI (NIL或DAS)。研究结果近日发表于《British Journal of Haematology》,同期发表点评文章“The Mozart effect in chronic myeloid leukaemia”(注:莫扎特现象指神童,莫扎特三岁时就开始演奏钢琴,五岁时就开始作曲,六岁时就开始巡回演出;CML的莫扎特现象,个人理解为,点评作者本以为二代TKI难以超越一代TKI伊马替尼,但法国研究或许打破了这一观点)。

研究方法&结果
该回顾性多中心分析包括Fi-LMC工作组5家中心,纳入在BCR::ABL1稳定无法测量至少2年后,首次TKI停药后复发(定义为丧失MMR)的慢性期CML患者。复发动力学的检测方法为加速失效时间(accelerated failure time,AFT)分析,即从稳定的深层分子学反应(MR4.5)到丧失主要分子学反应(MMR)(Wei LJ. The accelerated failure time model: a useful alternative to the Cox regression model in survival analysis. Stat Med. 1992;11(14–15):1871–9.)。
在82例符合条件的患者中,31例(38%)接受IM 400mg/d(作为初始治疗),25例(30%)接受NIL 600mg/d, 26例(32%)接受DAS 100mg/d。在NIL组中,7例一线接受NIL治疗,15例因IM不耐受更换为NIL, 3例转为NIL的原因不明;在DAS组中,12例作为一线治疗,9例因IM不耐受而更换,1例在IM治疗期间出现进展而更换,4例更换的原因不明。患者的基线特征见表1。3组患者在年龄、性别、Sokal风险评分、干扰素α治疗史、停用TKI时间等方面差异均无统计学意义。与NIL组相比,IM组在TKI停药前MR4.5持续时间更长(p<0.001),而IM组与DAS组(p=0.083)及NIL组与DAS组(p=0.08)之间均无显著差异。

在以IM为基线的交互模型中,采用AFT模型分析从TKI停药开始的复发动力学,该模型通过在多因素模型中添加混杂因素,可以关注治疗对复发动力学的具体影响。考虑到潜在的偏倚,以及TKI亚型和TKI停药前MR4.5持续时间的交互作用,将队列基线特征纳入模型。表2总结了多因素AFT模型的结果。
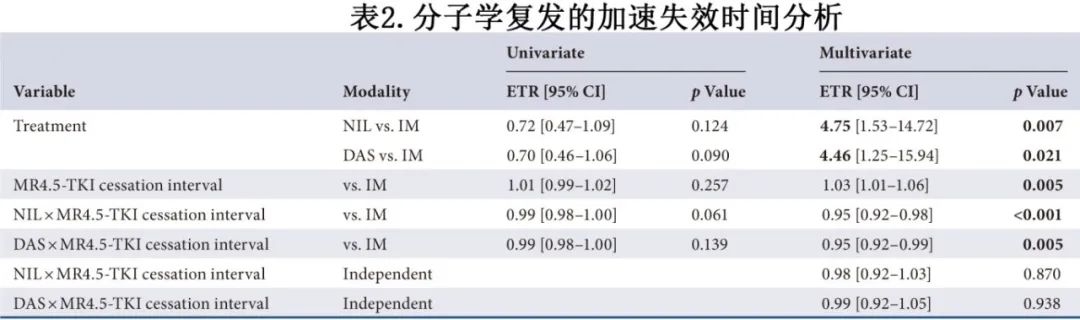
当考虑到MR4.5持续时间和TKI亚型时,与二代TKI相比,IM组的复发动力学显著更快,NIL和DAS的事件-时间比(event–time ratio,ETR)分别为4.75 (95% CI[1.53-14.72])和4.46 (95% CI[1.25-15.94])(分别为p=0.007和p=0.021,图1)。仅在IM组中,TKI停药前的MR4.5持续时间与较慢的复发相关,ETR为1.03 (95% CI [1.01-1.06], p=0.005)。

专家点评
丹麦Jesper Stentoft教授认为上述研究很重要,相对于伊马替尼,两种二代药物(尼洛替尼和达沙替尼)治疗后的白血病进展明显减缓,表明药物暴露对相关因子(这对白血病再生很重要)产生了不同的作用。这一结果很新颖,因为规模最大的停药试验(EURO-SKI)集中于伊马替尼,而许多其他停药研究也只涉及一种药物。
抑制 BCR-ABL 1 激酶活性就是抗肿瘤药物治疗中的“莫扎特”,TKI抑制剂彻底改变了 CML 的治疗,深刻改变了预后,并引入了分子学缓解、临时治愈和无治疗缓解等全新概念。新技术的及时出现,自动化实时定量PCR,为疾病监测和治疗决策的发展铺平了道路,新的分子遗传学时代的光芒照耀了白血病和肿瘤学。
然而,神童不一定遗传给后代(注:莫扎特子孙的成就远不如莫扎特本人)。尽管分子变化导致二代和三代TKI的出现,旨在解决由靶突变引起的特定耐药问题,但仍不确定新一代 BCR-ABL 1 激酶抑制剂增加的价值是否能达到应作为一线治疗的程度;而Alcazer 等人的研究具有讽刺和有趣的意义,证明三种药物停药期间存在临床有意义的差异。
在 CML 中,治疗目标并不稳定。肿瘤的传统终点生存期受到年龄匹配的非 CML 患者生存期的挑战。在短期随机研究中,聚焦于减瘤速度和获得预定标志物结果的代理终点更容易实现,但代理终点的合法性受到质疑,特别是随着数据的成熟,并没有揭示生存率的差异。而试验性更强的方法(如估计和靶向残留的白血病干细胞池)即使有希望,也没有标准化和广泛临床适用性的潜力。
关于 BCR-ABL 1 激酶抑制的最初假设在于,仅以非常有效的方式抑制疾病,而推迟激酶抑制不可避免地会重新开始疾病。然而,药物暴露3-6年和预定义的显著反应深度可诱导约50%的机会以获得持久的无治疗缓解,这一事实在临床方向上再次改变了最终目标。由于仅建议特定患者推迟(粗略地说,就是无耐药问题的患者和最佳反应者),因此现在的努力就是最大限度地提高 CML 患者的“可停止性”。因此,目前理想的 CML 研究是一个综合体,包括诱导治疗联合或不联合其他药物、数年维持治疗和足够长的无治疗期,以捕获大多数疾病进展。然而,研究持续时间需要7年,招募阶段约需要3年,再加上研究概念可能过时和结果不重要,都可能成为研究的障碍。
因此,有些重要问题可能长期甚至永远无法通过经典临床研究解答:现有TKI之间是否存在差异(除了在体外 BCR-ABL 1 突变抑制方面容易观察的明显差异,以及特定原发性耐药病例中的差异)?BCR-ABL 1 激酶诱导的反应是否等同(即使新一代药物反应更快)?在此背景下,Alcazer等人的研究极为重要,其结果与法国协作组第二次停药研究和北欧 CML 研究组的数据一致。法国协作组研究了额外两年的尼洛替尼,而北欧小组在中期报告了额外达沙替尼治疗至少3年后第二次停药尝试的结果【Leukemia】停药失败的CML接受达沙替尼再治疗,停药后的无治疗缓解率:DAstop2研究中期结果。在法国研究中,12个月和24个月后无治疗缓解的比例分别为68.2%和59.1%,而北欧研究报告6个月、12个月和24个月后无治疗缓解的比例分别为61%、56%和46%,16%的复发发生于12个月后。虽然因为患者数量较少,解释应谨慎,但二代TKI第二次停药后的复发动力学似乎比伊马替尼慢。
因此,似乎可以合理地假设,BCR-ABL 1 激酶抑制剂无法完全实现互换,通过对未知的生物学机制进行探索和利用,可以优化初始治疗,从而增加无治疗缓解率。但不幸的是,人们对这一点仍知之甚少。静止期干细胞池和骨髓微环境是重要靶点,免疫刺激可能是重要装备(正如 Alcazer 等人所证实)。但仍有新型疗法可能会出现。
特别值得注意的是,上述法国研究是一项回顾性、多中心分析。作者指出,数据来源于在 CML 国家研究组合作的6家中心,他们使用严格的疾病定义和分子评估的标准化抽样,实验室是国际标准化的。该文章非常清楚地证明,在相对较小的患者群体中,严格的临床协作和高质量的临床和实验室评估的价值。对于单个患者,其治疗结局得到了优化;对于患者组,与正式的前瞻性研究相比,可以以更少的费用产生显著的结果。因此,最佳治疗可能为当前和未来患者提供最佳结果。就像莫扎特一样,对他来说很容易,也很不言而喻;但你就需要排练很多。
参考文献
1. Alcazer V, Morriset S, Rea D, Legros L, Dulucq S, Hayette S, et al. Kinetics of molecular recurrence after tyrosine kinase inhibitor cessation in chronic phase chronic myelogenous leukaemia patients. Br J Haematol. 2024
2. Stentoft J. The Mozart effect in chronic myeloid leukaemia. Br J Haematol. 2024;00:1–2. https://doi.org/10.1111/bjh.19351