肺癌是目前全球最常见的恶性肿瘤之一,其发病率和死亡率常年位居前列。近年来,肺癌在我国持续位居发病率和死亡率之首。非小细胞肺癌(NSCLC)约占肺癌的 80%,在过去十余年的综合治疗发展历程中,精准医学理念在很大程度上改变了晚期NSCLC患者的治疗方案格局,针对驱动基因突变的小分子靶向药物在肺癌药物治疗中的重要性逐渐凸显。相对于传统化疗方案,靶向治疗显著提高了部分携带有敏感突变晚期NSCLC患者的客观缓解率(ORR),延长患者的无进展生存时间(PFS)和总生存时间(OS),改善了患者的生存质量。
针对基因检测在携带罕见突变肺癌患者中的价值,小编整理了几个问题:1.目前肺癌罕见靶点的诊疗现状如何?2.肺癌MET异常主要包括哪些,有哪些靶向药物可用?3.肺癌中BRAF V600E突变、BRAF非V600E突变的靶向治疗疗效如何?4.肺癌检出KRAS G12C,有哪些靶向药物可供选择?5.肺癌检出ROS1融合,有哪些靶向药物可供选择?
本期的【绘真有约·大咖答疑】非常荣幸邀请到了新乡市第一人民医院——赵乐教授,针对上述问题做了简要解答。
绘真:1.目前肺癌罕见靶点的诊疗现状如何?
赵乐教授:
临床上对于非小细胞肺癌(NSCLC)常见靶点,如EGFR和ALK等的研究日趋成熟,而对罕见靶点的探索也在不断深入。当下,研究多集中于MET、BRAF、HER-2、KRAS和ROS1等罕见靶点。在携带罕见靶点突变的NSCLC患者中,传统化疗模式已经难以契合临床需求。随着精准医疗时代的来临,针对这些罕见靶点的靶向药物相继问世并应用于临床,为患者带来了新的曙光,其预后得到了进一步改善。
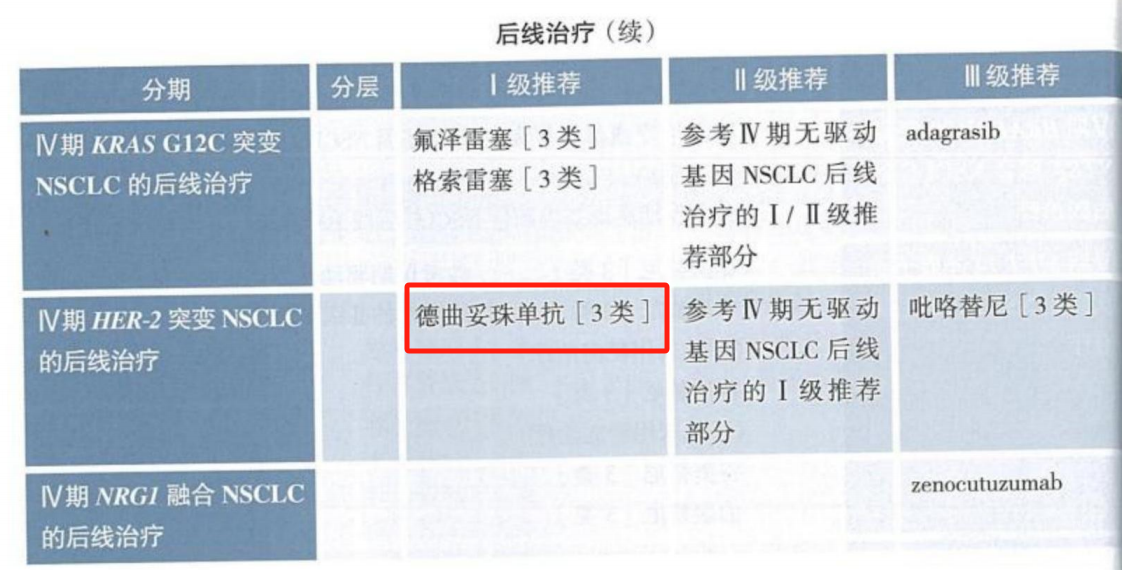
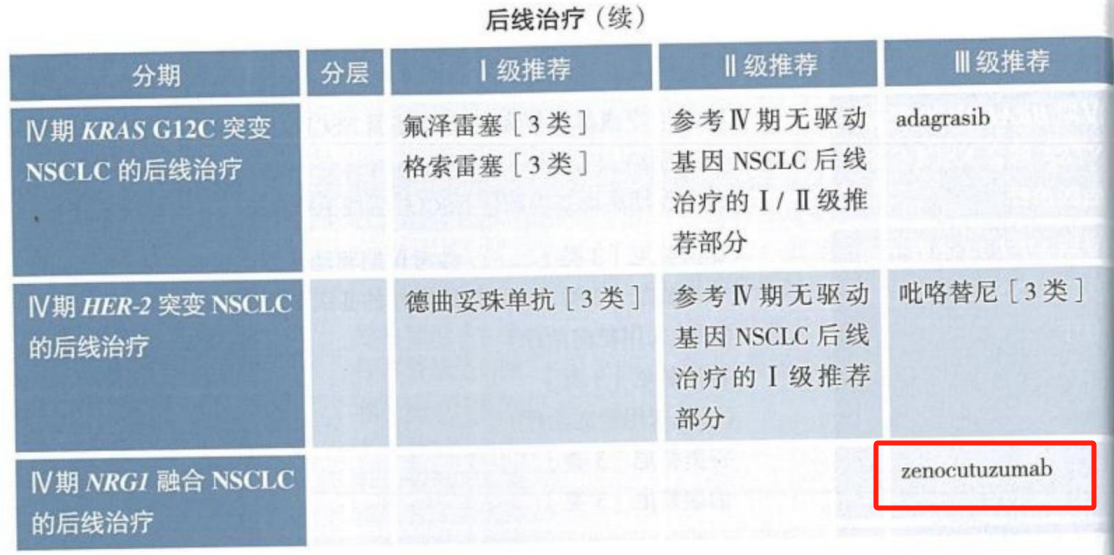
2025 CSCO非小细胞肺癌诊疗指南中,针对多种罕见靶点的诊疗策略均有更新。例如,在HER2突变方面,指南在后线治疗中上调德曲妥珠单抗作为I级推荐。在NRG1融合领域,新增泽妥珠单抗(zenocutuzumab)作为后线治疗的III级推荐。
不仅如此,检测技术的进步,如二代测序(NGS)的普及,让罕见靶点的精准检测成为可能,为靶向治疗提供了有力支撑。此外,医保政策也逐步向罕见靶点药物倾斜,例如拉罗替尼纳入医保后,极大减轻了患者经济负担。这些成果标志着肺癌罕见靶点诊疗正从探索走向成熟,为更多患者带来新的希望。
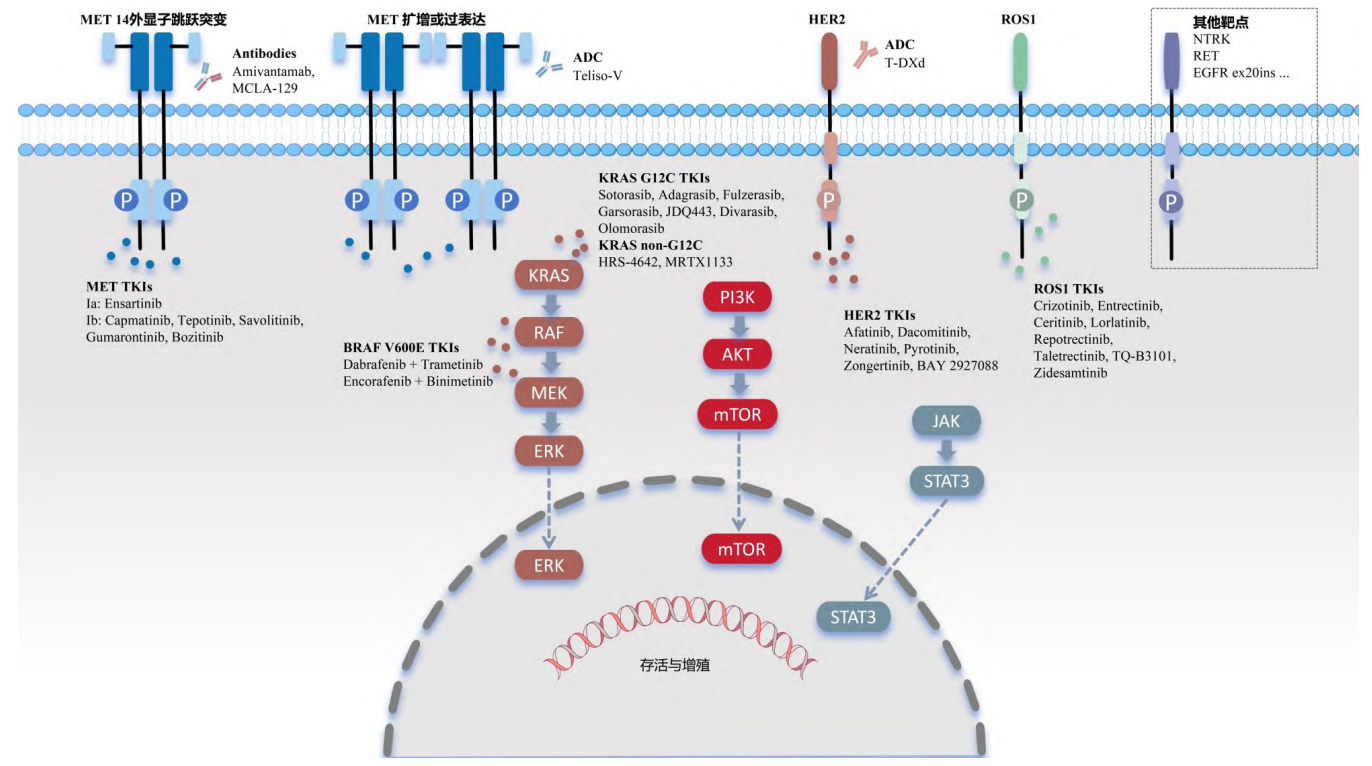


绘真:2.肺癌MET异常主要包括哪些,有哪些靶向药物可用?
赵乐教授:
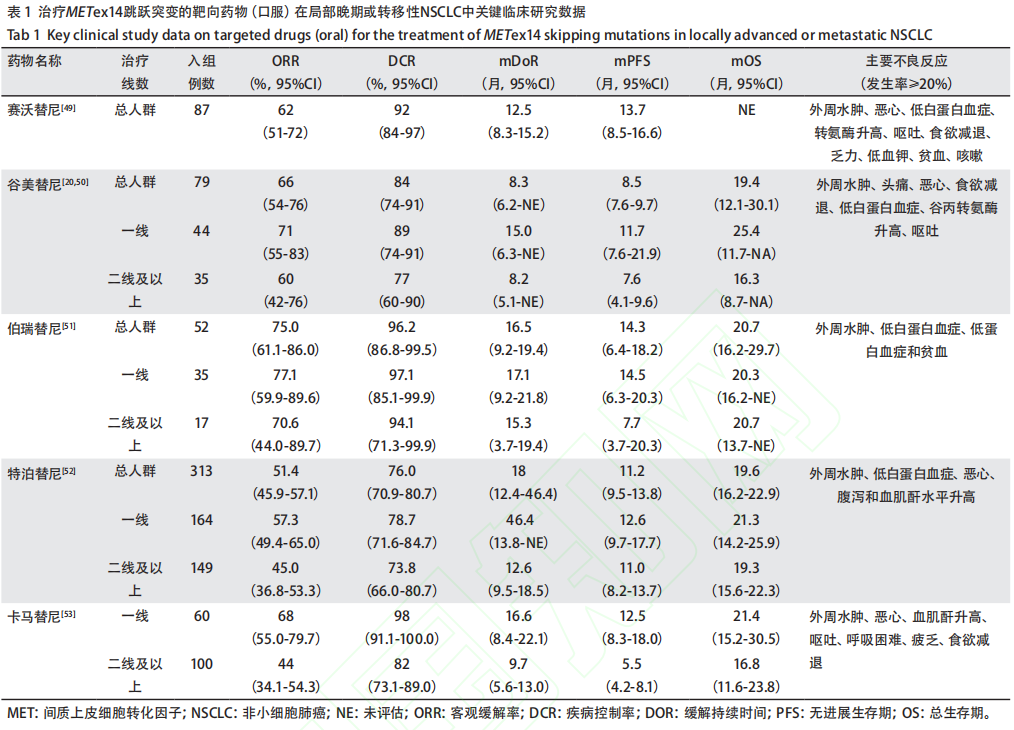
MET异常主要包括MET 14外显子(METex14)跳跃突变、MET基因扩增和MET蛋白过表达等。在中国NSCLC人群中,MET ex14跳跃突变的比例为 0.9%-2.0%。卡马替尼、特泊替尼、赛沃替尼、谷美替尼、伯瑞替尼先后获批用于MET ex14跳跃突变晚期NSCLC患者,其一线客观缓解率(ORR)为 57%-77%,中位无进展生存期(PFS)在 11.7-14.5 个月,二线及以上ORR达 44%-70%,中位PFS为 5.5-11 个月。2025 年CSCO指南将这 5 种药物均纳入一线及后线治疗的I级推荐。
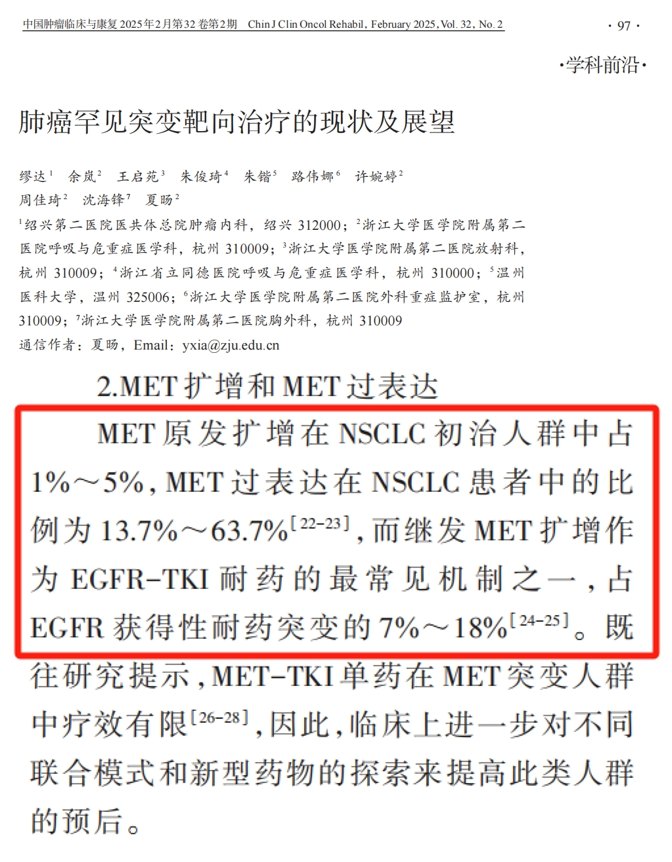
原发性MET扩增在NSCLC初治人群中发生率较低,为 1%-5%,而继发MET扩增作为EGFR-TKI耐药的最常见机制之一,占EGFR获得性耐药突变的 7%-18%。针对原发MET扩增,专家共识推荐,EGFR突变伴MET扩增的晚期NSCLC患者可使用奥希替尼联合赛沃替尼进行治疗;EGFR阴性、MET扩增患者可使用卡马替尼、特泊替尼、谷美替尼或克唑替尼单药进行治疗。另外,MET继发扩增的晚期NSCLC患者可使用EGFR-TKIs联合MET-TKIs进行治疗。
MET过表达在NSCLC患者中的比例是 13%-63%。专家共识指出,可尝试使用谷美替尼治疗驱动基因阴性MET蛋白过表达患者,或使用EGFR-TKIs联合MET-TKIs治疗EGFR耐药后MET蛋白过表达的NSCLC患者。





绘真:3.肺癌中BRAF V600E突变、BRAF非V600E突变的靶向治疗疗效如何?
赵乐教授:
NSCLC中BRAF突变率约为 1.5%-5.5%,其中以BRAF V600突变最为常见,占所有BRAF突变类型的 30%-50%。
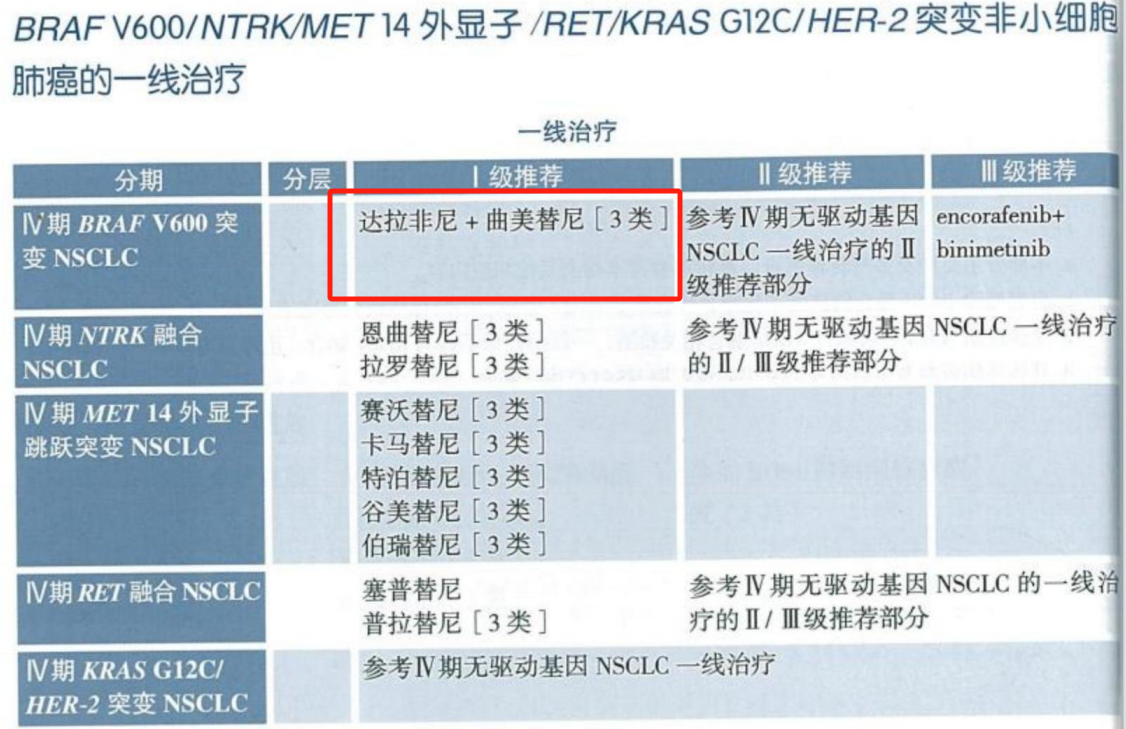
针对晚期BRAF V600E突变NSCLC患者,2025 CSCO非小细胞肺癌诊疗指南在一线治疗中I级推荐达拉非尼+曲美替尼。研究显示,达拉非尼+曲美替尼在中国人群中展现了更大优势,一线治疗ORR高达 75%,疾病控制率(DCR)达到95%。而且在BRAF V600E领域出现了新的治疗组合,有研究显示了康奈非尼(Encorafenib)联合比美替尼(Binimetinib)在BRAF V600E突变晚期NSCLC中的初步疗效,且初治患者疗效优于经治患者,ORR分别为 75% 和 46%,24周DCR分别为 64% 和 41%。指南也将康奈非尼联合比美替尼作为一线治疗的III级推荐。
对于BRAF非V600E突变的NSCLC,当前专家共识推荐的一线治疗方案是以免疫检查点抑制剂为基础的治疗策略,不过该类患者目前缺乏标准的靶向治疗策略。一项回顾性研究显示,携带激活型BRAF非V600E突变的患者可有效接受BRAF/MEK TKI或(化疗)免疫治疗,而携带非激活型突变的患者无法从靶向治疗中获益,但可从(化疗)免疫治疗中获益。鉴于此,对该类患者进行靶向治疗前,还需确定具体的突变亚型。








绘真:4.肺癌检出KRAS G12C,有哪些靶向药物可供选择?
赵乐教授:
中国NSCLC中KRAS突变发生率约为 10%,多见于吸烟患者中。根据突变类型,G12C突变最为常见,约为 39%,其次是G12V突变(约 18%-21%)和G12D突变(约 17%-18%)。
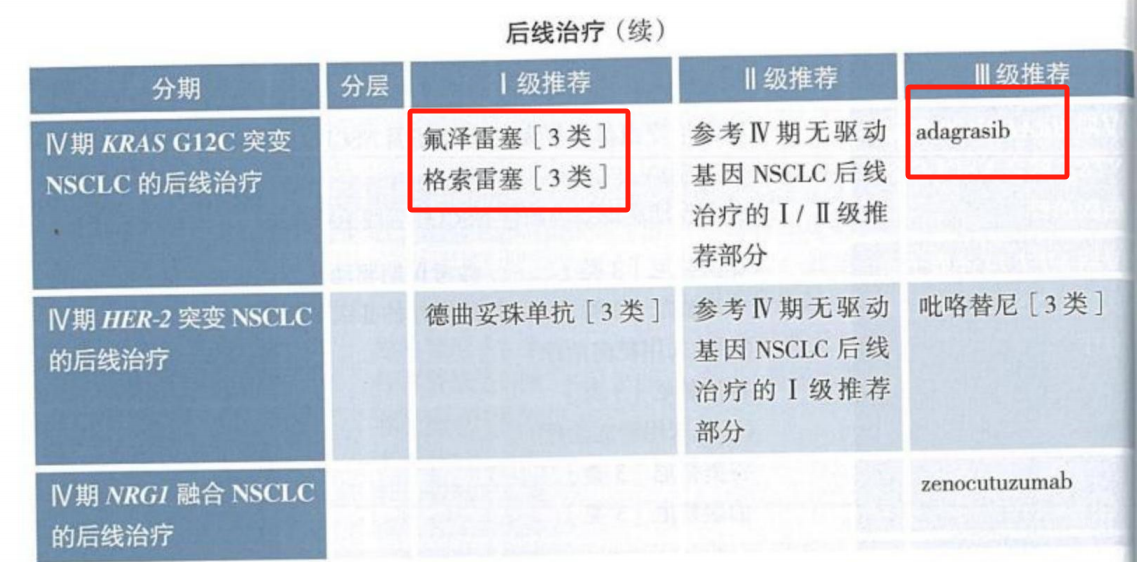
目前,靶向治疗在KRAS G12C突变NSCLC患者中取得重大突破,但限于二线及后线治疗,一线治疗仍无标准靶向治疗方案。2025 年CSCO指南在KRAS G12C突变晚期NSCLC患者的二线及后线治疗中,新增I级推荐氟泽雷塞和格索雷塞,并在III级推荐中删除索托雷塞(Sotorasib),仅推荐阿达格拉西布(Adagrasib)。
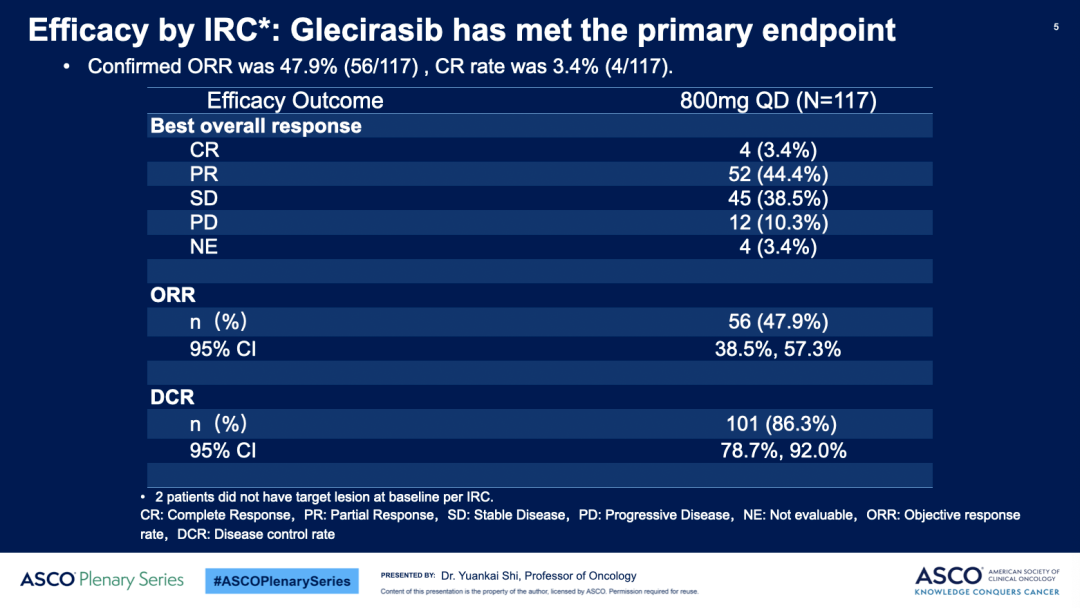
另外今年 5 月底,戈来雷塞获批上市,用于治疗至少经历过一种系统性治疗的KRAS G12C突变NSCLC。研究结果显示,确认ORR为 47.9%(56/117),其中包括 4 例患者实现完全缓解(CR),36 例患者肿瘤缩小超过 50%,DCR为 86.3%。
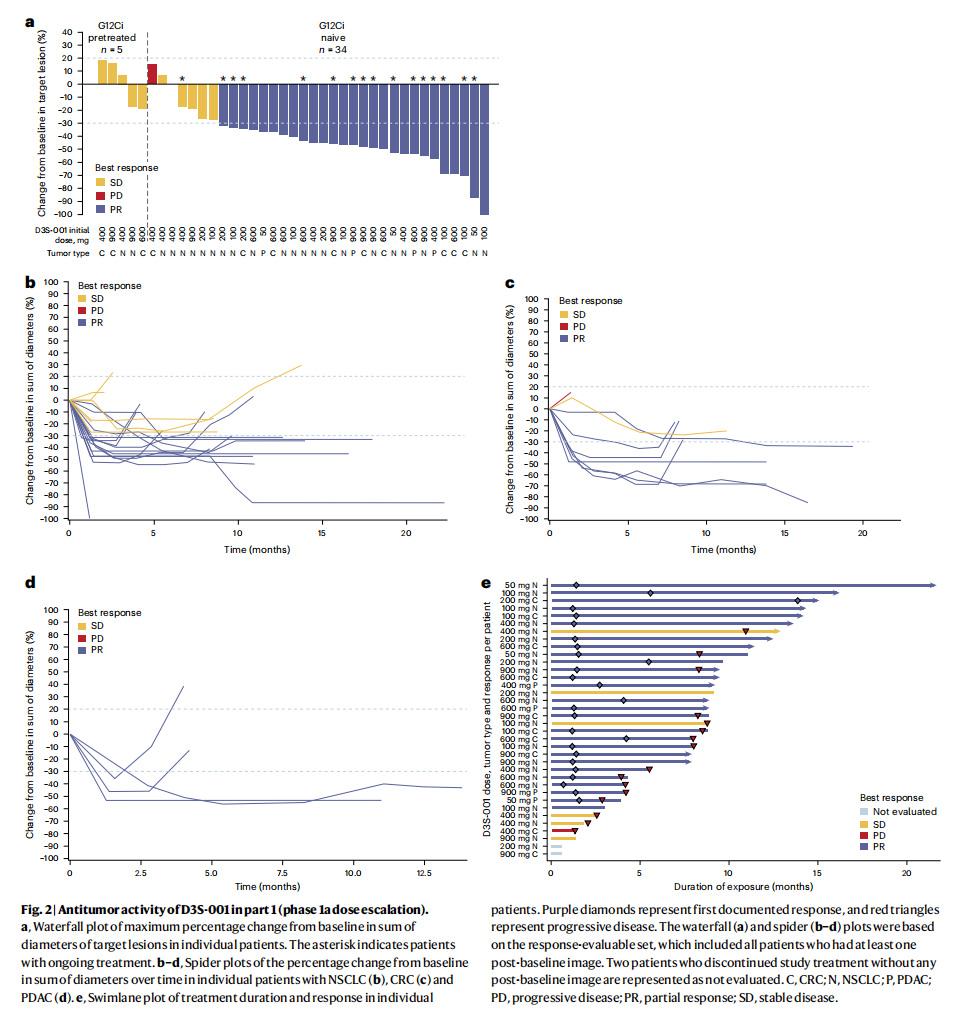
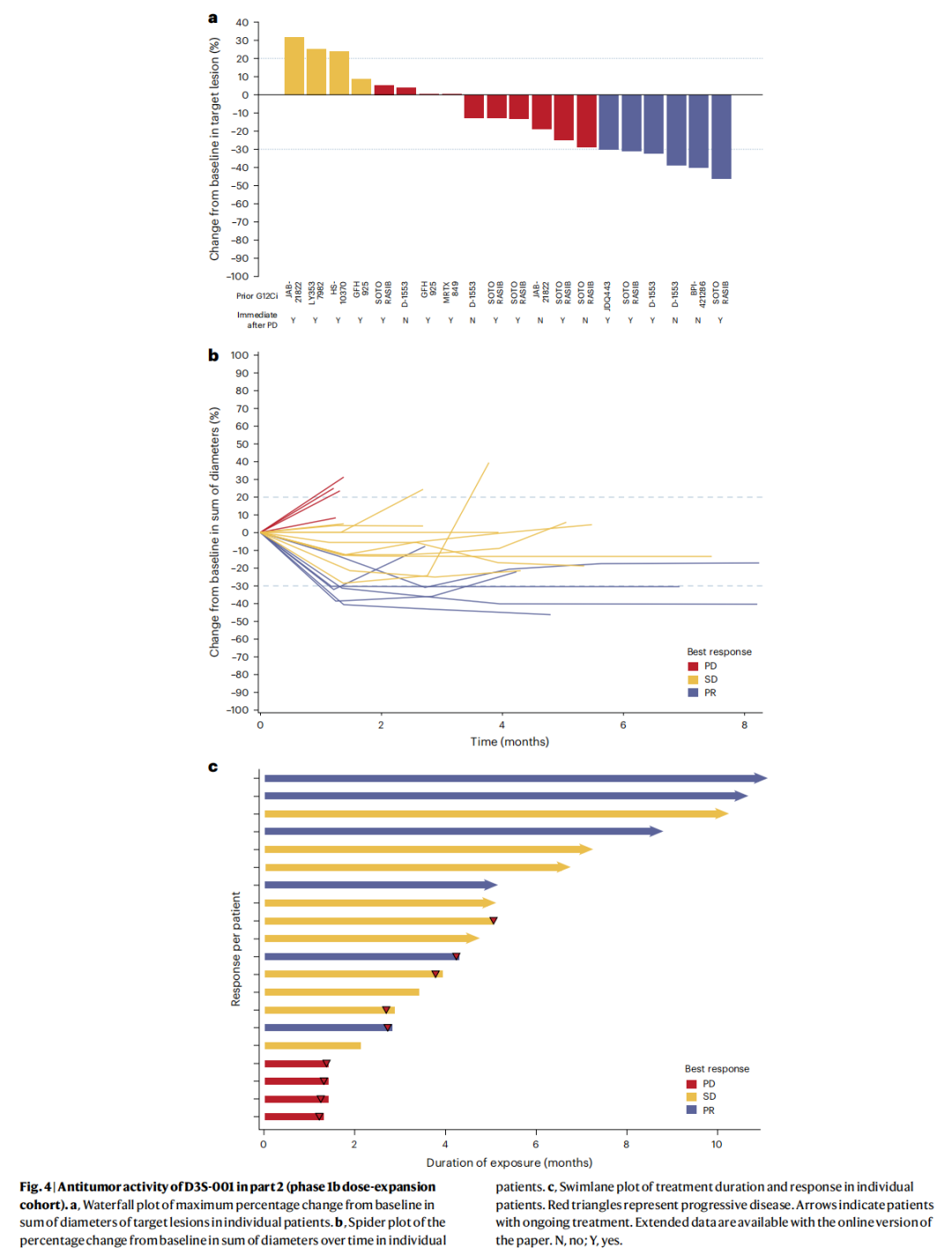
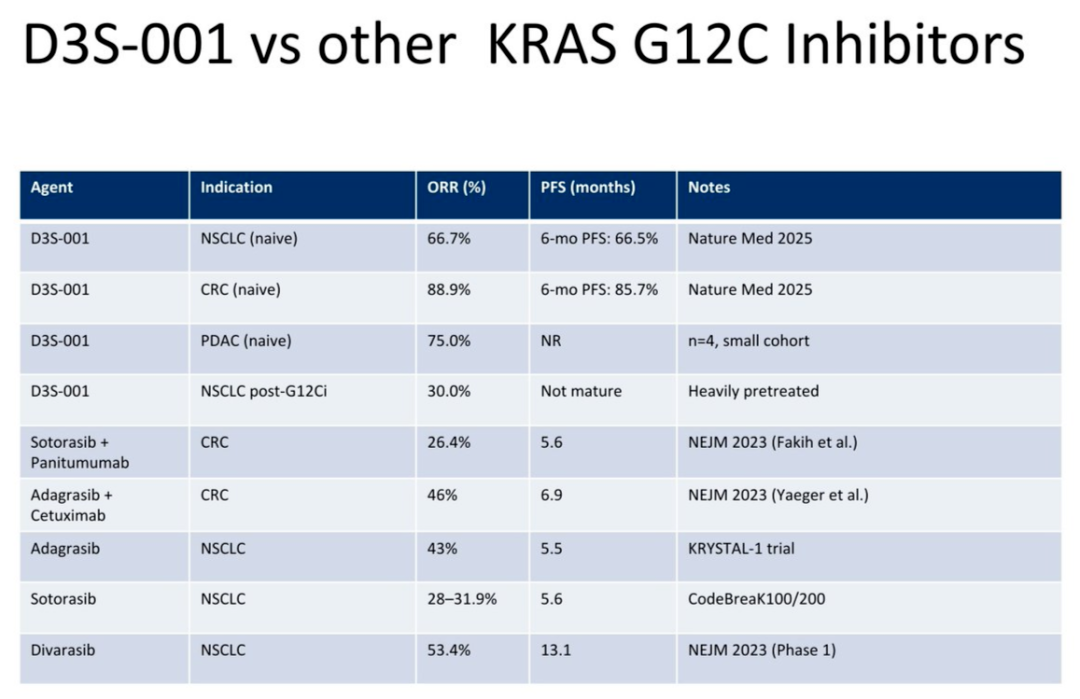
当然也有许多靶药正在临床试验中,并且有些靶药已显示出初步疗效。例如,一项发表在Nature Medicine期刊上的研究显示,在既往未接受过KRAS G12C抑制剂治疗的实体瘤患者中,D3S-001治疗后整体ORR为 73.5%,其中NSCLC患者的ORR为 66.7%;在既往接受过KRAS G12C抑制剂治疗的NSCLC患者中,ORR和DCR分别为 30% 和 80%,且大多数缓解仍在持续。该研究表示,相比于阿达格拉西布和索托雷塞,D3S-001有望改善KRAS G12C突变癌症患者的预后。


绘真:5.肺癌检出ROS1融合,有哪些靶向药物可供选择?
赵乐教授:
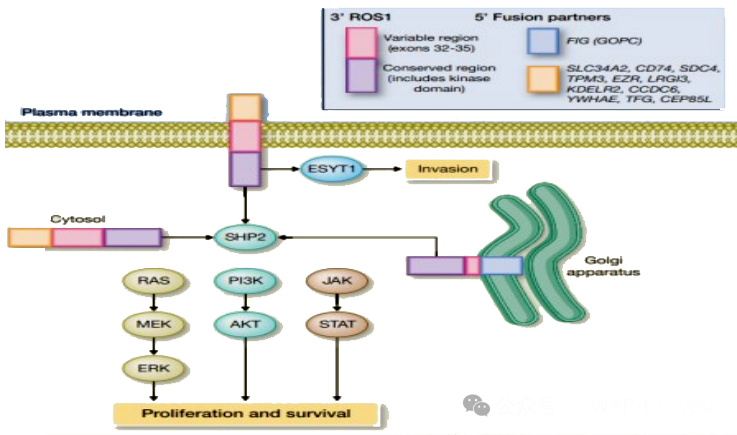
ROS1基因位于人类第 6 号染色体的长臂上,是一个蛋白基因编码,具有酪氨酸激酶活性,可作为一个生长或分化因子的受体,参与细胞分化、增殖、生长和存活的信号通路激活,包括MAPK-ERK等(PI3K-AKT-mTOR、AK-STAT和SHP1/2)。ROS1融合阳性发生于 1.0%-3.4% 的NSCLC患者中,在肺腺癌、非吸烟、女性患者中多见。
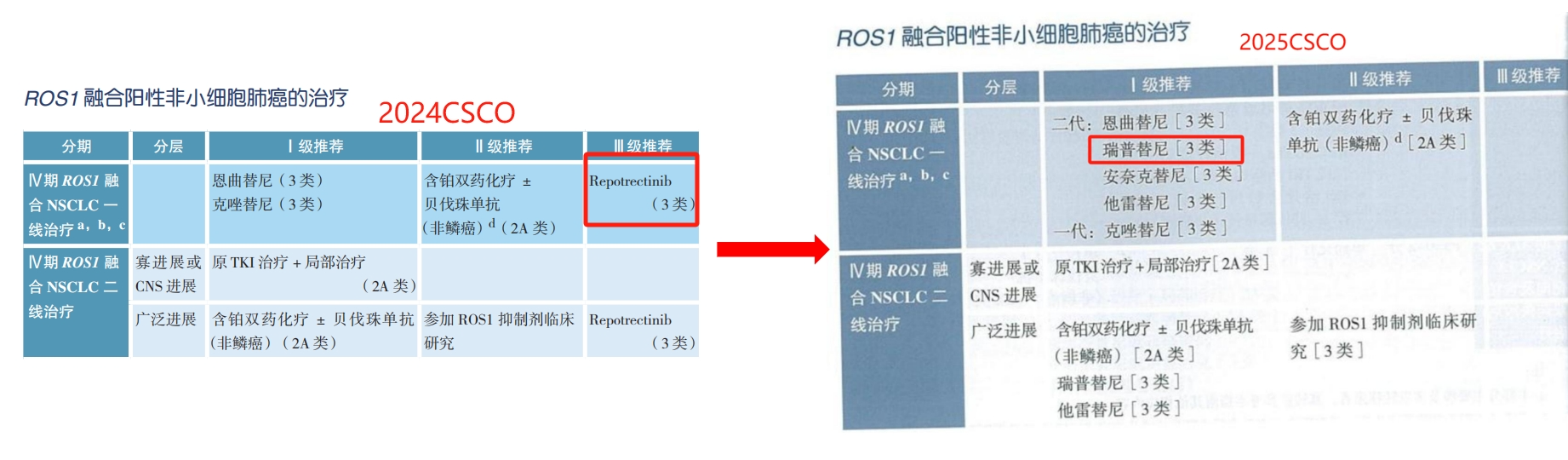
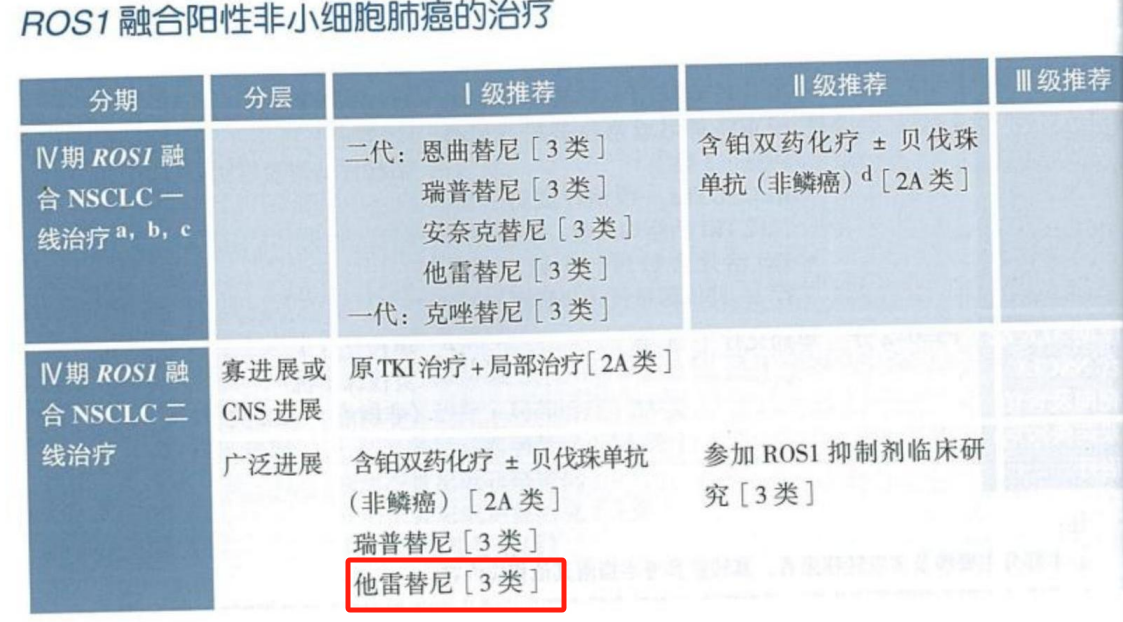
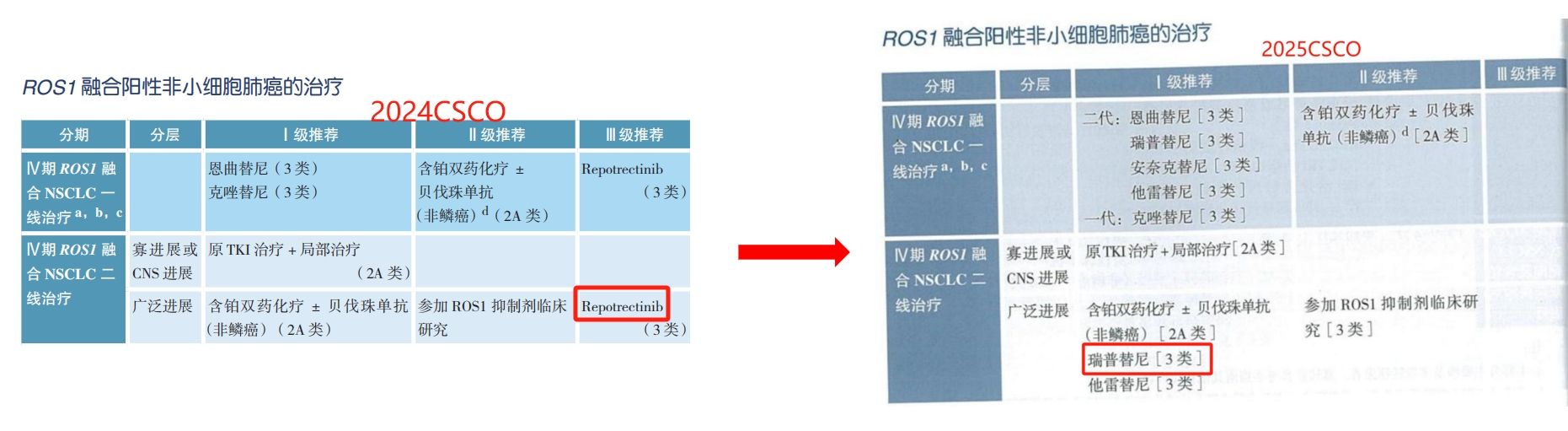
针对ROS1融合阳性晚期NSCLC,2025 CSCO指南在用药推荐上进行了多项调整。首先在一线治疗中,I级推荐除了包含之前的恩曲替尼和克唑替尼,还新增了他雷替尼和安奈克替尼,并将瑞普替尼从III级推荐上调至I级推荐。在二线治疗中,对于寡进展或中枢神经系统进展患者,原TKI+局部治疗;对于广泛进展患者,I级推荐新增靶向治疗他雷替尼,也将瑞普替尼从III级推荐上调至I级推荐。
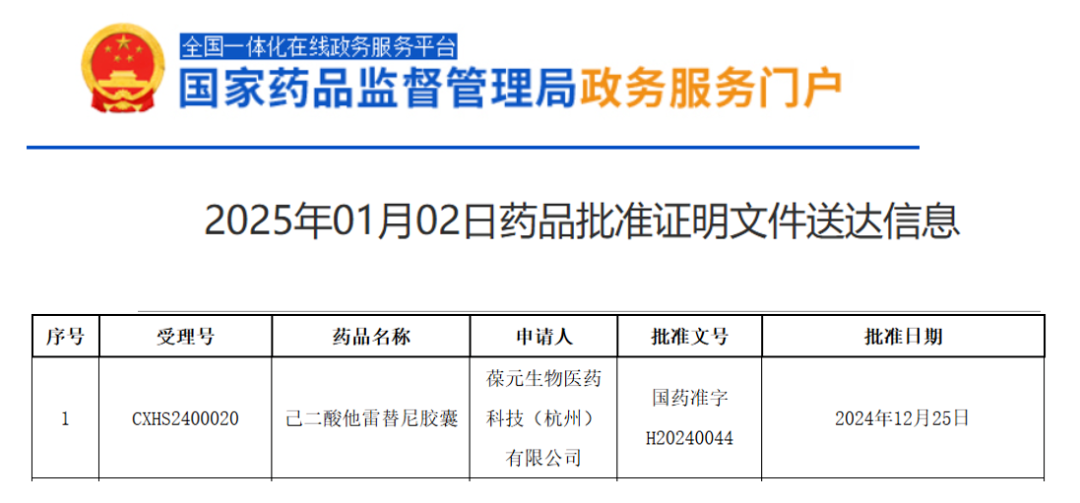
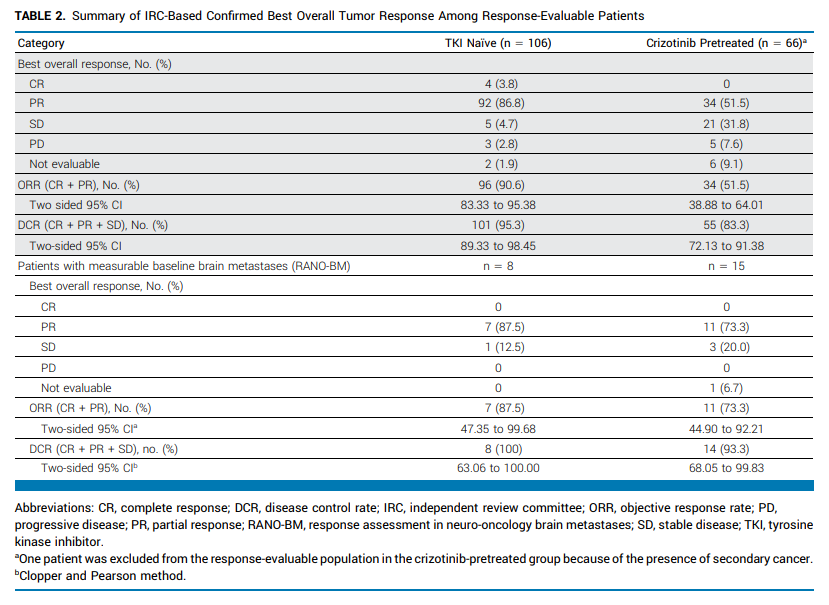
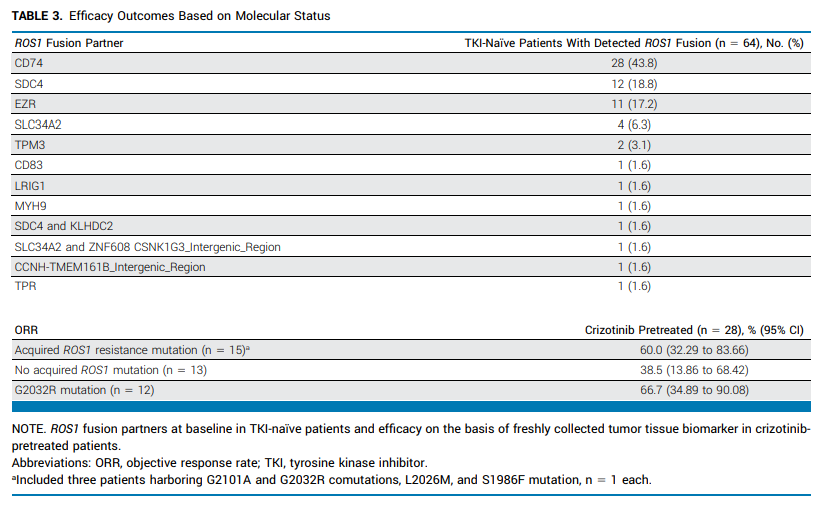
最近广受关注的他雷替尼,于 6 月 11 日获美国FDA批准上市。其实在去年年底,国内NMPA就已经批准他雷替尼,用于经ROS1 TKI治疗后进展的ROS1阳性局部晚期或转移性NSCLC成人患者。随后不到半个月,NMPA又批准他雷替尼用于该类患者的一线治疗。研究显示,无论是初治还是经治患者,他雷替尼的疗效显著并且持久,并且对颅内病灶及获得性耐药突变(如G2032R)显示出强劲活性,且安全性特征良好,神经系统不良事件发生率较低。