研究亮点
- 系统梳理了哮喘发病机制中氧化应激与炎症的关键通路,揭示多靶点天然活性成分的调控潜力。
- 汇总了多种天然植物源化合物及中药复方在调节哮喘相关分子通路中的作用机制与实验证据。
- 结合纳米递送技术进展,探讨提升天然成分生物利用度与疗效的新策略,为哮喘的个性化及长期管理提供创新思路。
哮喘是一种复杂、异质性的慢性过敏性呼吸系统疾病,具有发病机理多样、临床表现差异显著的特点。近年来,氧化应激与炎症反应被广泛证实为哮喘发生发展中的关键驱动因素。哮喘发病机制涉及遗传、环境及职业等多种内外因,使得临床表现及病理过程表现出高度异质性。传统药物以缓解症状及抗炎为主,但长期大剂量使用会导致副作用及耐药问题。最新研究表明,氧化应激通过失衡的活性氧(ROS)产生及抗氧化防御系统受损,促进炎症细胞活化和气道重塑。炎症方面,免疫细胞及多种炎症介质在介导过敏反应和气道高反应性中起核心作用。当前对这些分子通路的深入认识为筛选天然活性成分提供了理论基础,也促使人们探索多靶点、多机制的综合调控方案。
近期,发表在Chinese Medicine杂志的一项综述,探讨了哮喘相关的氧化应激和炎症信号通路,还回顾了靶向通路的传统中药复方及其组合治疗优势。

研究结果
1,哮喘的病理生理机制
哮喘典型特征包括可逆性气道受限、气道高反应性、慢性气道炎症及黏液过度分泌(见图1)。氧化应激通过激活Nrf2、NFκB、线粒体及MAPK信号通路等,驱动炎症反应及气道重塑。免疫反应主要依赖JAK-STAT、NFκB、炎症复合体(NLRP3)、TLRs/NLRs及GPCR等通路,促进Th2型炎症及气道损伤。
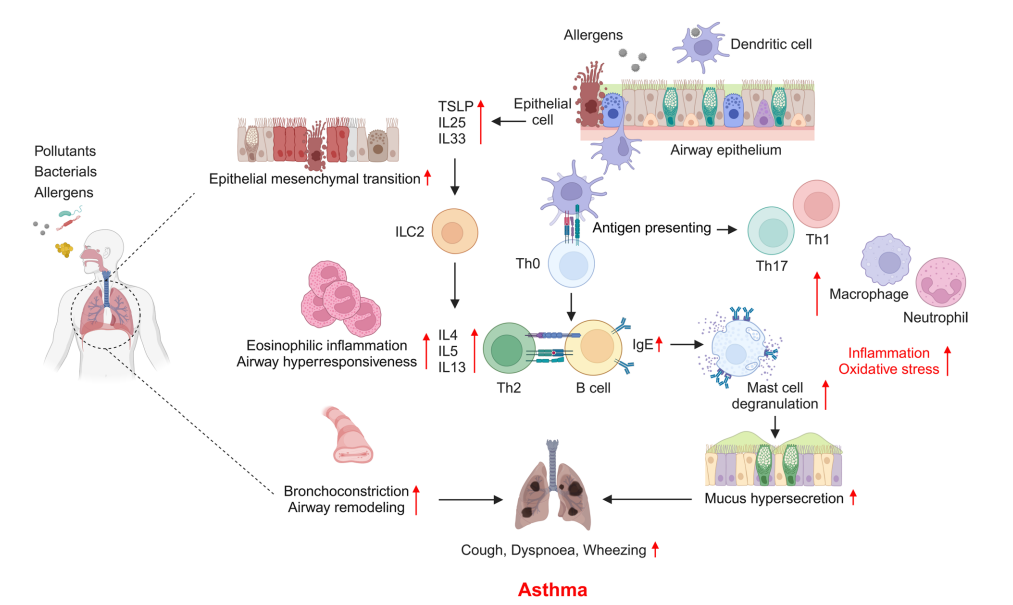
图 哮喘发病机制示意图
2,氧化应激相关核心信号通路
Nrf2通路:在氧化应激下激活,诱导抗氧化酶(HO-1、谷胱甘肽过氧化物酶)表达,缓解气道氧化损伤。多种天然物(如丹参酮、槲皮素和白藜芦醇)能激活该通路。
NFκB通路:氧化应激促进IκBα降解,NFκB核内转位,诱导多种炎性因子表达,参与气道慢性炎症。
线粒体通路:线粒体功能障碍导致ROS过度产生,激活NLRP3炎症复合体,促进局部炎症和气道损伤。
MAPK通路:包括ERK、JNK及p38,参与氧化应激诱导的信号转导,调控炎症因子表达。
硫氧还蛋白1(Trx1)及醛糖还原酶(AR):Trx1通过清除ROS及抑制MIF减缓氧化损伤及炎症;AR调控NFκB依赖的炎症反应,是潜在治疗靶点。
3,炎症相关核心信号通路
JAK-STAT通路:IL4、IL5、IL13等细胞因子介导的细胞信号,调控Th2免疫反应,促进炎症。
NFκB通路:维持炎症微环境,介导平滑肌表型转化,增加气道重塑。
炎症复合体(NLRP3):介导IL1β、IL18成熟,相关严重类固醇耐药性哮喘及炎症加重。
TLRs和NLRs:通过识别微生物及过敏原,调控下游PI3K/Akt、JNK、TRIF途径,协调炎症。
MAPK和GPCR:参与细胞应激及炎症反应调节,GPCR家族成员如GPER、DP2、GPR120等是新兴药物靶点。
4,天然来源生物活性化合物
多种天然化合物显示其调控哮喘相关氧化应激与炎症通路的潜力:
维生素E(d-α-生育酚乙酸酯):抗氧化,抑制5-脂氧合酶途径,降低炎症反应。
螺旋藻成分(藻蓝胆红素):模拟胆红素抑制NADPH氧化酶,减少气道氧化负荷。
2,3,5,4′-四羟基苯乙烯葡萄糖苷(TSG):调节Th1/Th2平衡,抑制TGFβ信号,减轻气道炎症和重塑。
槲皮素:通过SIRT1/Nrf2/HO-1途径抑制铁死亡,调控免疫平衡,减轻气道纤维化。
白藜芦醇:调控肠肺轴,抑制HMGB1/TLR4/NFκB通路,改善肺功能。
姜黄素及其衍生物:多靶点抑制NFκB、STAT6、GATA3等通路,改善气道高反应。
黄芩苷(Baicalin):靶向TLR4/NFκB及MAPK,抑制平滑肌增生和黏液分泌。
此外,黄酮类异黄酮染料素(Formononetin)、大蒜成分(Allicin)、北沙参提取物(Salidroside)、柑橘类黄酮(Naringenin)、草本倍半萜醇(Farnesol)等也均展示良好的抗炎抗氧化活性。
5,天然活性成分治疗靶点汇总
涵盖氧化应激通路,如Nrf2激活剂、线粒体抗氧化剂(MitoQ)、Trx1、AR抑制剂;炎症通路,包括JAK-STAT抑制剂、NFκB调控剂、NLRP3阻断剂、TLRs拮抗剂、MAPK抑制剂及多类型GPCR调控剂。多重靶点治疗显示出改善中重度或类固醇不敏感性哮喘的潜能。
6,纳米递送系统应用
为解决天然活性化合物生物利用度低等瓶颈,纳米载体技术成为提升肺部药物递送效率的关键手段。例如,包裹多酚的PLGA纳米粒、β-葡聚糖纳米颗粒及高载药纳米胶囊等均在临床前模型中显著改善了靶向输送及生物活性,推动哮喘治疗进入精准医学时代。
7,传统中医复方的综合调控优势
平喘方:通过抑制PI3K/Akt/NFκB途径,调节氧化与炎症反应,兼顾肠道菌群改善,实现系统性抗炎平衡。
泽泻汤:主打消炎抗氧化,降低基质金属蛋白酶表达,有效抑制气道平滑肌细胞增殖。
淫羊藿叶与女贞子联合提取物:协同抑制TGFβ/Smads信号,减少纤维化及黏液生成,缓解气道重塑。
布地奈德与上述提取物复合制剂:增强药效,促进炎症细胞凋亡,改善自噬异常,提升疗效稳定性。
抗哮喘草药干预(ASHMI):通过协同抑制Th2细胞因子及趋化因子,临床上与激素类药物相当且副作用低,已获FDA临床试验认可。
研究价值与意义
本文综述深刻揭示了哮喘发病过程中氧化应激与炎症的相互作用网络,强调多靶点、多机制调控策略的重要性。天然来源的生物活性化合物及其组方不仅提供有效缓解哮喘症状的新途径,更因其安全性和多靶点协同效应,成为克服传统药物局限性的有力选择。纳米技术的引入大幅提升了天然药物的靶向递送效率和稳定性,推动其向临床转化。传统中医结合现代药理学理念,利用复方药物的综合调控优势,彰显了中西医结合治疗哮喘的新模式。未来,跨学科整合基础研究、药物递送技术与临床试验,将加速天然药物开发与精准治疗策略的落地,为哮喘患者带来更安全、高效的治疗选项。
原始出处
Lee J, Choi H-K, Shin HS, Kim G-D. Naturally derived bioactive compounds as regulators of oxidative stress and inflammation in asthma. Chinese Medicine. 2025;20:94. https://doi.org/10.1186/s13020-025-01142-w