CAR-T细胞疗法通过基因工程改造患者自身的T细胞,使其表达嵌合抗原受体(CAR),从而能够特异性识别并攻击癌细胞。这种疗法在治疗复发/难治性B细胞恶性肿瘤和多发性骨髓瘤方面取得了显著成功,已有多种CAR-T产品获得FDA和EMA的批准。然而,急性髓系白血病(AML)作为一种具有高度异质性和复杂克隆进化特征的疾病,其治疗面临诸多挑战。AML患者的中位诊断年龄为68岁,通常表现为高侵袭性和高复发率,且复发/难治性AML是治疗失败的主要原因。尽管近年来在AML治疗中取得了一些进展,但目前尚无CAR-T产品获得AML的监管批准,全球正在进行的临床试验正在探索CAR-T细胞疗法在AML中的应用,但面临缺乏理想靶点、免疫抑制性微环境等挑战。
西班牙Josep Carreras白血病研究所Pablo Menéndez和Inés Zugasti等人全面回顾CAR-T细胞疗法在癌症治疗中的发展历程,总结其在血液系统恶性肿瘤和实体瘤中的应用现状,并深入探讨CAR-T细胞疗法在AML中的具体挑战、正在进行的全球临床试验以及未来发展方向,为未来CAR-T细胞疗法在AML中的优化提供方向和策略。相关内容以“CAR-T cell therapy for cancer: current challenges and future directions”为题发表在《Signal Transduction and Targeted Therapy》上。

【全文总结】
1. CAR-T细胞疗法的发展历程
文中展示了CAR-T细胞的结构,包括单链可变片段(scFv)、铰链区、跨膜区和内源信号区。CAR-T细胞疗法的发展经历了多个阶段,从最初的单信号CAR(第一代)到目前的多信号CAR(如第二代、第三代),以及更先进的第四代和第五代CAR-T细胞。这些改进旨在提高CAR-T细胞的活性、持久性和安全性。例如,第五代CAR-T细胞通过整合额外的膜受体(如IL-2受体信号)来激活JAK/STAT通路,不仅增强CAR-T细胞的活性和记忆T细胞的形成,还能重新激活并刺激更广泛的免疫系统。
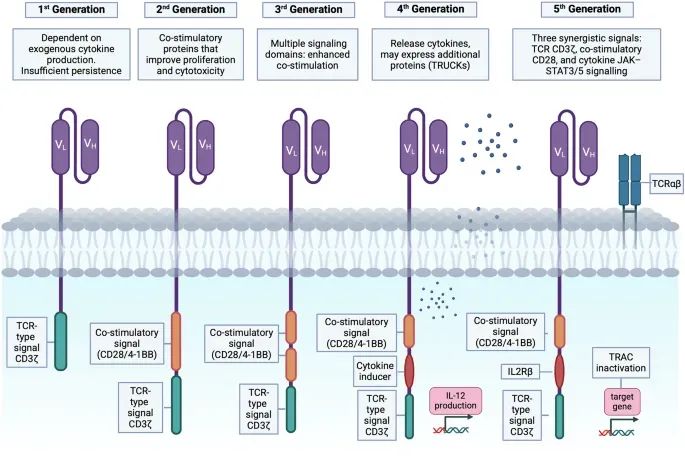
图1 CAR的结构
2. CAR-T细胞疗法在血液系统恶性肿瘤中的应用
文中详细列出了目前FDA和EMA批准的CAR-T细胞疗法,包括针对CD19和BCMA的CAR-T产品。这些产品在治疗复发/难治性B细胞恶性肿瘤和多发性骨髓瘤方面取得了显著成功。例如,Kymriah®和Yescarta®是首批获得批准的CAR-T细胞疗法,分别用于治疗儿童和年轻成人的B细胞急性淋巴细胞白血病(B-ALL)和成人复发/难治性大B细胞淋巴瘤(DLBCL)。
3. CAR-T细胞疗法在AML中的挑战
缺乏理想靶点:AML细胞与正常造血干细胞和祖细胞(HSPCs)共享大多数表面抗原,缺乏既能有效识别AML细胞又安全的靶点。同时靶向AML细胞和HSPCs可能导致危及生命的靶向/非肿瘤毒性,如长期骨髓抑制。
免疫抑制性微环境:AML的肿瘤微环境具有免疫抑制性,影响免疫反应的效果,进一步限制了CAR-T细胞疗法的疗效。
AML的异质性:AML具有高度的克隆异质性,不同的分子和细胞遗传学异常导致疾病表现、进展和治疗反应的差异。这种异质性使得CAR-T细胞疗法的开发更加复杂。
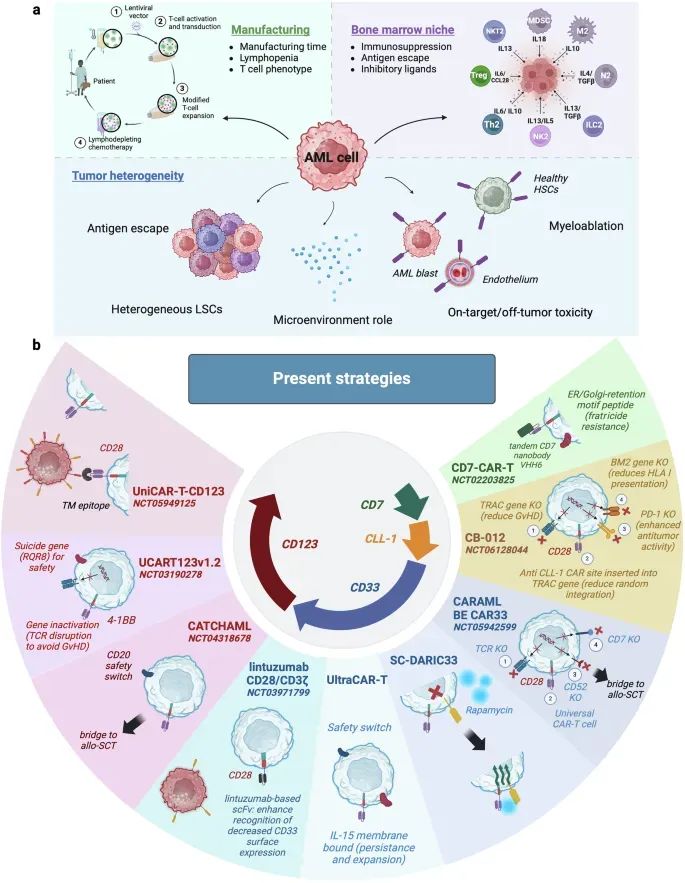
图2 AML的CAR - T制备面临的挑战
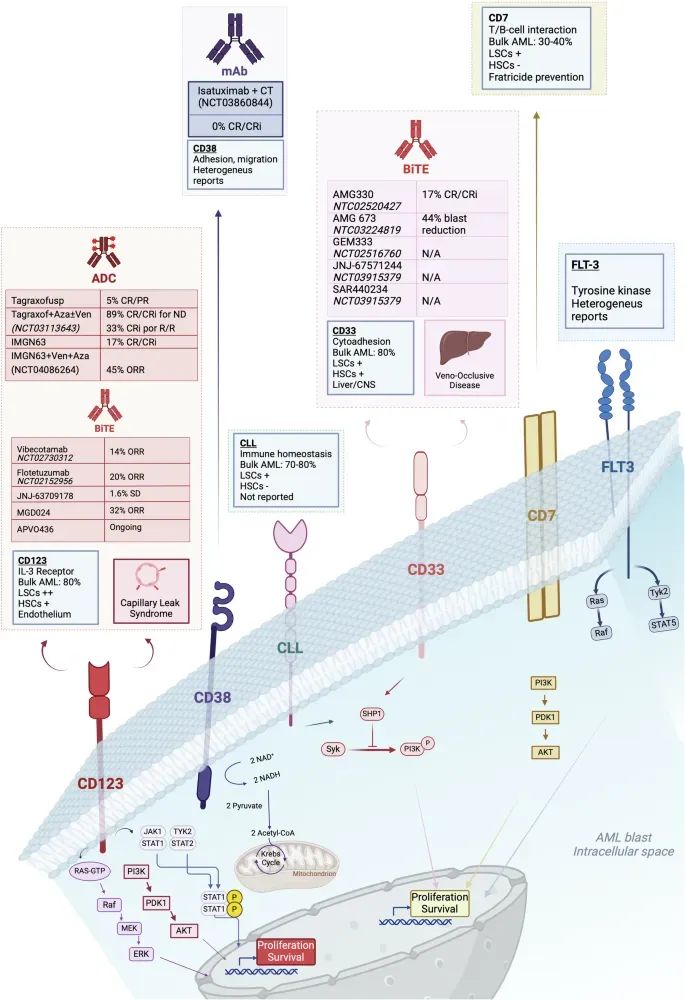
图3 当前AML定向疗法所针对的最常见抗原的主要特征及相关临床试验
4. CAR-T细胞疗法在AML中的研究进展
当前正在进行的CAR-T细胞疗法临床试验,主要集中在CD123和CD33这两个靶点。
CD123-CAR-T细胞:CD123是AML细胞上高度表达的抗原,但其在正常造血干细胞上也有低水平表达,可能导致骨髓抑制。目前正在进行的临床试验包括使用UniCAR-T-CD123(NCT04230265)和Allo-RevCAR01-TCD123(NCT05949125)等策略,这些策略通过基因编辑技术提高CAR-T细胞的安全性和有效性。
CD33-CAR-T细胞:CD33是另一个在AML细胞上广泛表达的抗原。目前正在进行的临床试验包括使用lintuzumab-CD28/CD3ζ(NCT03971799)和PRGN-3006(NCT03927261)等策略,这些策略通过优化CAR结构和生产工艺提高CAR-T细胞的疗效和安全性。
5. 未来发展方向
多靶点策略:通过靶向多个抗原来提高CAR-T细胞疗法的特异性和有效性。例如,文中提到了双特异性CAR(如CD123/CD33 cCAR)和逻辑门控CAR(如AND、OR、NOT逻辑门)等策略,这些策略可以通过复杂的抗原表达模式来识别AML细胞,减少非肿瘤毒性。
基因编辑技术:利用CRISPR/Cas9等基因编辑技术对CAR-T细胞进行改造,提高其安全性和有效性。例如,文中提到了通过基因编辑技术敲除CAR-T细胞中的PD-1等抑制性受体,以增强其抗肿瘤活性。
联合治疗策略:将CAR-T细胞疗法与其他治疗方法(如免疫检查点抑制剂、代谢调节剂、表观遗传药物等)联合使用,以克服AML的免疫抑制性微环境,增强CAR-T细胞的疗效。
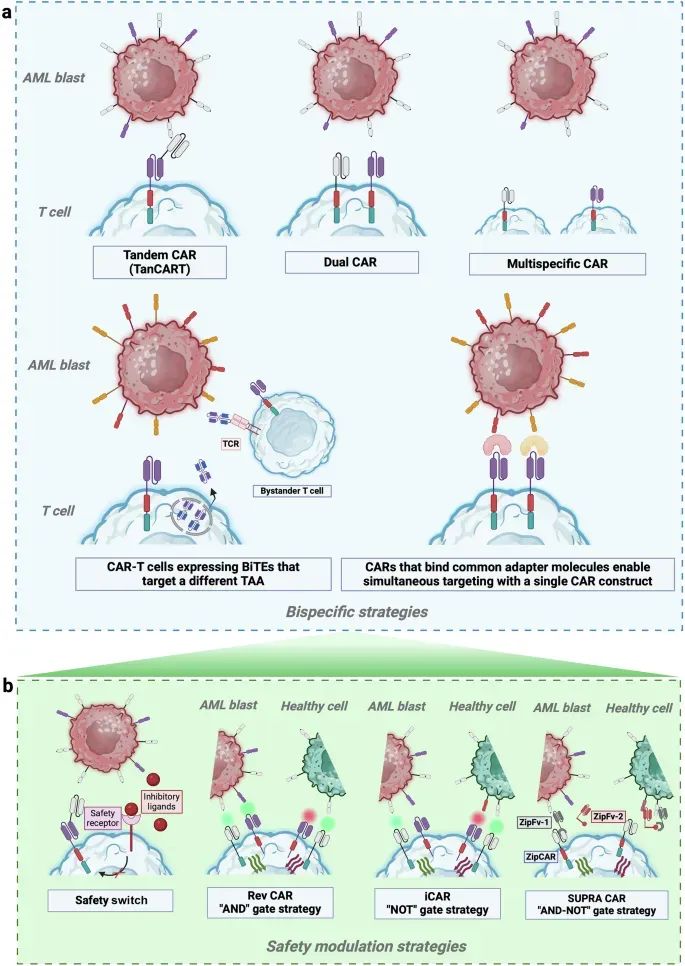
图4 双特异性策略
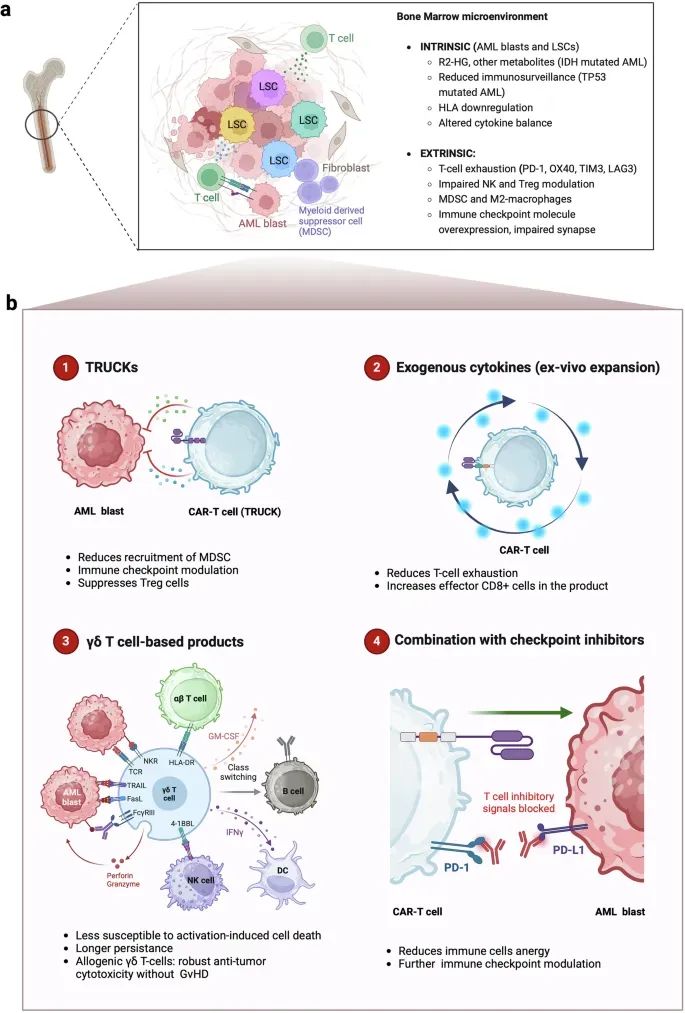
图5 具有内在和外在特征的急性髓系白血病骨髓微环境
【全文总结】
本文总结了CAR-T细胞疗法在癌症治疗中的研究进展,特别是在AML中的挑战和未来发展方向。尽管CAR-T细胞疗法在B细胞恶性肿瘤和多发性骨髓瘤中取得了显著成功,但在AML中的应用仍面临诸多挑战。通过优化CAR结构、开发多靶点策略、利用基因编辑技术和联合治疗策略,未来有望克服这些挑战,提高CAR-T细胞疗法在AML中的疗效和安全性。
原文链接:
https://doi.org/10.1038/s41392-025-02269-w