【题记】当科学遇见自然,当兽药跨越物种鸿沟,在纪念斯隆凯特琳的实验室里,研究人员竟将一种原本用于治疗犬类癌症的植物提取物,改造成能「爆破」人类肿瘤的全新武器。这个故事里没有科幻大片的穿越,有的却是严谨的机制探索;没有过度炒作的反转,有的却是持续十年的验证与突破。
一、癌症治疗的「爆破式革命」:肿瘤消失后6个月全无复发
2024年秋日的纽约,纪念斯隆凯特琳癌症中心的研究团队正在整理那份让他们心跳加速的报告。在QB46C-H07这项针对软组织肉瘤的2a期临床试验中,10名患者接受了创新疗法的治疗——将抗癌药Tigilanol tiglate直接注射至27枚肿瘤中。更令人震撼的是,在6个月随访期内,所有确认完全消失的肿瘤没有出现任何复发迹象。
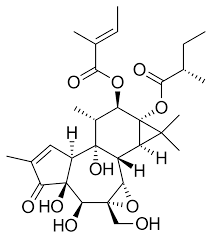
Tigilanol tiglate是一种以巴豆素-3-酮为骨架的巴豆素衍生物。Tigilanol tiglate 是从澳大利亚昆士兰州的红木浆果中提取的,因此可能含有其他巴豆素-3-酮衍生物的杂质。2020 年 1 月,欧盟批准 Tigilanol tiglate 用于犬类治疗。该药适用于治疗位于犬肘部或跗关节或远端的不可切除、非转移性(WHO 分期)皮下肥大细胞肿瘤,以及不可切除、非转移性皮肤肥大细胞肿瘤。专家告诉我们,这并非传统意义的缩小:实验室观察到的是真正的「溶解级」反应。52%的肿瘤在治疗6周后完全溶解,超过90%的残留肿瘤组织出现显著退缩。这种效果不仅体现在实体肿瘤的体积变化上,更在生物机制层面展现出颠覆性可能。当我们把这些肿瘤想象成必须清除的「矿脉」,Tigilanol tiglate就像精准投放的特制TNT——爆破血管同时激发免疫系统,让肿瘤从内部崩塌。
*注:获得肿瘤完全病理反应的数据通常需要至少3个月,而该试验纳入的随访数据已是6个月.
二、从犬类肿瘤到人类新希望:跨物种的抗癌基因奥秘
这项跨越式进展并非偶然。故事始于十分独特的转化路径:原用于治疗犬类肥大细胞瘤(MCT)的药物,如何跨越物种鸿沟为人类服务?
深度探索其生物机制,我们发现Tigilanol tiglate的双重抗癌特性:
- 血管爆破效应:药物能在48小时内选择性破坏肿瘤内皮细胞,阻断肿瘤营养供应通道,这种血管系统崩溃速度是传统靶向药物的10倍;
- 免疫激活链式反应:通过诱导癌细胞「自杀性焦亡」,释放大量危险信号分子(DAMPs),如同暴风雪中倒下的第一块多米诺骨牌,激活局部及全身T细胞风暴。
澳大利亚东北部雨林的Fontainea picrosperma树,这种常被误认为神圣图腾植物的成员,其未成熟种子提取物经化学结构改造后,最终被美国生物医学团队成功合成。这种从天然产物到合成药物的转变过程耗时7年,解决了原始植物工业化量产的难题。
三、破壁新战线:2a期试验的科学细节与突破意义
这项2a期试验严格遵循癌症研究金标准:
- 患者选择:仅招募ECOG评分≤2的晚期患者(即能正常生活)
- 肿瘤靶区:体表可触及肿瘤或超声可视肿瘤,精确性达毫米级
- 治疗方案:单针注射后持续观察至3个月,90%患者无需辅助治疗
值得关注的疗效节点:
- 首次注射后7-14天出现显著肿瘤塌陷
- 28天时52%患者达到完全缓解
- 60%患者肿瘤维持6个月无病状态
- 治疗部位创面愈合率达92%,几乎无瘢痕
对比传统软组织肉瘤治疗路径:
四、物种跃迁的科学启示:动物医学如何点亮人类希望
让人惊讶的是,该药物在犬类中的疗效更早展现了潜力。当兽医团队启动临床前研究时,两条金毛犬成为了关键性试验案例。注射3天后,它们肿瘤部位的毛细血管呈现「虫蛀式」破坏。随访数据显示:单次注射治疗后76%的MCT肿瘤完全消失,再次印证了跨物种抗癌机制的可行性[3]。
纪念斯隆凯特琳主任医师Ralph Weichselbaum指出:「我们一直在寻找既能直接消除肿瘤又不损伤正常组织的方案。这种药物展示出的血管选择性和免疫持久性,创造了『双重打击』效应的新范式。」
五、纽约癌症实验室:140年的转化医学基因
(图:纪念斯隆凯特琳癌症治疗中心实景图)
在QB46C-H07试验背后,是这个顶级研究机构深厚的转化医学积淀。从1884年最初的癌症病房,到1980年癌症研究所并入,近40年间共诞生9款FDA批准的创新药物。这次试验所在的介入肿瘤科研团队,拥有120多个专门研究肿瘤微环境的先进实验室。
值得关注的参与门槛:
- 肿瘤定位限制:必须位于体表或皮下等可注射区域
- 患者状态要求:活动能力需满足PS评分,但不强制要求基因检测
- 药物研发背景:目前无商业推广,仅通过临床试验机制应用
- 全球扩展计划:计划2024年底前启动欧洲多中心试验
六、未来展望:肿瘤靶向治疗的『第三路』可能
尽管数据充满希望,专家们强调仍需保持科学谨慎。澳大利亚昆士兰大学植物化学家Peter Bergner正在比较原始植物提取物与合成药物的活性差异。纪念斯隆凯特琳的分子生物学家团队则开启了「加密信号」研究——戴奥辛样结构的分子如何在不同物种中激活相似的免疫应答?
值得思考的技术路线选择:
- 联合治疗:是否与免疫检查点抑制剂形成协同效应?
- 新型递送:能否开发微环境响应型智能药物载体?
- 耐药监测:6个月无复发的持久性预言能否持续?
梅斯小编点评:
这个看似「灵光乍现」的医学突破,实则是产学研合作的典范。当一句「我们为什么不用自己的实验室合成品?」促成兽药向人药的跨越,这条药物研发路径值得我们深思。不过,对于正在苦苦寻找治疗方案的晚期患者来说,所有进展都是希望。值得提醒的是,6个月缓解期不能轻易等同于治愈预期,仍需等待更长期的跟踪数据。您如何看待这种从动物医学转化而来的新型抗癌策略?是否应该更多关注跨物种药物开发的临床价值?