胆道闭锁(BA)是新生儿期最为严重的肝胆疾病之一,以肝外胆管进行性炎症和纤维化为特征,最终导致胆汁淤积和肝硬化。目前,BA的病因尚未完全明确,可能与病毒感染、免疫异常或遗传因素有关。尽管Kasai手术(肝门肠吻合术)可暂时缓解症状,但多数患儿最终仍需肝移植。因此,深入探索BA的发病机制并寻找新的诊疗靶点至关重要。近年来,基质金属蛋白酶7(MMP7)被证实是诊断BA的重要血清标志物,但其在疾病进展中的具体作用机制尚不清楚。据MMP7作为一种蛋白水解酶,可能通过调控下游分子的表达参与BA的胆管损伤和肝纤维化过程。
2025年6月14日,复旦大学附属儿科医院王军锋、郑珊和陈功团队在《Hepatology Research》发表的研究发现,趋化因子CXCL6是MMP7的下游靶点,并在BA患儿的胆管上皮细胞中特异性高表达。
首先,对BA患者和正常对照(肝母细胞瘤旁正常肝)的肝组织进行单细胞RNA测序(scRNA-seq)分析,发现MMP7及其潜在下游靶点CXCL6在胆管上皮细胞中特异性高表达,且MMP7与CXCL6的表达呈显著正相关。
然后,研究团队从多维度验证了MMP7和CXCL6在肝组织中的表达情况。qRT-PCR和Western blot结果显示,BA组中MMP7和CXCL6的表达显著高于非BA胆汁淤积(CS)组和正常对照(NC)组。免疫组化和免疫荧光实验明确了MMP7和CXCL6共定位于胆管上皮细胞,并再一次验证了各组之间蛋白的表达量差异。
进一步通过对公共数据库和临床样本的分析发现,BA患者的MMP7和CXCL6表达随肝纤维化程度显著升高,提示他们可能参与了纤维化进程。
接着,研究者继续收集了BA、CS和NC组的血清样本并开展ELISA实验,结果提示BA患者血清中MMP7和CXCL6浓度显著升高,且两者对BA的诊断均具有较高的价值。
最后,为明确MMP7对CXCL6的调控作用,研究团队构建了MMP7过表达和敲低的原代胆管上皮细胞模型。通过Western blot探究MMP7表达改变对CXCL6的影响,结果提示:过表达MMP7后,细胞胞质和细胞上清中的CXCL6表达均有显著上升,敲低MMP7后则出现了相反的趋势。这说明胆管上皮细胞中的MMP7调控CXCL6的表达。
该研究首次揭示了CXCL6是BA的一种新型胆管标志物,是MMP7的下游靶点。在胆管上皮细胞中MMP7的表达能够促进CXCL6的产生。此外,MMP7和CXCL6可能在BA肝脏纤维化的过程中发挥重要作用。以现有证据可以推测,BA中MMP7/CXCL6轴可能通过招募中性粒细胞(如CD177+CXCR2+细胞)促进中性粒细胞胞外诱捕网(NETs)的形成,进而加剧胆管损伤和肝纤维化,但这还需要进一步体内外实验进行验证。综上所述,本研究的发现为BA的诊断和治疗提供了新思路和新靶点。
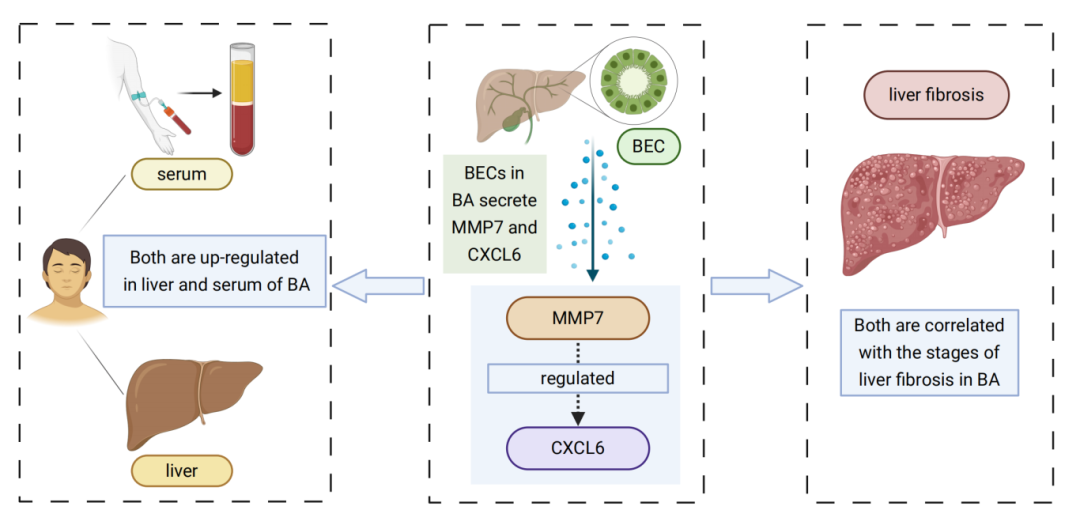
摘译自:KONG F, JIANG J, DU M, et al. CXCL6 Is a Novel Biliary Marker and a Downstream Target of MMP7 in Biliary Atresia[J]. Hepatol Res, 2025. DOI: 10.1111/hepr.14217. [Epub ahead of print].
