亮点总结
- 芦康沙妥珠单抗(Sac-TMT)作为抗TROP2抗体药物偶联物,在不可切除局部晚期及转移性三阴性乳腺癌(TNBC)及HR+/HER2-乳腺癌患者中展现出良好的安全性及诱人的抗肿瘤活性。
- 经过剂量递增,确定最大耐受剂量为5.5 mg/kg,推荐扩展剂量为4 mg/kg和5 mg/kg。
- 在Ⅱ期扩展队列中,TNBC患者的客观缓解率(ORR)达到34.8%至38.9%,HR+/HER2-乳腺癌患者ORR达到31.7%,显示其潜在的临床应用前景。
近日,发表于2025年《Journal of Hematology & Oncology》的一项由Ouyang等人发起的多中心I/II期临床研究(注册号:NCT04152499)公布了抗TROP2抗体药物偶联物Sac-TMT在不可切除局部晚期或转移性实体瘤患者中的安全性和疗效结果。该研究由中国四川科伦生物医药有限公司与美国默克公司联合支持,涵盖了多种类型晚期实体瘤患者,重点考察了三阴性乳腺癌及HR+/HER2-乳腺癌的治疗反应。研究验证了Sac-TMT较为良好的耐受性及显著的抗肿瘤活性,支持其在未来更大规模试验中的进一步应用。

免疫治疗已成为多种实体瘤,尤其是转移性三阴性乳腺癌的标准治疗组成部分,但仍存在显著的耐药和疾病进展问题,迫切需要新型治疗策略。TROP2是一种高表达于多种肿瘤类型表面的跨膜糖蛋白,与肿瘤增殖、迁移及不良预后密切相关,成为抗肿瘤靶点的研究热点。已有的抗TROP2 ADC,如Sacituzumab govitecan,已获批用于晚期TNBC及HR+/HER2-乳腺癌,显示出良好的疗效。Sac-TMT是新型抗TROP2 ADC,采用相同的抗体部分,搭配不同的连接子和派生自贝洛特康的拓扑异构酶I抑制剂KL610023,优化了ADC的稳定性和药理特性,有望减少毒副作用并提升治疗效果。
研究方法
本项开放标签、国际多中心临床试验包括Ⅰ期剂量探索和Ⅱ期剂量扩展两部分。
- Ⅰ期招募不可切除局部晚期或转移性实体瘤(包括但不限于乳腺癌、肺癌、胃癌等)患者,采用2 mg/kg至12 mg/kg的Sac-TMT静脉给药,每两周一次,旨在确定最大耐受剂量(MTD)及Ⅱ期推荐扩展剂量(RDE)。
- Ⅱ期专注于转移性TNBC和HR+/HER2-乳腺癌队列,根据Ⅰ期确定的RDE进行治疗,主要终点为客观缓解率(ORR),次要终点包括无进展生存期(PFS)、总体生存期(OS)及安全性分析。
研究结果
Ⅰ期剂量递增
共计30名患者接受Sac-TMT治疗,剂量组分布如下:2 mg/kg (4人),4 mg/kg (7人),5 mg/kg (7人),5.5 mg/kg (5人),6 mg/kg (7人)。
- 剂量限制性毒性(DLT)包括3级口腔炎、3级皮疹及3级荨麻疹,主要分布在4 mg/kg及以上剂量组。
- 6 mg/kg剂量组中,29%的患者出现DLT,最大耐受剂量确定为5.5 mg/kg,基于安全和毒性数据,Ⅱ期推荐剂量为4 mg/kg及5 mg/kg。
- 常见治疗相关不良事件(TRAEs)包括恶心(63%)、脱发(57%)、贫血(50%),多数为轻/中度,治疗相关3/4级不良事件占57%,无人出现治疗相关死亡。
Ⅰ期关键药代动力学参数
Sac-TMT ADC及总抗体浓度随剂量升高呈线性增加,KL610023(payload)浓度也随剂量增加。
抗药物抗体(ADA)出现率在低剂量组较低,仅零星发生。
Ⅱ期剂量扩展(TNBC及HR+/HER2-乳腺癌)
(表1:Ⅱ期队列肿瘤反应总结)
患者治疗期间多数报告至少一例TRAE,TNBC及HR+/HER2-队列中,最常见的3/4级TRAEs为贫血、白细胞减少和中性粒细胞减少。治疗中断和剂量调整均较少,极少因不良事件完全终止治疗。
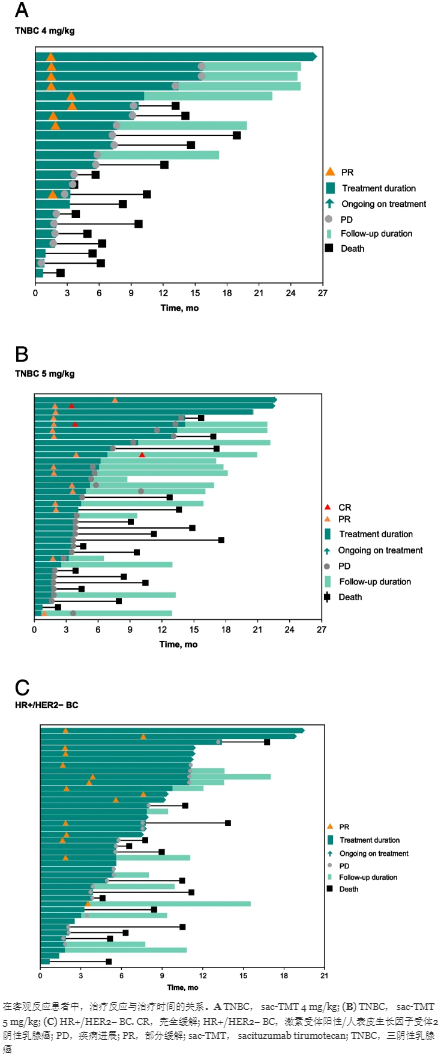
研究中部分患者治疗时间与反应示意图(TNBC 4 mg/kg、5 mg/kg及HR+/HER2- 5 mg/kg)
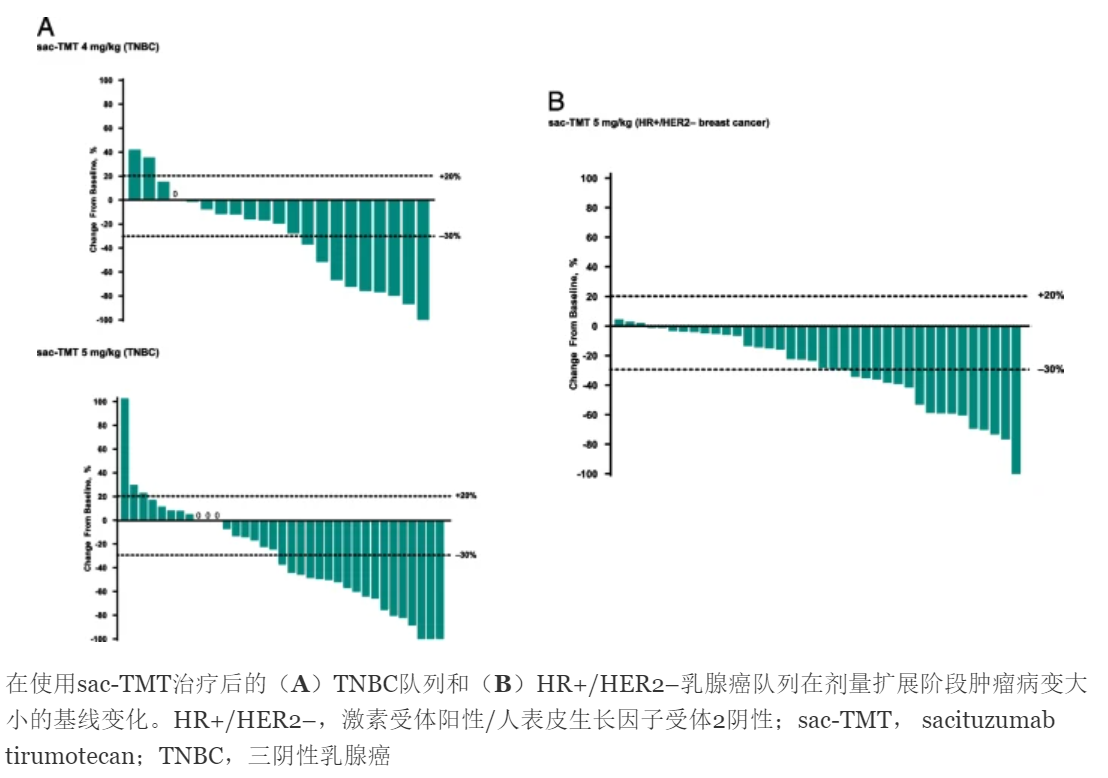
肿瘤病灶大小变化瀑布图,显示多数患者有肿瘤缩小趋势。
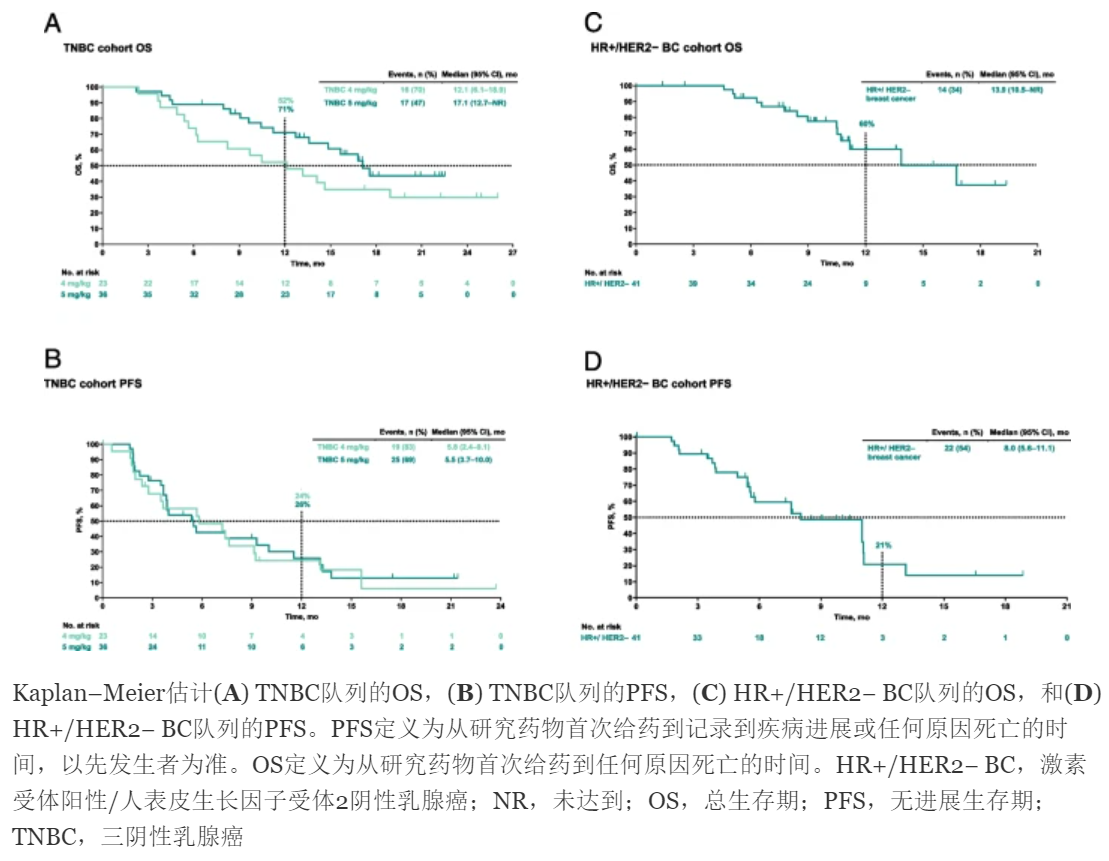
存曲线Kaplan-Meier图,显示3组的PFS及OS估计情况。
本研究首次系统评估了Sac-TMT在不可切除晚期实体瘤中的安全性及初步疗效,特别是在转移性TNBC及HR+/HER2-乳腺癌中的应用。Sac-TMT利用稳定的连接子确保payload高效释放,减少非特异性毒副作用,Ⅰ期确认最大耐受剂量为5.5 mg/kg,常见毒性主要为口腔炎及皮肤反应,均可被有效管理。
2个推荐剂量(4 mg/kg与5 mg/kg)在Ⅱ期均展现出较高的ORR及较长的缓解持续时间,与目前获批的Sacituzumab govitecan疗效相仿,但显示出潜在更优的毒性谱,尤其中性粒细胞减少等血液毒性相对较低,提示新型payload的优势。
此外,HR+/HER2-乳腺癌患者组同样表现出可观的治疗反应,提供了该ADC在非三阴乳腺癌中的进一步开发依据。鉴于该项研究的受试患者普遍为预处理、高度耐药的群体,Sac-TMT的活性尤为值得关注。
当前研究局限于单臂设计及样本量有限,未来多中心、随机对照的Ⅲ期研究将更准确评估其疗效及安全优势,如OptiTROP-Breast01研究中数据显示Sac-TMT单药治疗TNBC有显著的疗效提升,预示其潜在临床价值。
梅斯小编点评
Sac-TMT作为一款结构优化的新型抗TROP2 ADC,不仅凭借创新的payload带来了更优药代学特性,且其良好耐受性和临床活性为晚期难治乳腺癌患者提供了新的选择。尤其是TNBC患者面对有限的治疗手段,该药的出现无疑为临床带来曙光。未来结合免疫疗法的联合用药研究,以及生物标志物筛选与机制探究,将推动该领域个体化治疗方案的进步,为患者带来更精准和有效的治疗管理。
原文出处
Ouyang Q, Rodon J, Liang Y, et al. Results of a phase 1/2 study of 芦康沙妥珠单抗 in patients with unresectable locally advanced or metastatic solid tumors refractory to standard therapies. J Hematol Oncol. 2025;18:61. https://doi.org/10.1186/s13045-025-01705-2