人表皮生长因子受体2(HER2)是乳腺癌诊疗的关键生物标志物。本文综述了HER2的分子生物学特性、检测方法以及呈现了5个典型免疫组化和FISH的结果对比、临床意义及新兴治疗方式,重点关注了FDA近期针对HER2低表达(HER2-low)和超低表达(HER2-ultralow)亚型的最新批准进展。
本期就由加州病理科住院医师雨落轻尘为大家带来HER2/ERBB2在乳腺癌诊疗中的最新进展。
一、HER2分子生物学基础
基因与蛋白结构
ERBB2基因:位于染色体17q12,跨度约327 kb
蛋白:跨膜酪氨酸激酶受体
功能:与EGFR/ERBB3/4形成同源/异源二聚体,激活下游通路:
-
PI3K-AKT通路:细胞存活
-
RAS-MAPK通路:增殖/迁移
治疗靶点
药物类型
代表药物
单克隆抗体
曲妥珠单抗、帕妥珠单抗
抗体偶联药物
德曲妥珠单抗(T-DXd)
酪氨酸激酶抑制剂
来那替尼、图卡替尼
免疫疗法
HER2特异性CAR-T细胞
二、乳腺癌亚型中的临床意义
分子分型与HER2阳性率
亚型
占比
HER2状态
特征
Luminal A型
40-60%
阴性
低级别,内分泌治疗敏感
Luminal B型
20-30%
+/-
高复发风险
HER2过表达型
10-20%
阳性
侵袭性强,抗HER2治疗有效
基底样型
15-20%
阴性
三阴性,高级别
三、组织学特异的HER2表达
不同亚型的异质性
1.浸润性导管癌(NST型)
-
髓样特征:通常三阴性
-
多形性癌:19% HER2阳性
-
皮脂腺分化:33.3% HER2阳性
2.浸润性小叶癌(ILC)
-
经典ILC:罕见HER2阳性(0-2%)
-
多形性ILC:可表达HER2
3.特殊亚型
亚型
HER2阳性率
特征
顶浆分泌癌
25-100%
ER/PR阴性,AR阳性
神经内分泌肿瘤
通常阴性
常ER/PR阳性
涎腺型肿瘤
三阴性
如腺样囊性癌
四、HER2检测指南(ASCO-CAP 2023更新)
核心建议
检测指征:
-
所有新发乳腺癌必须检测
-
转移病灶需重新检测
IHC判读标准:
评分
染色模式
处理方案
0
无染色
阴性
1+
微弱/隐约可见膜染色
阴性
2+
弱-中度不完整膜染色
需ISH验证
3+
强而完整膜染色
阳性
FISH判读流程:
阳性:HER2/CEP17 ≥2.0 且 HER2拷贝数/细胞 ≥4.0
需IHC复核的临界病例:
-
第2组(比值≥2.0,拷贝数<4.0)
-
第3组(拷贝数≥6.0,比值<2.0)
IHC-FISH对照的五组范例:
1.Case 1
IHC 3+阳性; HER2/CEP17比值 >2.0;拷贝数>4.0
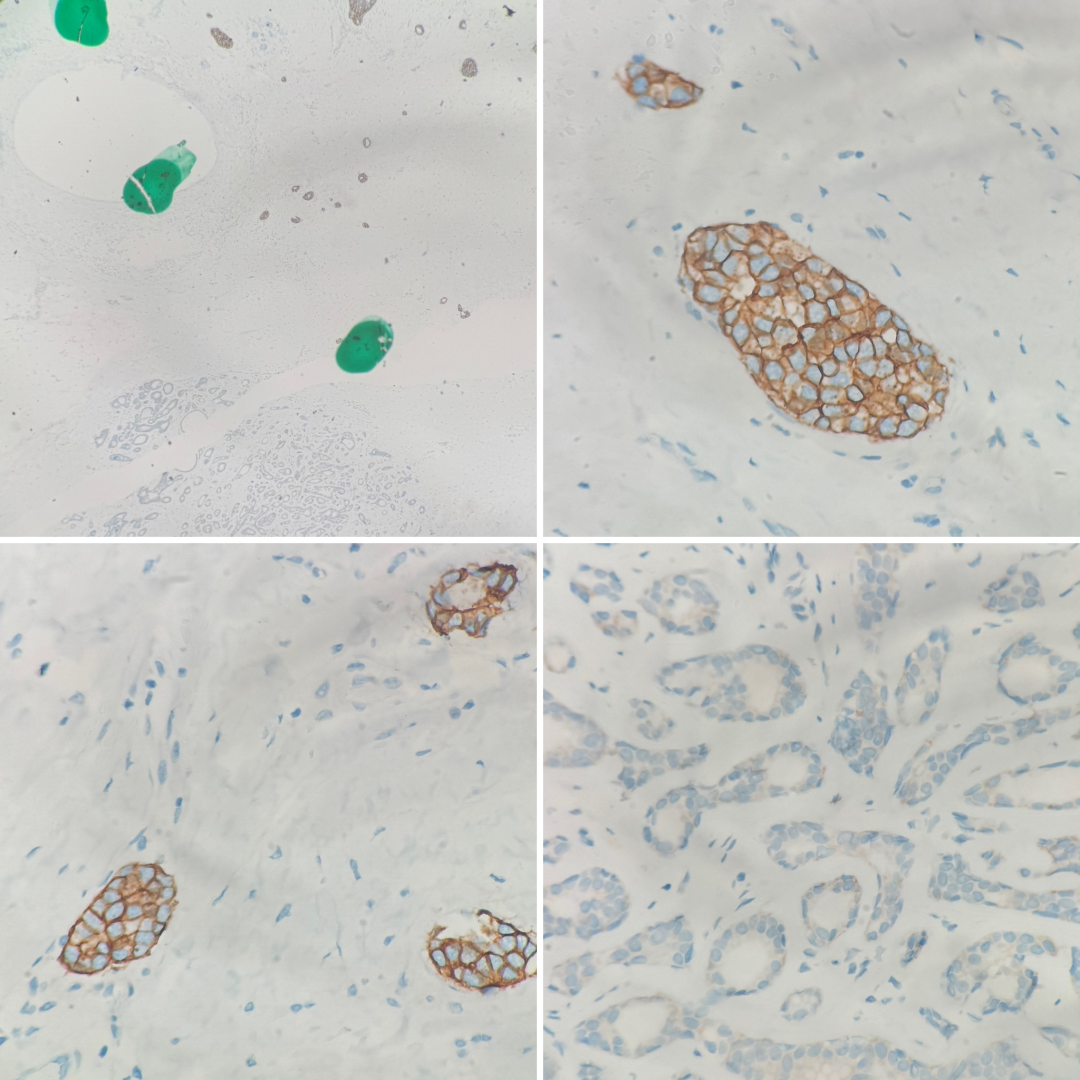
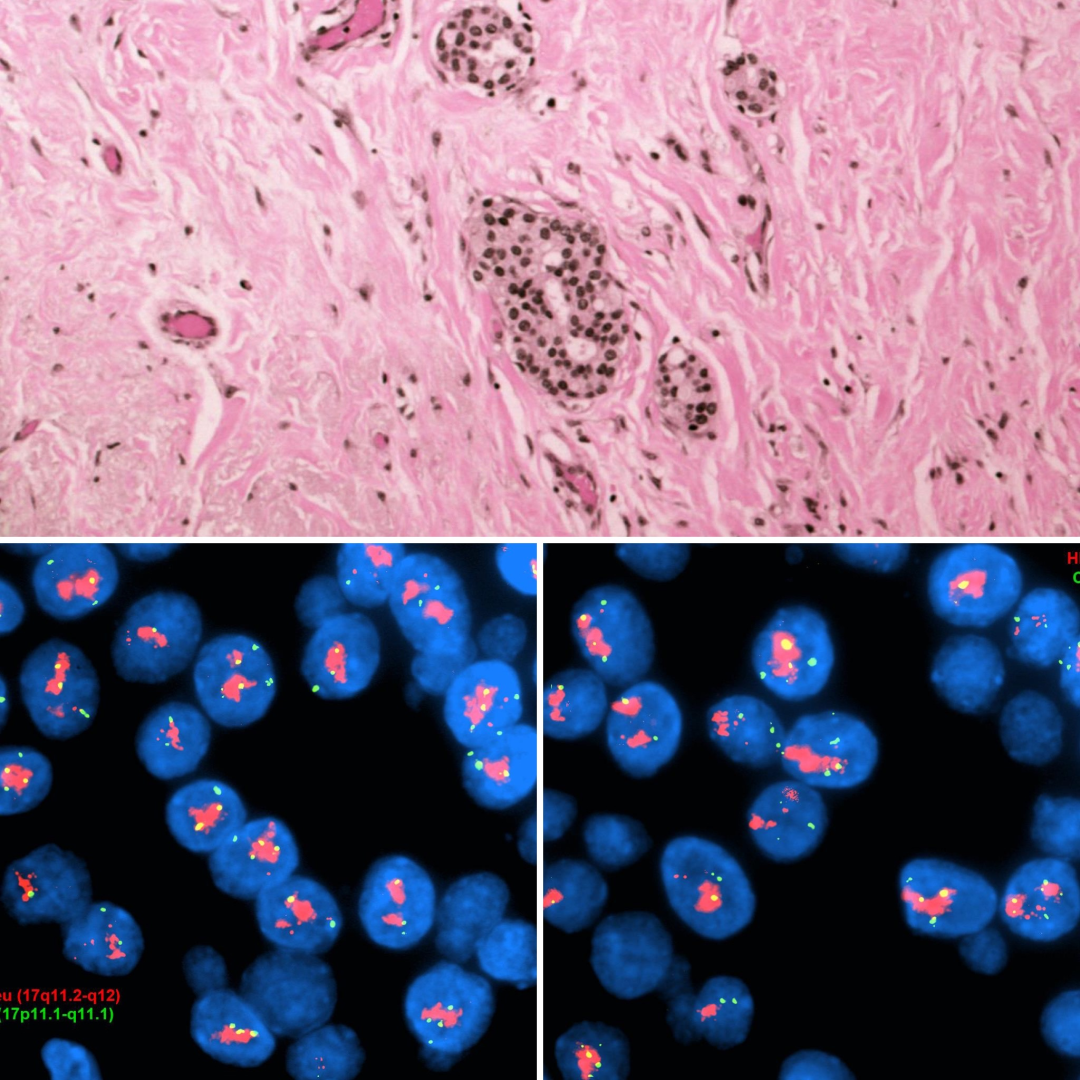
Case 1
2.Case 2
IHC 0-阴性, ultra-low; HER2/CEP17比值 <2.0;拷贝数<4.0
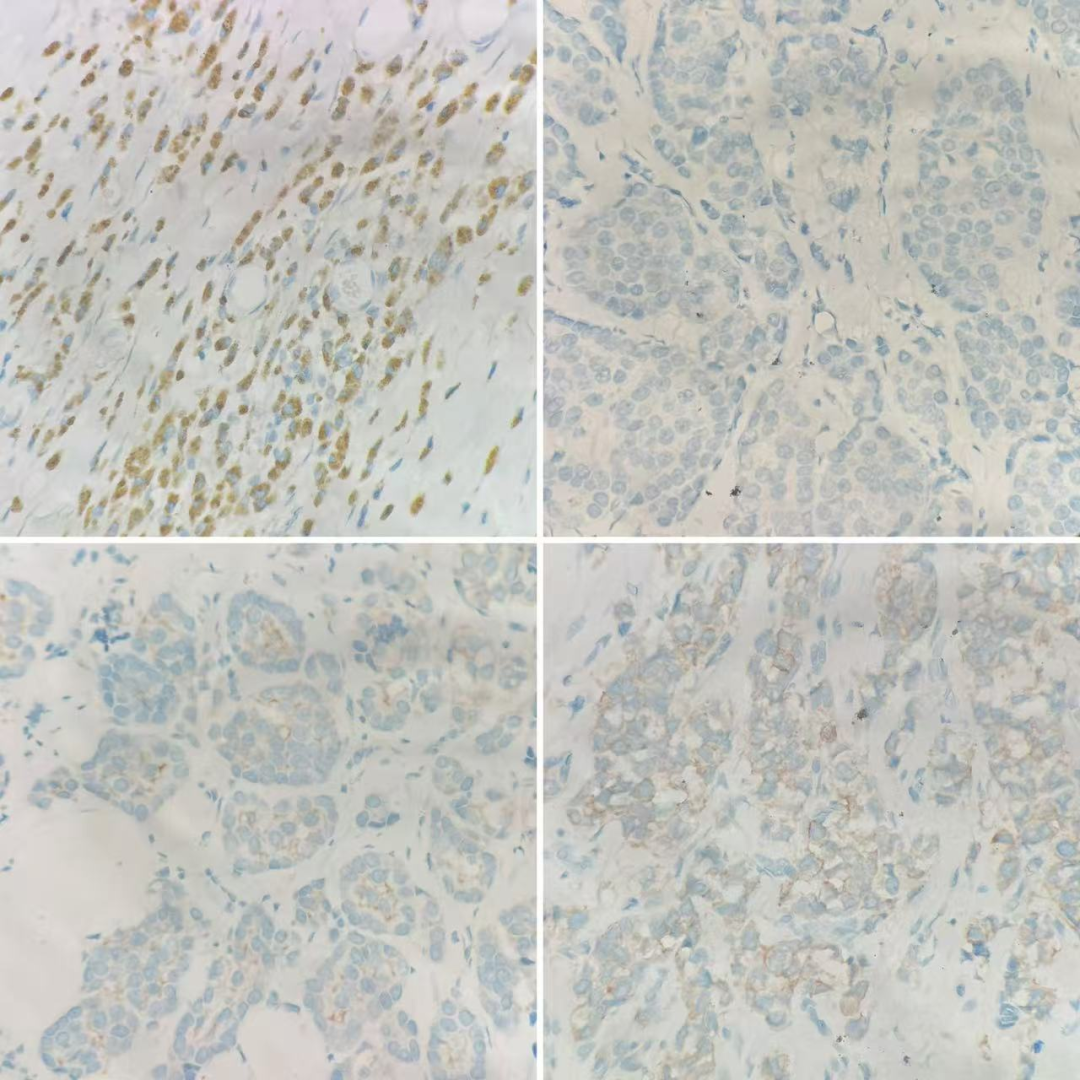
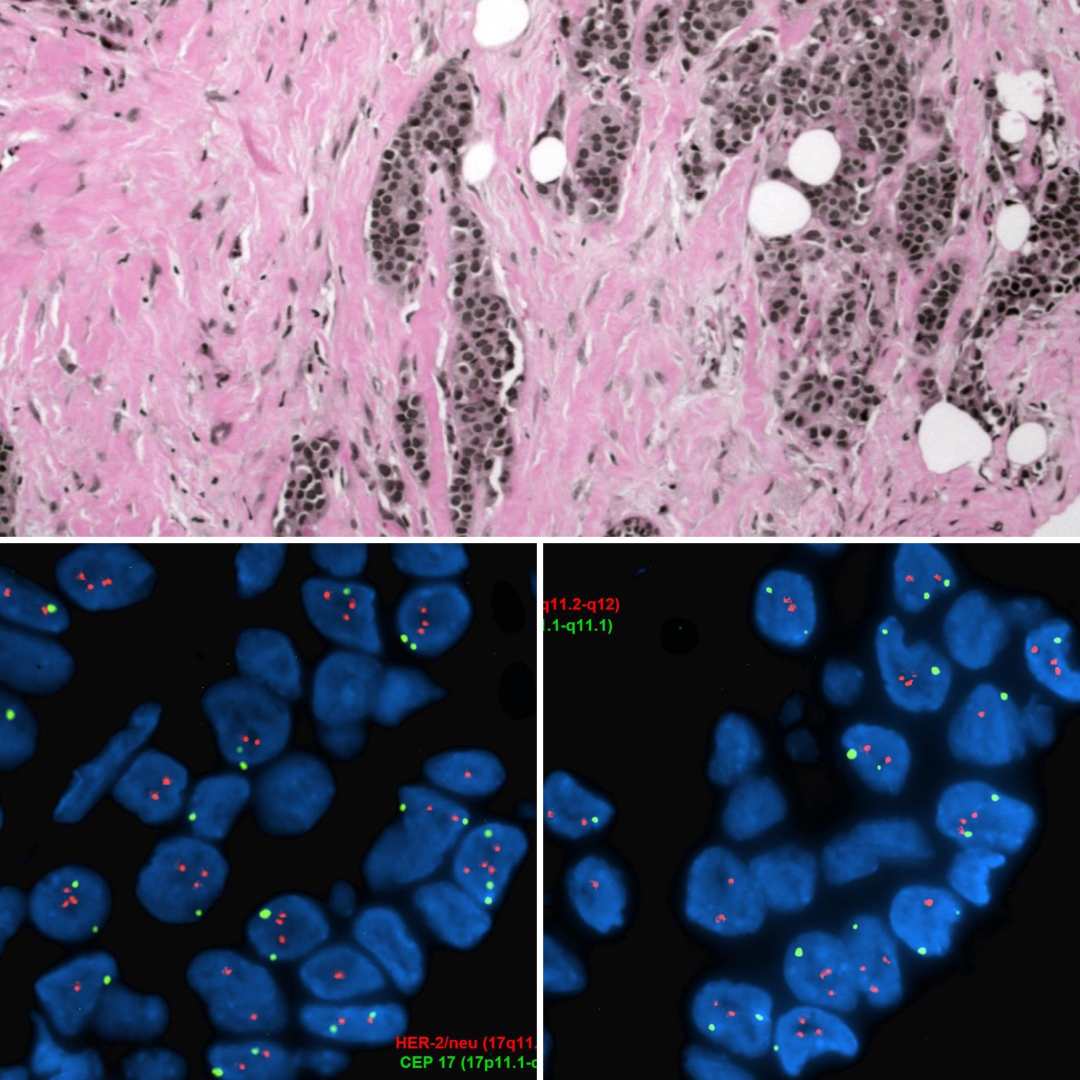
Case 2
3. Case 3
IHC 2+不确定阳性; HER2/CEP17比值 >2.0;拷贝数<4.0
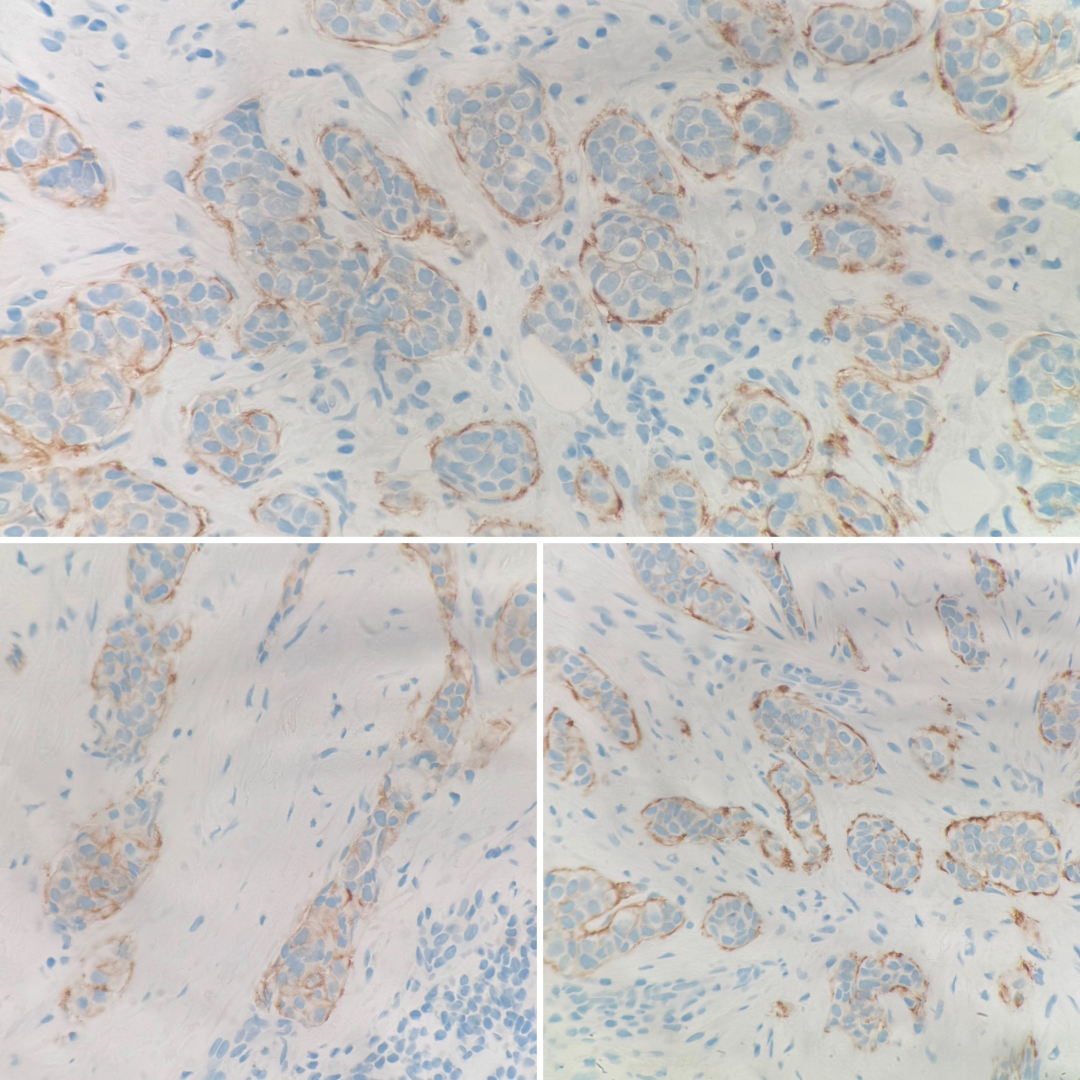
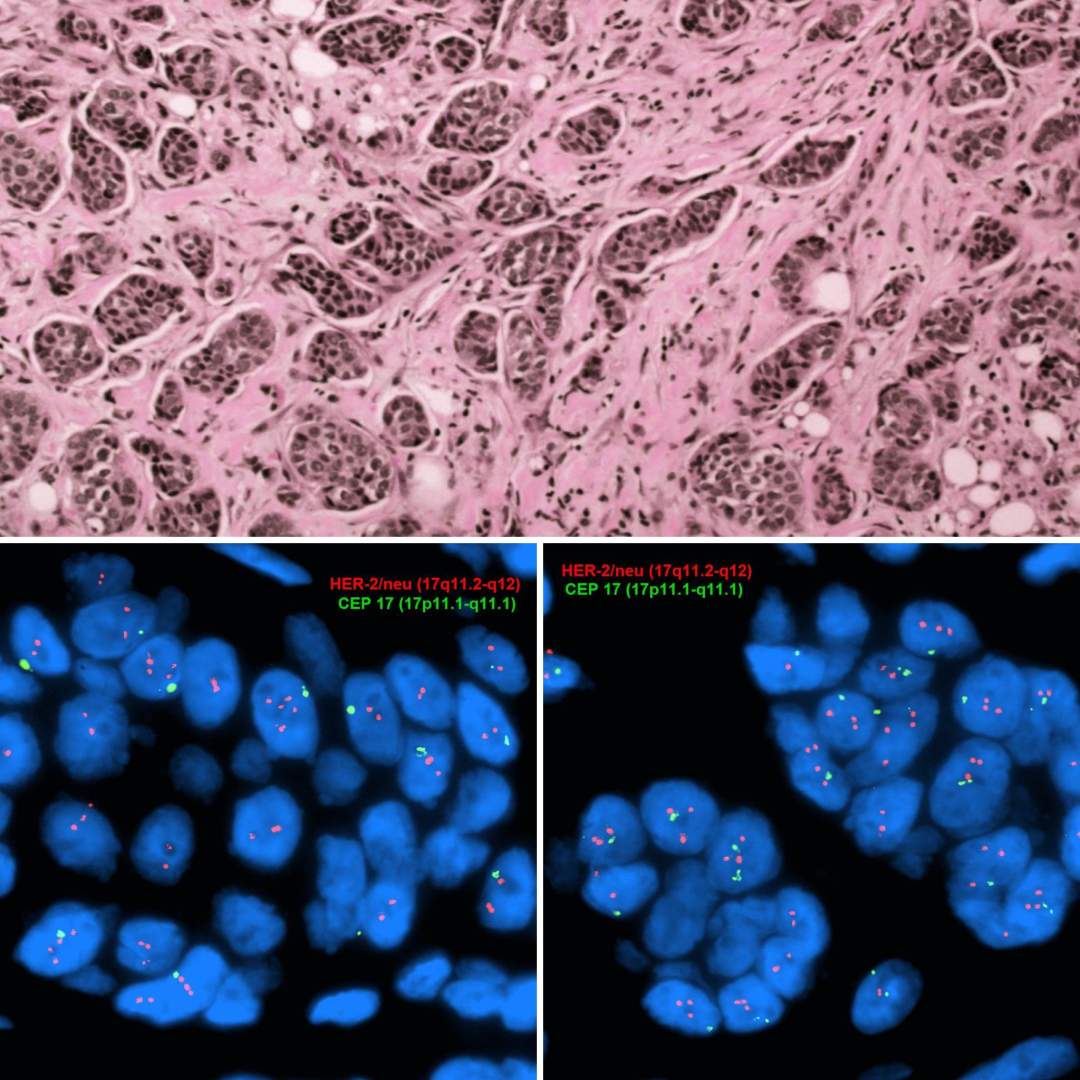
Case 3
4.Case 4
IHC 2+不确定阳性; HER2/CEP17比值 <2.0;拷贝数<4.0
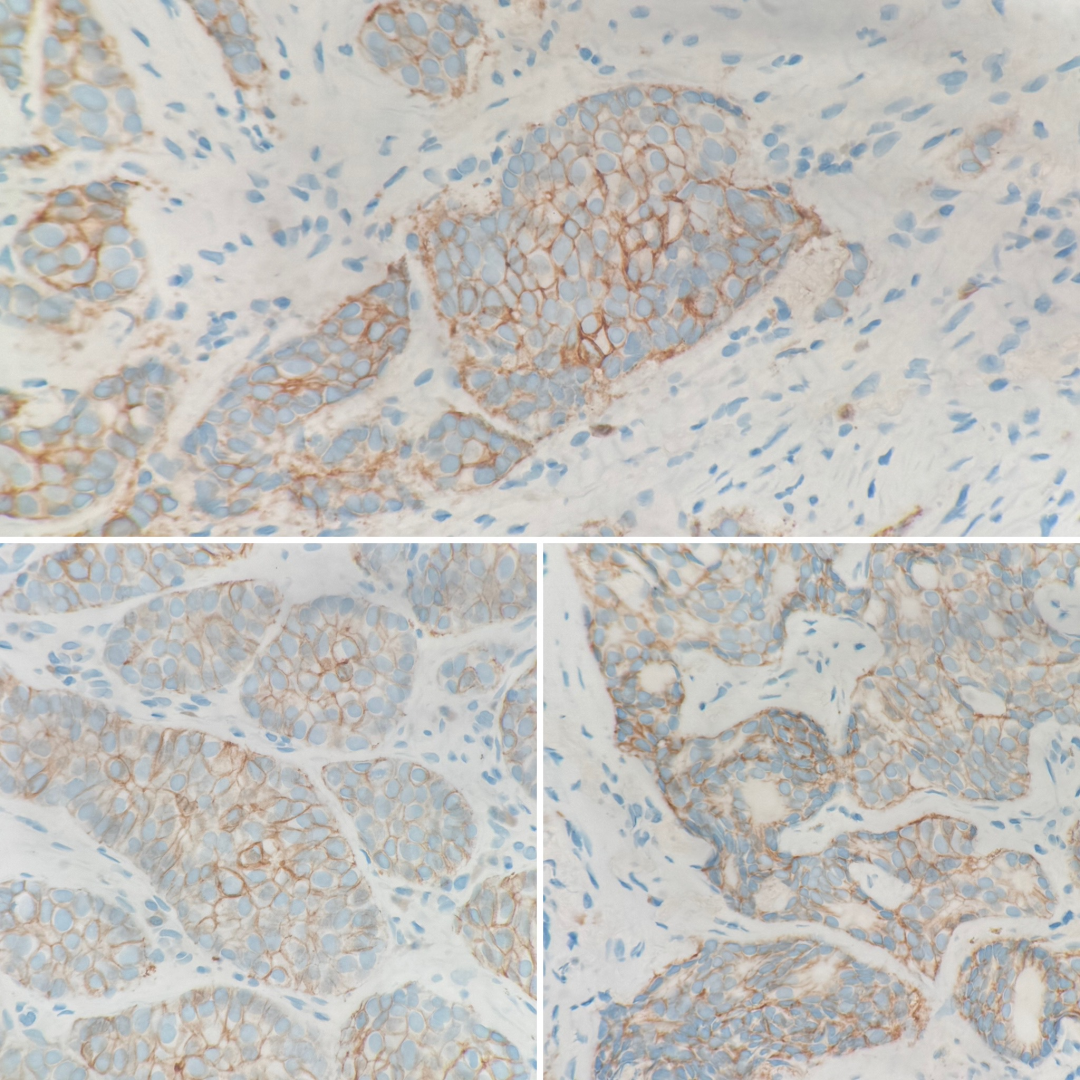
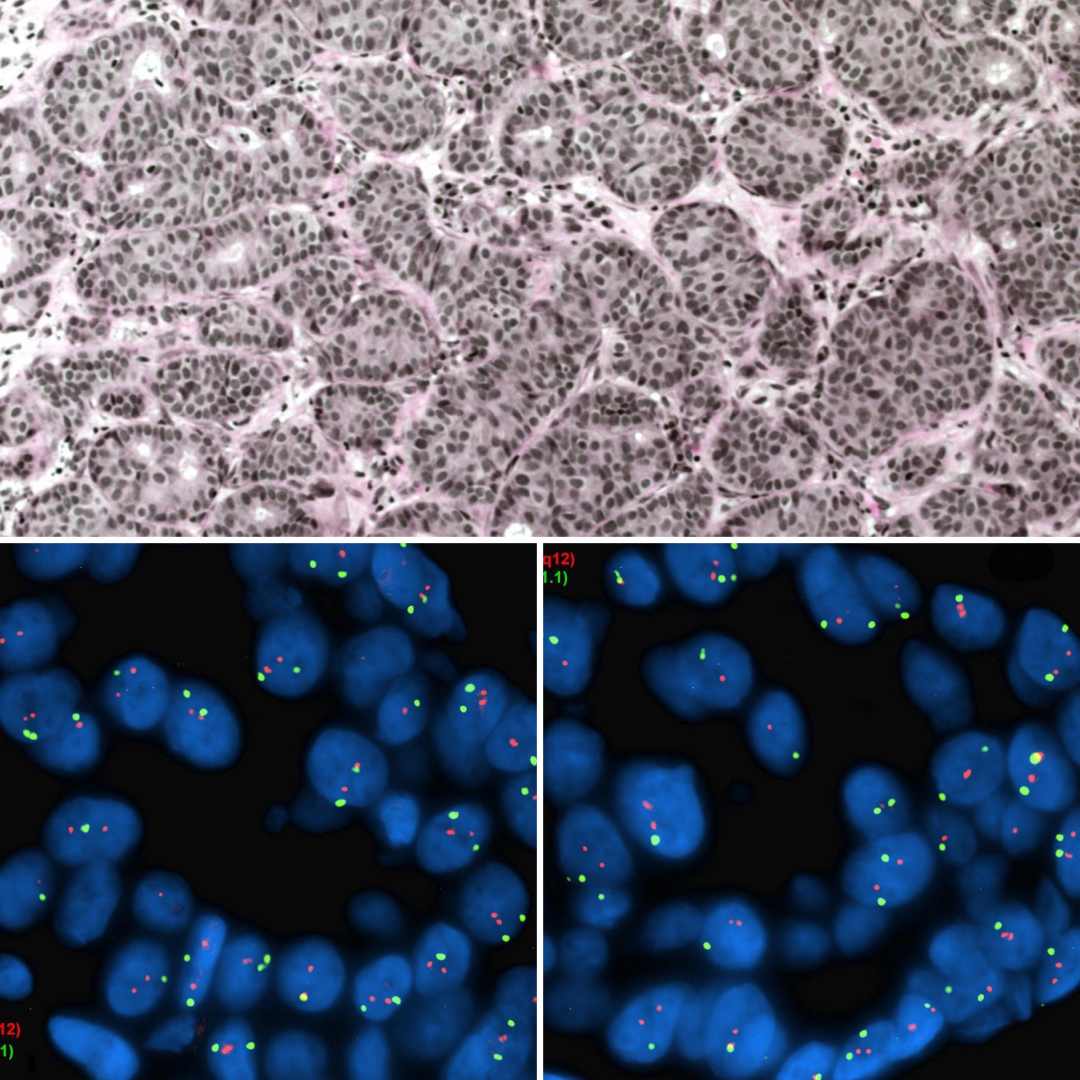
Case 4
5.Case 5
IHC 3+阳性; HER2/CEP17比值 >2.0;拷贝数>4.0
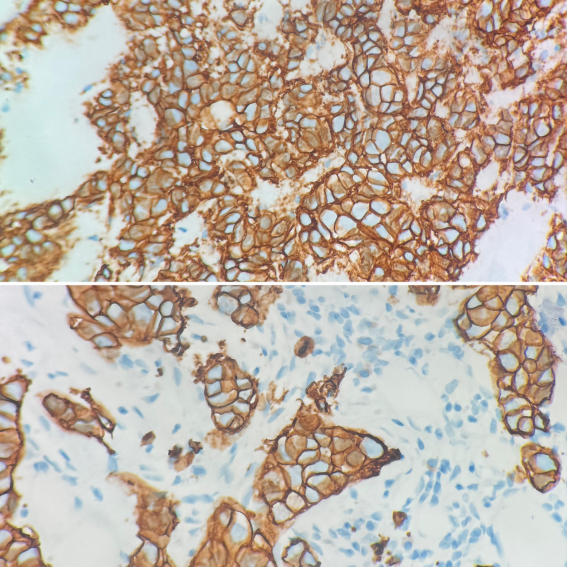
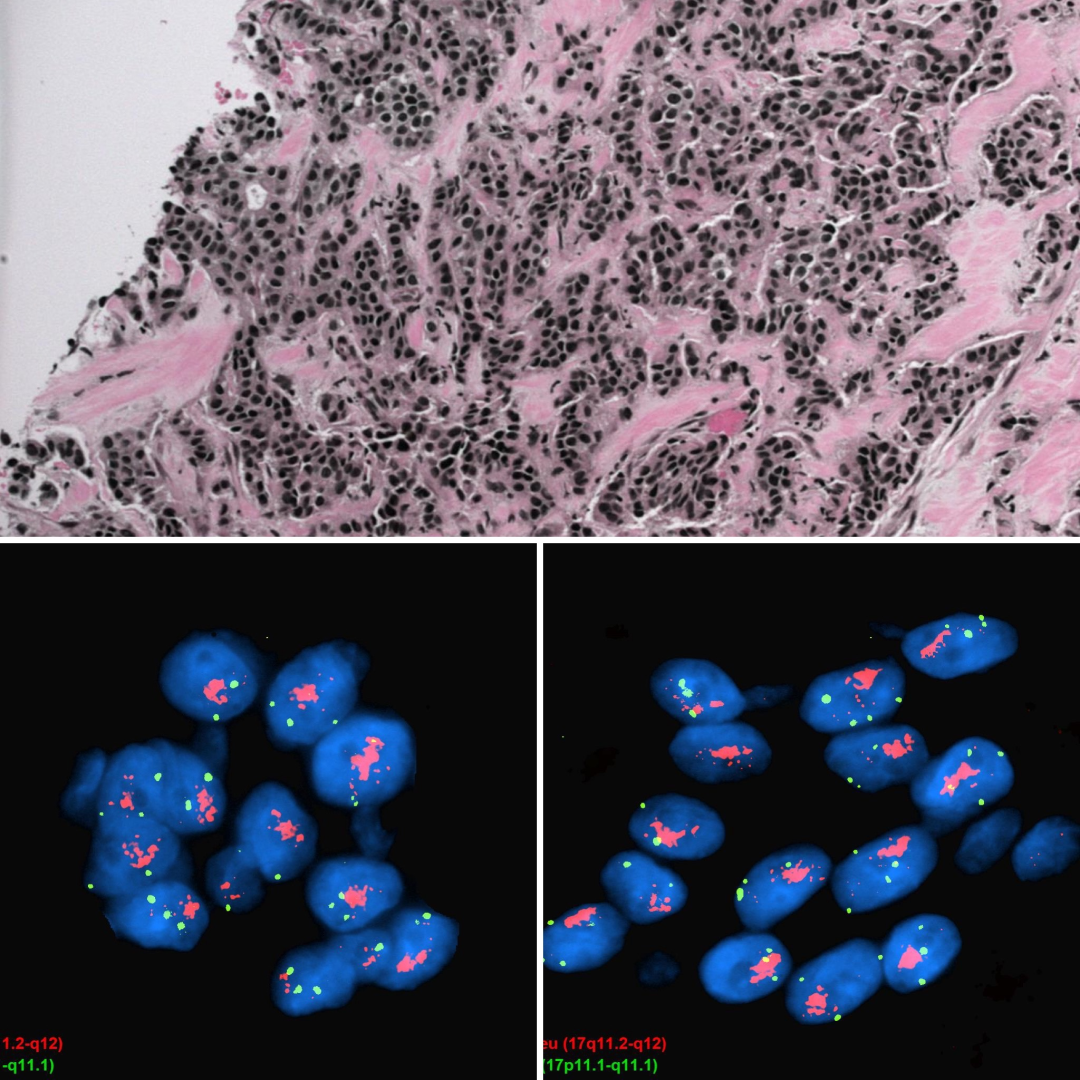
Case 5
五、HER2低表达与超低表达:新进展
定义与临床价值
-
HER2低表达:IHC 1+ 或 IHC 2+/ISH-
-
HER2超低表达:≤10%肿瘤细胞呈现微弱膜染色(IHC 0但膜染色)
FDA批准药物(2025)
Fam-德曲妥珠单抗-nxki(Enhertu):
-
适应症:不可切除/转移性HR+ HER2低表达或超低表达乳腺癌
-
伴随诊断:Ventana PATHWAY anti-HER2 (4B5)检测
临床试验证据
DESTINY-Breast04研究:
-
T-DXd vs 化疗治疗HER2低表达转移性乳腺癌
-
无进展生存期:9.9 vs 5.1个月(HR=0.50; p<0.001)
-
总生存期:23.4 vs 16.8个月(HR=0.64; p=0.001)
六、HER2分析前的重要变量:冷缺血时间(CIT)
对检测结果的影响
CIT >1小时导致组织降解:
-
HER2 IHC染色强度改变
-
FISH检测HER2/CEP17比值降低
最佳实践:
-
离体后≤60分钟内用10%中性福尔马林固定
CIT对生物标志物的影响
CIT时长
HER2 IHC变化
HER2 FISH比值变化
≤1小时
轻微
变异度<10%
>4小时
假阴性风险↑
比值降低0.29–0.98
七、潜在争议
1.HER2低表达治疗获益争议:
NSABP B-47试验:早期HER2低表达乳腺癌中,曲妥珠单抗未改善生存
-
5年DFS:89.6%(化疗+曲妥珠) vs 89.2%(单纯化疗)
2.HER2超低表达的生物学意义:
1,363例患者研究显示:
-
与HER2零表达/低表达的临床病理差异(如HR状态、Ki-67)
-
无病生存期无显著差异(P>0.05)
八、核心结论
德曲妥珠单抗的出现,为HR阳性且HER2低表达或超低表达的转移性乳腺癌患者提供了新的治疗选择,拓展了既有治疗格局。在HER2检测方面,应根据组织学特征优先检测某些特殊亚型乳腺癌,如顶浆分泌癌和多形性癌。对于FISH检测结果接近临界值的病例,必须使用相同组织样本进行IHC复核,以确保诊断准确性。同时,分析前变量的控制同样关键,尤其是样本的冷缺血时间应控制在60分钟以内,以最大限度提升HER2检测的准确度。然而,目前HER2超低表达状态的生物学意义仍不明朗,尚需进一步研究加以阐明。临床要点提示:即便IHC评分为0,若存在轻微膜染色,也应高度警惕HER2超低表达的可能性,因为这类患者亦可能符合使用Enhertu治疗的标准。
参考文献:
[1]Larionov AA. Current Therapies for Human Epidermal Growth Factor Receptor 2-Positive Metastatic Breast Cancer Patients. Front Oncol. 2018 Apr 3;8:89. doi: 10.3389/fonc.2018.00089. PMID: 29670855; PMCID: PMC5894159.
[2]WHO Classification of Tumours Editorial Board. (2023). Breast tumours. In WHO classification of tumours, 5th edition, volume 2. International Agency for Research on Cancer. Retrieved from https://tumourclassification.iarc.who.int/chaptercontent/32/18
[3]https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-fam-trastuzumab-deruxtecan-nxki-unresectable-or-metastatic-hr-positive-her2-low-or her2#:~:text=ultralow%20breast%20cancer-,FDA%20approves%20fam%2Dtrastuzumab%20deruxtecan%2Dnxki%20for%20unresectable%20or%20metastatic,%2C%20Daiichi%20Sankyo%2C%20Inc.)
[4]National Comprehensive Cancer Network. (2025). NCCN Clinical Practice Guidelines in Oncology: Breast Cancer (Version X.X). Retrieved June 15, 2025, from https://www.nccn.org/professionals/physician_gls/pdf/breast.pdf
[5]Wolff AC, Hammond ME, Hicks DG, Dowsett M, McShane LM, Allison KH, Allred DC, Bartlett JM, Bilous M, Fitzgibbons P, Hanna W, Jenkins RB, Mangu PB, Paik S, Perez EA, Press MF, Spears PA, Vance GH, Viale G, Hayes DF; American Society of Clinical Oncology; College of American Pathologists. Recommendations for human epidermal growth factor receptor 2 testing in breast cancer: American Society of Clinical Oncology/College of American Pathologists clinical practice guideline update. Arch Pathol Lab Med. 2014 Feb;138(2):241-56. doi: 10.5858/arpa.2013-0953-SA. Epub 2013 Oct 7. PMID: 24099077; PMCID: PMC4086638.
[6]Li J, Wang X, Wang S, Wang S, Wang T, Liu Y, Geng C, Jin F, Yin Y, Zhang Q, Song E, Wu J, Jiang Z; Chinese Society of Clinical Oncology Breast cancer committee; Chinese Anti-Cancer Association; Committee of Breast Cancer Society. Expert consensus on the clinical diagnosis and targeted therapy of HER2 breast cancer (2023 edition). Transl Breast Cancer Res. 2022 Oct 31;3:30. doi: 10.21037/tbcr-22-48. PMID: 38751529; PMCID: PMC11093007.
[7]Ghlichloo I, Shi WJ, Fadare O. The effect of prolonged cold ischemia time on breast cancer biomarker expression after neoadjuvant chemotherapy. Pathol Res Pract. 2025 Feb;266:155781. doi: 10.1016/j.prp.2024.155781. Epub 2024 Dec 18. PMID: 39709874.
[8]Fehrenbacher L, Cecchini RS, Geyer CE Jr, Rastogi P, Costantino JP, Atkins JN, Crown JP, Polikoff J, Boileau JF, Provencher L, Stokoe C, Moore TD, Robidoux A, Flynn PJ, Borges VF, Albain KS, Swain SM, Paik S, Mamounas EP, Wolmark N. NSABP B-47/NRG Oncology Phase III Randomized Trial Comparing Adjuvant Chemotherapy With or Without Trastuzumab in High-Risk Invasive Breast Cancer Negative for HER2 by FISH and With IHC 1+ or 2. J Clin Oncol. 2020 Feb 10;38(5):444-453. doi: 10.1200/JCO.19.01455. Epub 2019 Dec 10. PMID: 31821109; PMCID: PMC7007289.