前言
近年来,随着核苷(酸)类似物(NAs)和干扰素等药物的广泛应用,国内外指南对于慢性乙型肝炎(乙肝)抗病毒治疗的适应证均已逐步放宽。2021年,中国慢性乙肝领域首个原研的口服抗病毒药物--艾米替诺福韦(TMF)上市,为广大慢性乙肝患者带来新选择。我们欣喜地发现,中国肝病/感染领域的研究进展、诊疗理念等正在发生日新月异的变化。
为帮助学界和业界同仁及时了解最新、最热的肝病领域学术研究进展和动态,北京医药科学技术发展协会联合肝胆相照平台特别打造全新栏目——“沐语新声”。
近日,第34届亚太肝病学会年会(APASL 2025)在北京国家会议中心隆重举行。会议期间,郑州大学第一附属医院曾庆磊教授团队关于TMF有多项新成果发布,肝胆相照平台特邀曾庆磊教授分享研究成果与心得体会,现整理如下。
肝胆相照平台:我们了解到,您的团队有多项研究在APASL上公布。其中,一项关于TMF用于慢性乙型肝炎(CHB)孕妇的研究引起了广泛关注,能否请您介绍一下这项研究?
曾庆磊教授:TMF作为我国自主研发的I类新药,在上市前经过一系列严格的临床试验,已充分证明其具备良好的疗效与安全性。然而,针对特殊人群,尤其是孕妇群体的相关研究却相对较少。我们开展的此项研究并非特意针对孕妇群体,而是在众多TMF治疗的CHB患者中,有部分是处于育龄期的女性,她们在孕前就以TMF治疗,随后怀孕,在整个孕期未更换治疗方案。于是,我们通过这一研究探讨了TMF治疗CHB孕妇的疗效与安全性,及其对乙型肝炎病毒母婴传播(HBV-MTCT)的阻断作用。
【研究方法】
回顾性收集2022年1月至2024年9月在郑州大学第一附属医院和许昌市中心医院接受TMF(每日25 mg,餐后口服)治疗并妊娠的13例育龄女性的临床资料。分析基线期、孕期以及产后7个月内HBV标志物、生化指标、血常规等参数的变化和不良事件的发生情况,同时评估婴儿出生时和7月龄时的生长指标、乙肝疫苗免疫接种效果。
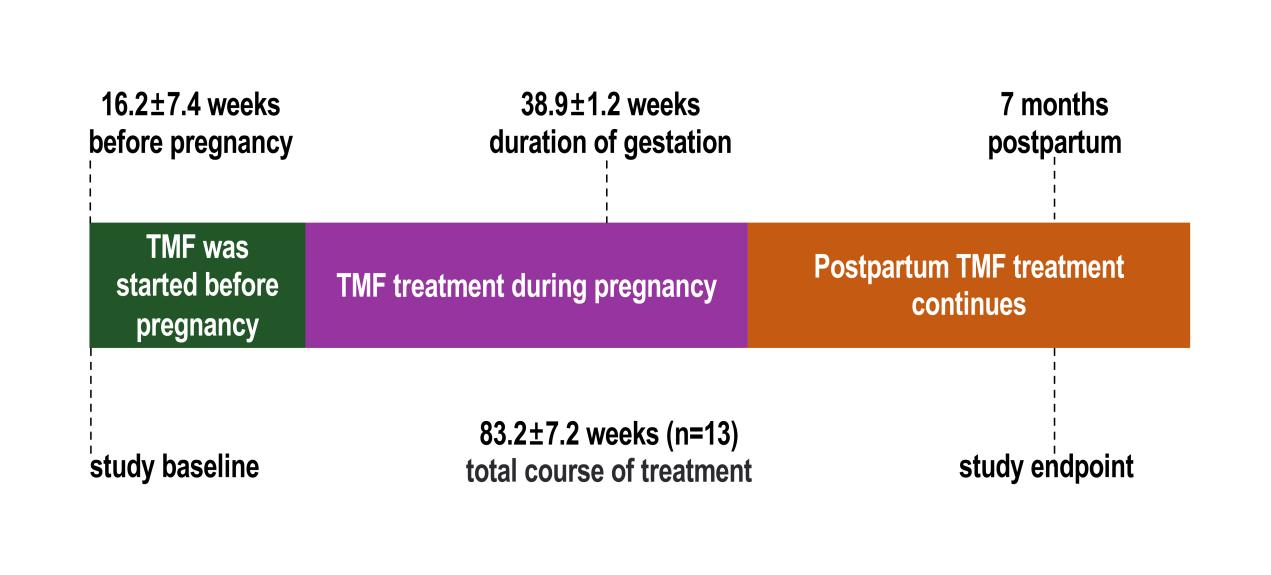
研究设计
【研究结果】
(1)基线期(孕前期16.2±7.4周):13例育龄女性中10例乙肝e抗原(HBeAg)阳性,年龄29.4±4.1岁,HBV DNA水平为5.6±3.3 log10IU/mL。丙氨酸氨基转移酶(ALT)水平为127.2±77.3U/L,血常规和肾功能指标均正常。
(2)孕期:孕妇的HBV DNA和ALT水平逐渐下降,分娩时分别降至0.5±1.2 log10IU/mL和20.9±14.3U/L。此外,血红蛋白和肌酐水平逐渐降低,估算肾小球滤过率(eGFR)逐渐升高。
(3)产后7个月:共有1名女性[7.7%(1/13)]实现HBeAg血清学转换,所有女性的HBV DNA水平均低于检测下限(LLOQ,<25IU/mL),ALT水平为18.5±8.0U/L,血红蛋白、血清肌酐、eGFR水平恢复至基线水平。
(4)治疗期间的主要不良事件为恶心[84.6%(11/13)]、厌食[69.2%(9/13)]和乏力[53.8%(7/13)],主要并发症为胎膜早破[15.4%(2/13)]。
(5)13名婴儿出生时的胎龄为38.9±1.2周,其中7名为男婴,无早产或延期出生的情况,也无出生缺陷或畸形。出生后1分钟Apgar评分为9.4±0.7,出生时的生长指标(身高、体重、头围等)均正常。所有婴儿均接受了标准的乙肝免疫预防。8例婴儿进行母乳喂养。
(6)婴儿7月龄时,生长指标正常,13例婴儿均成功阻断HBV-MTCT,乙肝表面抗体水平为502.4±292.0mIU/mL。
【研究结论】
本研究首次证实TMF治疗CHB孕妇具有良好的母婴安全性和有效性,联合标准的乙肝疫苗免疫接种,可成功阻断HBV-MTCT。
肝胆相照平台:除了用于CHB孕妇这一特殊人群,您的团队还关注了TMF在CHB相关肝硬化人群中的疗效与安全性,能否请您介绍下研究结果?
曾庆磊教授:在真实世界中,关于TMF治疗CHB相关肝硬化患者疗效和安全性的数据较少。本研究旨在评估TMF治疗CHB相关肝硬化患者48周的疗效和安全性,最初发表于《延安大学学报(医学版)》上。研究发表时,真实世界中针对TMF治疗此类疾病的相关研究几乎处于空白状态,本研究是国内较早发表的关于TMF治疗CHB相关肝硬化的真实世界研究。
【研究方法】
这是一项回顾性单臂研究,纳入了2021年1月至2023年8月在郑州大学第一附属医院接受TMF或TAF治疗(每日25mg)的CHB相关肝硬化患者。主要终点为第48周时HBV DNA检测不到(<20IU/mL)的比例。次要终点包括第48周时ALT的复常率,以及肾功能和血脂谱的变化,并进行组间比较。
【研究结果】
共纳入212例患者,TMF组104例,TAF组108例。基线特征如下:TMF组与TAF组患者的年龄分别为45(38,55)岁 vs 44(40,51)岁;HBV DNA水平分别为4.72±2.09 vs 3.92±1.27 log10 IU/mL;ALT水平分别为38.0(24.3,76.5)U/L vs 35.1(22.0,89.5)U/L;肝脏硬度值(LSM)分别为14.7(10.4,25.0)kPa vs 12.6(9.55,17.8)kPa,两组间无显著差异(P均>0.05)。
治疗48周时,TMF组HBV DNA检测不到的比例为96.2%,TAF组为96.3%(P=0.618)。TMF组ALT复常率为77.3%(34/44),TAF组为75.0%(36/48)(P=0.823)。
在肾脏安全性方面,治疗48周后,两组的eGFR[TMF vs TAF=106.5(99.1,113.4)mL/min/1.73m² vs 108.8(101.5,114.6)mL/min/1.73m²,P=0.134]和血清肌酐水平(TMF vs TAF=68.3±12.3μmol/L vs 67.8±10.4μmol/L,P=0.323)均无显著差异。此外,患者的血脂谱保持稳定,两组间无显著差异(P均>0.05)。
在安全性方面,两组在治疗期间均未发生严重不良事件,也无患者因不良事件停药。
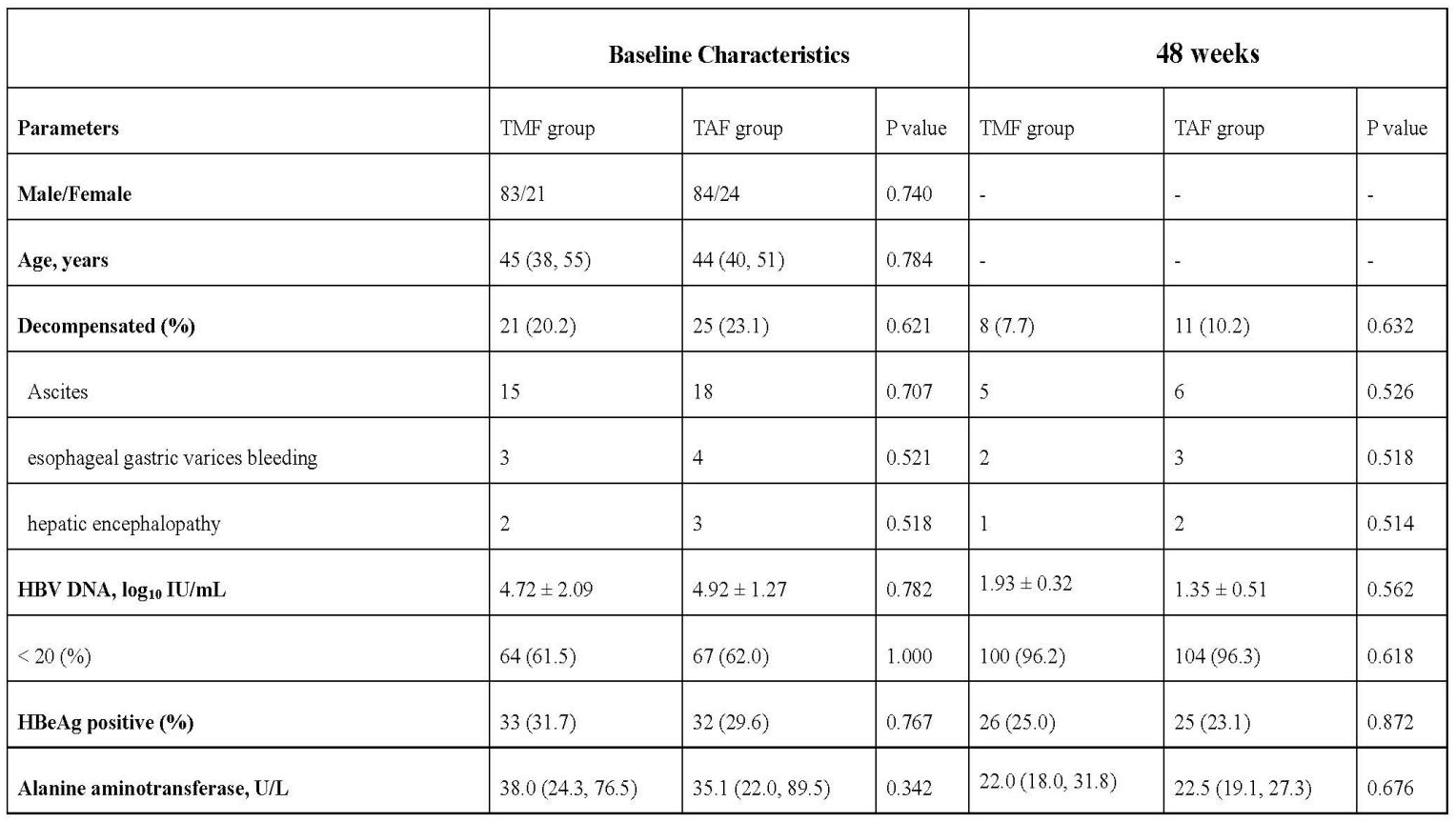
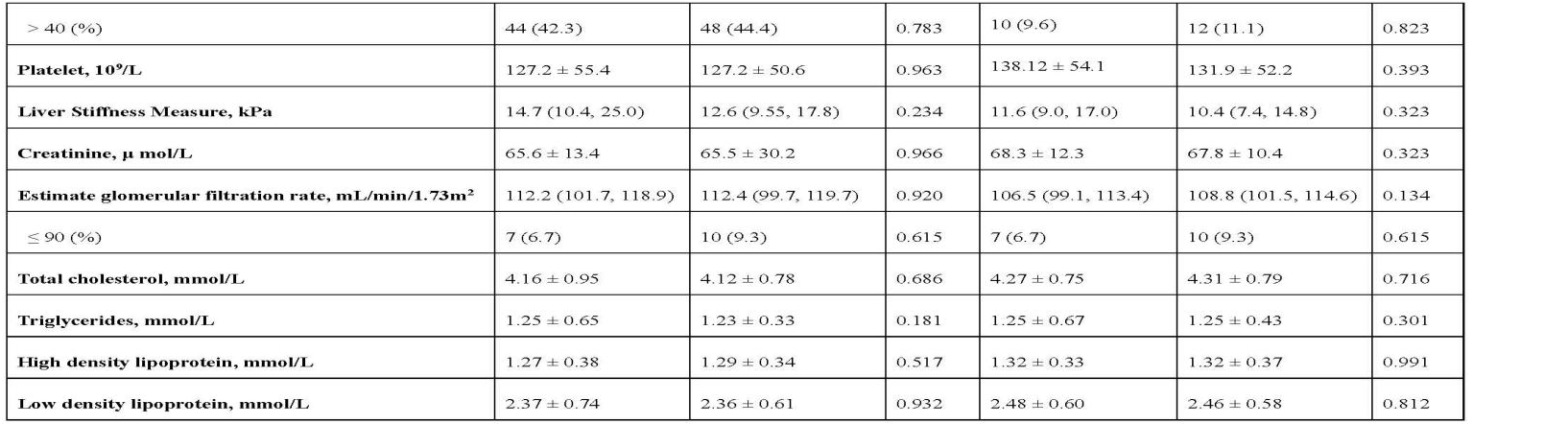
受试者基线和48周时的实验室参数
【研究结论】
在真实世界中,TMF和TAF治疗CHB相关肝硬化患者48周的疗效和安全性相似。未来需要前瞻性、长期的验证研究。
肝胆相照平台:除了上述人群,您的团队关于TMF在HBV相关肝细胞癌(HBV-HCC)人群中疗效与安全性的研究也被大会收录,这项研究又取得了哪些结果呢?
曾庆磊教授:随着TMF被纳入医保体系,其价格优势凸显,经济性良好,药物可及性也得到了显著提升。这使得许多HBV-HCC患者在抗病毒治疗方案的选择上,倾向于TMF。然而,尽管TMF在临床中的应用越发广泛,但目前在真实世界中,关于TMF治疗HBV-HCC患者的研究数据仍相对匮乏。本研究旨在评估真实世界中TMF治疗HBV-HCC患者48周的疗效和安全性。
【研究方法】
本回顾性研究纳入了2018年8月至2024年8月在郑州大学第一附属医院HCC手术后接受TMF(25mg/d)或恩替卡韦(ETV)(0.5 mg/d)抗病毒治疗的HBV-HCC患者。主要终点是第48周时HBV DNA检测不到(<20IU/mL)的比例。次要终点包括第48周时ALT的复常率,肾功能指标及血脂的变化,并进行组间比较。
【研究结果】
共纳入63例患者,TMF组29例,ETV组34例。基线特征如下:TMF组平均年龄为51.93±10.94岁,ETV组为54.91±8.35岁(P=0.225);HBV DNA水平分别为1.10±1.66 log10IU/mL和1.41±2.03 log10IU/mL(P=0.516);ALT水平分别为26.00(18.50,42.50)U/L和30.00(20.75,52.25)U/L(P=0.440)。
在治疗48周时,TMF组HBV DNA检测不到的比例为96.6%(95% CI,89.9%-100%),ETV组为94.1%(95% CI,86.2%-100%)(P=0.651)。然而,TMF组的ALT复常率显著高于ETV组[89.7%(95% CI,78.6%-100%) vs 64.7%(95% CI,48.6%-80.8%),P=0.020]。
在肾脏安全性方面,治疗48周后,两组的eGFR(TMF vs ETV=106.19±11.80 vs 104.31±8.39mL/min/1.73m²,P=0.738)和血清肌酐水平(TMF vs ETV=65.68±11.88 vs 63.82±9.65μmol/L,P=0.688)均无显著差异。
在血脂谱方面,TMF组的血清总胆固醇水平显著低于ETV组[TMF vs ETV=3.21(2.87,3.52)mmol/L vs 3.72(3.17,3.93)mmol/L,P=0.002],其他血脂参数组间无显著差异(P均>0.05)。
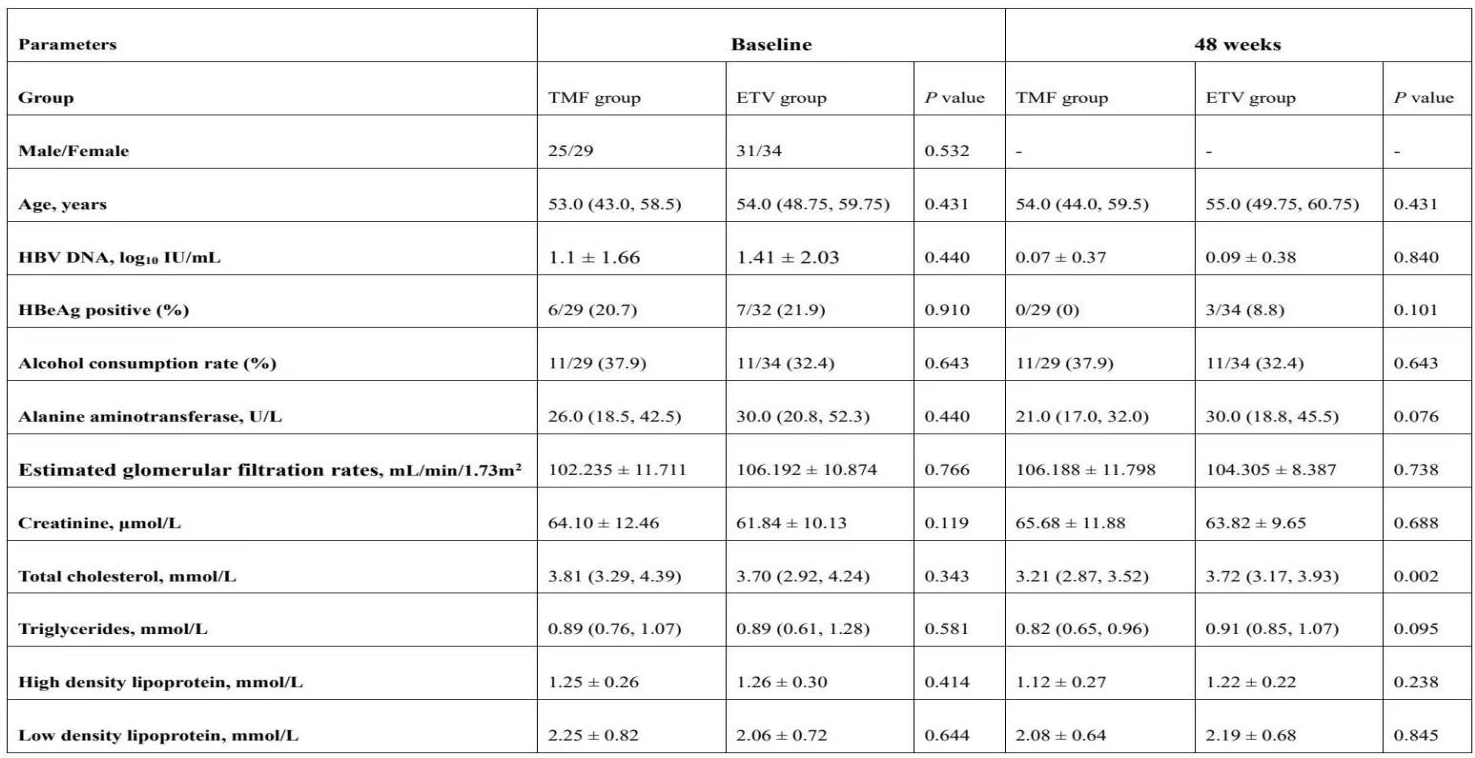
受试者基线和48周时的实验室参数
【研究结论】
本研究首次证明TMF治疗HBV-HCC患者具有良好的疗效和安全性。与ETV相比,TMF显示出显著更高的ALT复常率和更好的血脂谱,且肾脏安全性相当。未来需进一步开展大规模研究以验证上述结果。
肝胆相照平台:在您看来,上述三项研究成果有何意义?结合研究结果,您如何看待TMF在我国临床应用的前景?
曾庆磊教授:在临床试验领域,TMF 针对孕妇、乙肝肝硬化以及HBV-HCC人群的研究数据相对匮乏。我们团队开展的这几项研究,以目前国内指南推荐用于CHB治疗的其他一线抗病毒药物作为对照,系统观察了TMF在这三类特殊人群中的治疗效果与安全性。研究结果令人欣喜,TMF不仅在这三类人群中展现出良好的疗效与安全性,在ALT复常率方面甚至表现得更为出色。这些研究数据,极大地弥补了TMF临床试验在特殊人群研究方面的不足,与已有的临床试验数据相互补充,为TMF在真实临床环境中的合理应用提供了坚实可靠的依据。
正如前面所提到的,TMF作为我国自主研发的I类新药,现已被纳入医保体系。无论是前期的临床试验,还是大量的真实世界研究,都充分验证了TMF卓越的疗效与可靠的安全性。基于这些有力的证据,TMF在抗病毒治疗中占据一线地位可谓是实至名归。随着医保政策的助力以及临床实践经验的不断积累,TMF在我国临床应用中必将拥有广阔的前景,为更多患者带来有效的治疗方案和康复的希望。
*研究摘要号:SA-APASL2025-14594、16297、15984