危重哮喘相对少见,其发病率呈下降趋势;然而,它可能需要重症监护,包括机械通气。本文概述了危重哮喘的管理。
危重哮喘 (CA) 是一个涵盖不同定义的总称,所有定义均指哮喘急性发作,可迅速恶化为呼吸衰竭,通常需要重症监护治疗,可能还需要机械通气 (MV)。在本文中,我们总结了危重哮喘治疗的当前证据。
定义和发生率
哮喘是一种复杂且异质性的肺部疾病,以慢性气道炎症和可变的呼吸道症状为特征,包括由于可逆性气流阻塞和过度支气管反应性导致的喘息、气短、咳嗽和胸闷。这些症状的强度和频率各不相同,通常由空气污染、过敏原、呼吸道感染或运动等因素引发(GINA 委员会 2024)。
过去 30 年来,哮喘的发病率及其死亡率均有所下降(Cao 等人,2022 年;Ebmeier 等人,2017 年)。然而,哮喘仍然是最常见的慢性呼吸系统疾病之一,并且仍然是出院后几个月内再次入院的主要原因(Cao 等人,2022 年;Gonzalez-Barcala 等人,2018 年)。据估计,全世界有 3 亿人患有哮喘(Masoli 等人,2004 年)。2009 年,欧洲每 10 万居民平均有 53 人因哮喘入院(Bousquet 等人,2014 年)。在美国进行的一项研究中,10% 的入院哮喘作为初步诊断被转入重症监护病房 (ICU),2% 需要插管(Pendergraft 等人,2004 年)。值得注意的是,入住 ICU 的大多数患者都是女性。与标准入院的哮喘患者相比,需要入住 ICU 和/或插管的哮喘患者死亡率更高,住院时间更长(平均+1.75 天),并且更有可能再次入住医院或 ICU(Pendergraft 等,2004) 。
风险因素和合并症
哮喘的确切原因尚不清楚,但各种危险因素和基因-环境相互作用促进了其发展。哮喘风险增加还包括其他因素,如早年呼吸道感染,尤其是严重的病毒感染、特应性病症和环境因素,如吸入性过敏原、烟雾、污染和化学品接触;此外,其他因素如压力、饮食和微生物组成分(Mims 2015)。
哮喘患者,尤其是重症哮喘患者,肺部和肺外合并症的发生率较高,老年女性、前吸烟者和皮质类固醇依赖患者尤其受影响(Tomisa 等,2021)。阿尔瓦雷斯等人。(2005) 研究了与 CA 相关的危险因素(特别是近致命性哮喘和致命性哮喘)。已确定的危险因素包括吸烟、特应性、药物需求增加(雾化 β 受体激动剂、口服皮质类固醇和口服茶碱)、住院史和/或 ICU 入住史以及 MV 需求。此外,医疗保健获取机会少、药物滥用以及伴随的精神疾病也与 CA 的较高风险相关(Louie et al. 2012)。
结果
哮喘急性发作导致的住院总死亡率为 0.5-5%,其中年龄较大(>65 岁)、女性和非洲裔美国人的死亡率较高(Krishnan 等人,2006 年;Louie 等人,2012 年)。CA 的死亡率为 3% 至 10%,死亡主要因低氧血症、脑缺氧和心肺骤停 (Gonzalez-Barcala et al. 2015)。既往有近乎致命的哮喘病史可使死亡率增加 16 倍(Louie 等人,2012 年)。
关键哮喘管理
通常,在临床评估中,患者会出现呼吸急促(通常高于 30 次呼吸/分钟)、喘息、使用辅助肌和周围发绀。反常呼吸可能是呼吸即将停止的征兆。心动过速(>120 bpm)和血流动力学不稳定很常见。当患者在接受氧疗后仍出现低氧血症(SpO 2 <92%)、严重高碳酸血症、神经系统改变(如意识下降、头晕、嗜睡或脑病)、心脏紊乱、存在气压伤(气胸或纵隔气肿)或需要重症监护时,建议入院重症监护呼吸支持(Adams 等人,2012 年;Schivo 等人,2015 年)。建议进行胸部 X 光检查以发现潜在的并发症,如肺不张、气压伤、肺炎或气胸。基本监测包括通过连续血气分析进行连续气体交换、组织灌注、足够的心输出量和水电解质状态。
CA 管理的基础包括逆转支气管收缩、通过纠正低氧血症来控制症状,以及预防病情恶化和降低死亡风险。初始治疗包括氧疗、支气管扩张剂、全身抗炎药和呼吸支持。CA 管理的概述如图 1所示。
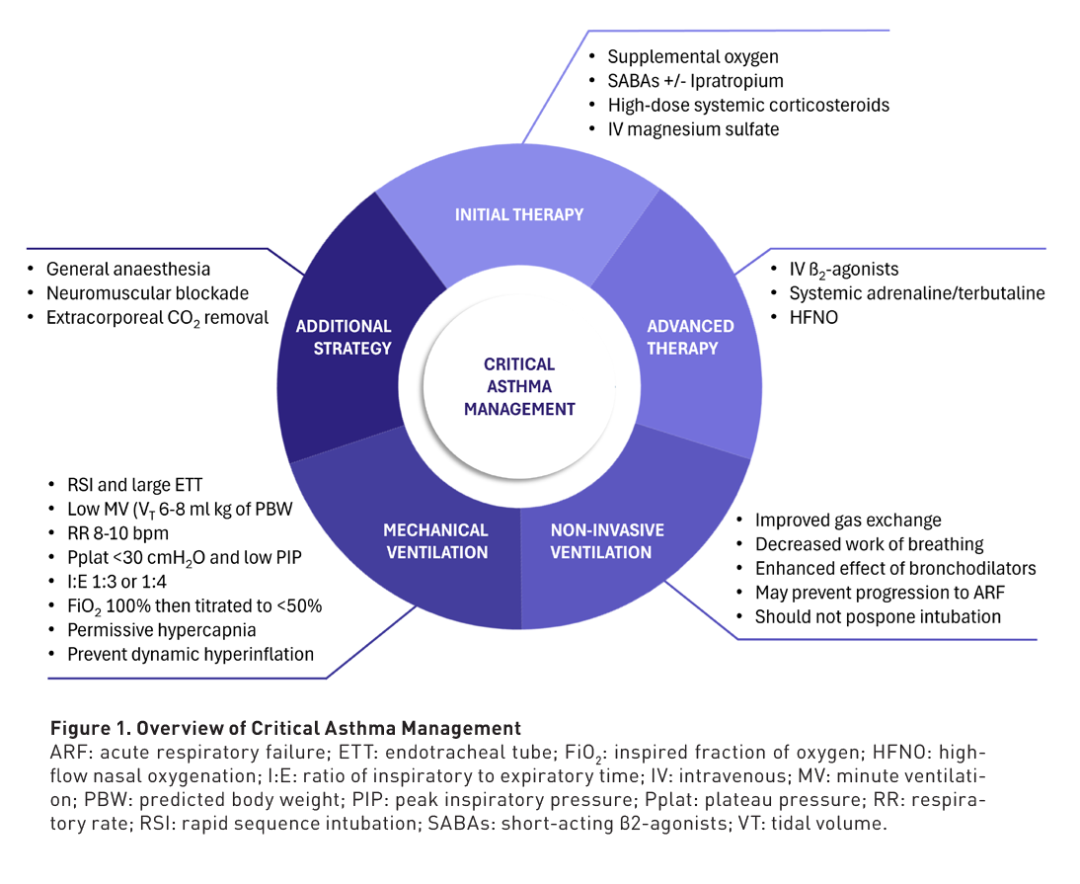
哮喘和酸碱平衡紊乱
CA 的特点是气道阻塞、高碳酸血症和呼吸性酸中毒,这些发现与插管的需要和较高的死亡率相关 (Vasileiadis et al. 2019)。此外,CA还可因低氧血症和组织灌注不足、心功能障碍和呼吸肌疲劳而导致乳酸性酸中毒。使用大剂量支气管扩张剂治疗还可能导致乳酸性酸中毒、低钾血症和低磷血症,这会进一步恶化肌肉疲劳和组织氧合,使临床结果复杂化(Vasileiadis et al. 2019)。
病理生理学和肺力学
传统上,哮喘主要被认为是气道炎症的一种病症。肺力学可能会受到气道过度狭窄的影响,气道直径的减小会导致气道阻力的大幅增加。这种阻力的增加会导致各种肺功能损伤,包括呼气流量受限、呼气时间延长、空气滞留和固有呼气末正压 (PEEP)、动态过度充气、通气不均匀、通气/灌注不匹配以及呼吸功增加。卡明斯基和查普曼 2020;斯卡拉 2010)。对气道狭窄的传统理解涉及两种主要机制:支气管收缩(由气道平滑肌激活引起)和管腔狭窄(由水肿、炎症浸润和粘液分泌过多导致气道壁增厚引起)。除了哮喘发作期间最明显的气道狭窄之外,在慢性哮喘中,组织重塑引起的结构变化也会影响呼吸顺应性(Mims 2015)。
在这种情况下,CA 经常表现为前面描述的最严重的改变形式。由增厚的壁和炎症浸润导致的气道狭窄可能比正常情况大 300% (James 2020),并伴有显着的平滑肌肥大和过多的粘液产生,这可能导致气道阻塞。肺过度充气和严重的通气/灌注不匹配是氧合受损和低氧血症的主要原因。一方面是由于区域通风不良,另一方面是由于急性炎症后毛细血管渗漏导致灌注改变(Louie et al. 2012)。当一秒用力呼气量 (FEV 1 ) 低于预测值的 30% (McFadden Jr 和 Hejal 1995) 且死腔增加时 (Louie et al. 2012),就会发生初期高碳酸血症。
药物治疗
吸入短效 β2激动剂(SABA) 仍然是急性哮喘的主要治疗方法,建议使用沙丁胺醇连续或间歇给药用于支气管扩张。高剂量沙丁胺醇与低剂量沙丁胺醇相比并没有显示出额外的益处。当对沙丁胺醇的反应不足时,福莫特罗和异丙肾上腺素等完全激动剂可能有用,尽管它们产生心血管副作用的风险较高。吸入异丙托铵和噻托溴铵是短效毒蕈碱拮抗剂,与 SABA 联合使用可增强支气管扩张作用。它们通过放松气道平滑肌和缓解气道狭窄来发挥作用。全身性皮质类固醇对于通过减少气道炎症、减少病情复发和最大限度地减少长期气道重塑来预防致命性哮喘至关重要(Rowe et al. 2001)。高剂量的皮质类固醇已被证明可以显着改善肺功能,并通过降低气道敏感性来增强 SABA 的有效性。对于 CA 病例,应在治疗早期给予甲基泼尼松龙,开始时每 6 小时 60 至 80 mg,然后随着患者病情改善逐渐减量 (McFadden 2003)。硫酸镁抑制钙通道并阻断副交感神经张力。静脉给药(20 分钟输注 2 g)作为其他支气管扩张剂治疗的辅助疗法已被证明可以改善肺功能并减少再入院率(GINA 委员会 2024 年;Kew 等人 2014 年);然而,尚未证明它可以降低死亡率(Irazuzta 和 Chiriboga 2017)。
CA 的高级支气管扩张剂治疗包括全身性 β2受体激动剂,主要是静脉注射沙丁胺醇,特别是当使用 SABA 不可行时。当患者对吸入治疗无反应时,也可以使用胃肠外肾上腺素和特布他林(皮下或静脉注射)。然而,它们缺乏强有力的证据,并可能产生潜在的副作用(心动过速、快速心律失常、心肌损伤和酸碱紊乱)(GINA 委员会 2024)。因此,目前的建议保留其用于无法使用吸入支气管扩张剂的 CA 患者。
氧疗
低氧血症是由气道狭窄或阻塞以及通气/灌注不匹配引起的。补充氧气是急性哮喘治疗的标准。CA 氧疗的目标是将 SpO 2维持在 92% 以上(GINA 委员会 2024)。30% 至 50% 的吸入氧分数通常足以纠正缺氧;应避免较高分数,因为高氧可能有害,并且已被证明会增加气道反应性(Kallet 和 Matthay 2013;Rodriguez-Roisin 等人 1989)。氧气通常通过鼻插管输送,有时也通过面罩输送。如果尽管补充氧气,缺氧仍然存在,则应考虑肺炎或气胸等并发症(Schivo et al. 2015)。
无创呼吸支持
无创呼吸支持改变了呼吸衰竭的治疗方法,自推出以来已被广泛采用。虽然其在慢性阻塞性肺疾病恶化和急性心源性肺水肿中的疗效已得到证实,但在急性哮喘中使用无创支持仍然存在争议(Osadnik 等人,2017 年;Vital 等人,2013 年)。
高频一氧化氮
高流量鼻氧合 (HFNO) 已成为治疗 CA 的一个有前途的选择,尽管支持其用于严重哮喘的证据仍然有限。在 Geng 等人的一项研究中。(2020),与接受标准氧疗的患者相比,接受 HFNO 的患者心率和呼吸频率有所降低,但没有发现额外的临床益处。
无创通气
双水平无创通气 (NIV) 作为一种无创策略在 CA 中被广泛采用,尽管其功效数据仅限于少数研究,并且对死亡率和预防插管的益处并不一致(Gupta 等人,2010 年;Lim 等人)索罗斯基等人,2003 年;
对于精心挑选的 CA 患者来说,它可能是一种有益的干预措施,可以减轻与侵入性 MV 相关的风险。事实上,NIV 已被证明可以改善肺功能和气体交换、降低呼吸频率、减少肌肉疲劳以及与气道阻塞和肺过度充气相关的呼吸功,最终可以防止进展为呼吸衰竭(Brandao 等人,2009 年;古普塔等,2010;林等,2003)。它还被证明可以增强吸入支气管扩张剂的有效性,可能是通过促进药物在整个气道中更均匀的分布(Brandao 等人,2009 年;Pollack 等人,1995 年)。它还被证明可以缩短住院时间,但有关其降低死亡率作用的证据仍然很少(Manglani 等人,2021)。事实上,欧洲呼吸学会/美国胸科学会关于急性呼吸衰竭的指南无法推荐使用非侵入性支持,因为没有数据显示与标准护理相比,结果具有临床相关差异(Rochwerg et al. 2017) 。
无创呼吸支持失败(定义为插管的需要)多年来一直在减少,年轻患者更有可能失败 NIV 并需要 MV(Ganesh 等,2015)。在 Manglani 等人的一项回顾性研究中。(2021),NIV 失败与基线哮喘严重程度、体重指数和吸烟史无关;此外,使用 NIV 并不会增加气压伤等并发症。
尽管无创呼吸支持似乎是精心挑选的 CA 患者的安全选择,但无创设备的升级不应延迟插管,因为 MV 启动的延迟与更差的结果相关(Lim 等,2012)。研究表明,当 NIV 开始后 1-2 小时内呼吸频率、呼吸努力和高碳酸血症恶化时,应立即开始 MV。NIV 的禁忌症包括恶心、呕吐、意识水平改变、血流动力学不稳定以及呼吸窘迫或即将发生的呼吸骤停(Schivo 等,2015)。呼吸支持的强度应根据呼吸功和低氧血症/高碳酸血症的改善情况进行调整。
有创呼吸支持
机械通气
哮喘急性发作时插管和启动 MV 取决于临床决策,因为对于插管指征尚未达成共识(Brenner 等,2009)。当患者对药物治疗和无创呼吸支持没有反应,并出现肌肉即将衰竭、精神状态改变、高碳酸血症恶化、严重呼吸性酸中毒和补充氧合难治性低氧血症时,应开始MV(Gayen et al. 2024;Talbot)等2024)。此外,插管的决定必须权衡与 MV 相关的潜在风险。事实上,MV 需要仔细处理,因为它可能导致气压伤、气胸和纵隔气肿等并发症。它可以恶化动态过度充气并延长炎症反应,并增加感染风险(Blanch 等人,1991 年;Zimmerman 等人,1993 年)。此外,胸腔内压力增加可能导致新的或恶化的血液动力学不稳定以及死腔增加。MV 的目标包括维持足够的氧合、缓解呼吸困难、减少动态过度充气、避免气压伤和预防严重酸血症(Oddo 等,2006)。
CA 患者的气管插管可能具有挑战性,应尽可能选择性地进行。哮喘患者插管后更有可能出现喉痉挛、支气管痉挛加重、血流动力学不稳定和肺误吸(Brenner et al. 2009)。低血压很常见,尤其是由于无意识损失而导致低血容量的患者(Garner et al. 2022)。通常建议快速顺序插管,并应避免气囊通气,因为它可能导致过度充气和气压伤(Brenner 等人,2009 年;Garner 等人,2022 年)。气管插管应比标准尺寸大 0.5-1 倍,以减少气道阻力并促进支气管抽吸和支气管镜检查(Adams 等人,2012 年;Burburan 等人,2007 年)。
可能需要采用深度镇静和神经肌肉阻滞进行全身麻醉,以提高患者与呼吸机的同步性并降低代谢需求,例如对于呼吸驱动力较高的患者(Burburan 等人,2007 年;Louie 等人,2012 年)。事实上,CA 患者很容易出现不同步,因为当内在 PEEP 需要更大的努力来触发呼吸机时,触发无效(Demoule et al. 2020)。此外,一些麻醉剂,如异丙酚和氯胺酮,可以减轻支气管痉挛。
呼吸机设置应以优化哮喘的病理生理学和肺力学改变为目标。最佳通气模式尚未建立,应适应每个患者,以保证患者与呼吸机的同步。辅助通气和控制通气模式都可以在 CA 的早期阶段使用,并且没有特定模式被证明更优越(Demoule et al. 2020)。建议采用低分钟通气量策略,通过低潮气量(每公斤预计体重 6-8 毫升)和低呼吸频率(8-10 次呼吸/分钟)来避免高峰压和平台压(Pplat 低于 30 cmH)2 O),结合延长呼气时间(I:E 为 1:3 或 1:4)以促进呼气并防止空气滞留(Brenner 等人,2009 年;Leatherman 2015 年)。低 PEEP 水平应设置为低于 5 cmH 2 O,并连续测量自动 PEEP。SpO 2应保持在 92% 以上,避免高氧,最初将吸入氧分数 (FiO 2 ) 设置为 100%,然后滴定至 50% 以下 (Leatherman 2015)。如果几小时后需要更高的 FiO 2,则应调查肺炎、肺水肿和栓塞等并发症(Kallet 和 Matthay 2013)。允许性高碳酸血症通常是可以耐受的。事实上,需要强调的是,正确的气体交换并不是 MV 早期阶段的首要任务;相反,将 pH 值维持在 7.25-7.30 之间就足够了(Darioli 和 Perret 1984),同时更加关注预防恶性通货膨胀引起的并发症。事实上,当患者由于呼气流量减少和呼气努力增加而无法在一次呼吸和另一次呼吸之间完全呼气时,就会发生动态过度充气。过度充气会导致过度扩张和 Pplat(吸气末气道压力)升高,从而带来气压伤、气胸、纵隔气肿和心血管衰竭的风险。因此,必须通过测量 Pplat 定期对其进行评估(Demoule et al. 2020);Pplat 的 30 cmH 2 O截止值被认为是安全的。
附加策略
尽管具有最佳 MV,但对常规治疗仍难治的 CA 患者,肺功能下降、持续性支气管痉挛和动态过度充气且内源性 PEEP 较高、气体交换恶化和严重酸中毒,可能需要接受其他治疗,包括体外 CO 2去除。
体外 CO 2去除被认为是一种挽救生命的干预措施,并且在最严重的 CA 病例中显示出益处,特别是对于 pH <7.2、严重动态过度充气和血流动力学受损的患者(Patel 等人,2020 年;Tajimi 等人,2020 年)。1988)。在接受体外 CO 2去除治疗的 24 名 CA 患者队列中,与难治性 CA 患者相比,生存率显着提高(Mikkelsen 等,2009)。然而,使用体外循环会增加风险,包括败血症、血栓形成、出血和器官衰竭,并且并非在所有中心都可行。
ICU Management & Practice, Volume 24 - Issue 5, 2024