
摘要:机械通气对于危重患者至关重要,它与自然呼吸形成鲜明对比,主要是由于胸膜压 ( P pleural ) 的差异。自然吸气会降低P pleural,将肺部拉离胸壁,而正压吸气则会增加P pleural,将肺部推向胸壁。这种转变有几个后果。首先,正压通气期间胸膜P升高可导致循环气道关闭,特别是在依赖性肺区域。这会增加肺不张的风险,从而损害氧合并可能导致肺炎等进一步的并发症。其次,胸膜P的增加破坏了胸膜负P和毛细血管力维持的平衡。这种破坏减少了胸膜之间的润滑性胸膜液,增加了肺组织的摩擦和剪切应力,这可能导致呼吸机引起的肺损伤和气胸等损伤和病症。此外,气道关闭会恶化肺顺应性,使机械通气更具挑战性并增加肺过度拉伸的风险。这就需要仔细管理通气设置,特别是使用呼气末正压 (PEEP) 和肺复张操作,以尽量减少这些不利影响。保护策略,例如使机械通气与患者的呼吸努力同步、俯卧位以及仔细应用 PEEP,对于降低胸膜肺气肿及其相关风险至关重要。由于负压通气 (NPV) 本质上会降低胸膜压,因此它可能有助于避免前面讨论的许多不良副作用。因此,在现代背景下重新考虑和重新引入净现值值得认真探索。
关键词: 机械通气; 胸膜压; 气胸; 呼吸机引起的肺损伤(VILI)
介绍
为了更好地了解机械通气的不利影响,有必要首先检查机械通气和自然呼吸之间的差异。 Loring ( 1 ),以及最近的 Butler等人。 ( 2 ) 认为负压通气 (NPV) 与正压通气 (PPV) 之间没有显着差异,负压通气通过向外拉胸壁来模拟自然吸气。当跨肺压相等时,两种模式确实产生相同的肺容量。然而,气道正压会增加胸膜压 ( P pleural ),而胸外负压和自然吸气会降低胸膜压。P胸膜起着至关重要的作用,可以将肺推向胸壁(正P胸膜)或将其拉开(负P胸膜)。因此,预计 PPV 的副作用将与P胸膜行为的这些差异密切相关。
呼吸系统的结构
在关于人工通气期间气胸发生和并发症的讨论中,我们强调胸膜内压力的关键作用。
在图1中,呼吸系统可以被解释为两个气球的组合:由胸壁和隔膜(气球2)包围的肺(气球1)。肺周围是胸膜,脏层(肺)胸膜作为肺的外盾/壁,在肺门处向后弯曲作为壁(肋)胸膜,跟随并附着在胸壁和与纵隔背面接壤的膈肌上至肺门。脏层胸膜和壁层胸膜之间的胸膜腔体积较小,充满润滑液。胸膜内压力(也简称为“胸膜压力”,P pleural)是胸腔内压力的特征。测量胸膜P 的侵入性最小的方法是通过食道中的球囊压力传感器。正常情况下,P胸膜是低于大气压的:在呼气末状态下,当所有呼吸肌都放松时,胸廓往往会扩张到更大的体积,但肺部会自然回缩,导致约-7 cmH 2 O的负压。此时,肺容量等于功能残气量(FRC)。负压胸膜将两个胸膜拉开,并与润滑剂结合,有利于呼吸过程中的平滑运动。
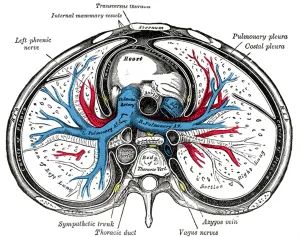
图 1胸部横切面,显示胸壁、胸膜腔、肺和纵隔。内部“气球”肺,由脏肺胸膜包围,被壁层肋胸膜包围,附着于胸壁,即外部“气球”。胸膜之间的空间,胸膜腔体积很小,充满润滑剂,有利于胸膜的相互运动。胸膜腔内的压力通常低于大气压,是胸腔压力的特征,并与肺泡压一起决定跨肺压。在平衡状态下,在没有气道关闭的情况下,肺泡压力等于气道压力(改编自 Henry Gray,人体解剖学,1918,https://archive.org/details/anatomyof humanbo1918gray/)。
然而, P胸膜并不统一。由于肺的重量,重力从上到下产生压力梯度。肺具有高度的灵活性,就像液体一样向各个方向传递压力并承受上方肺组织的重量。这导致梯度与肺高度和充满空气的肺的比重的乘积成正比,通常约为 7 cmH 2 O,个体差异取决于身体长度、总肺活量等因素(并且,如果存在) ,水肿!)。
肺部被胸膜液包围
卡夏等人。 ( 3 ) 描述负P胸膜力和毛细血管力之间的平衡如何使肺部(在 FRC 水平上比重约为 0.3 g/cm 3)被一层薄薄的更致密的胸膜液(具有特定的重量)包围。重量为1g/cm 3 )。
该流体层既充当润滑剂又充当隔离物。根据Casha的计算,这一层的厚度约为20至200微米,足以防止胸膜(3、4 )上众多长度不足5微米的微绒毛在呼吸周期过程中相互损坏。动作。负P胸膜对于维持毛细血管力的平衡至关重要。正压会导致胸膜之间的胸膜液被清除,导致肺部“漂浮”在较稠密的胸膜液上。因此,阳性P胸膜可能会损害微绒毛以及胸膜本身。
自然呼吸和机械通气期间P胸膜的行为
在本次讨论中,P pleural是指平均P pleural,即肺高度的平均值。
肺和胸壁都可以建模为气球,遵循线性压力-体积 (PV) 关系,其中体积与跨壁压力 ( P trans ) 成正比。P trans定义为气球内部的压力减去气球外部的压力。对于肺,这表示为气道压力 ( P气道) 减去P胸膜,对于胸壁,表示为P胸膜减去外部压力 ( P外部)。鉴于胸膜腔的体积可以忽略不计,胸腔和肺的体积可以被认为是相等的(假设没有气胸或其他漏气)。对于 FRC 中的非通气人员,适用以下条件(C = 顺应性,V = 容量):
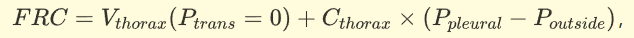

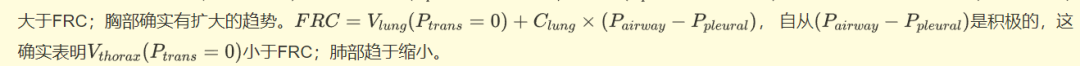
�右�=��小时哦�一个�(磷��一个��=0)+��小时哦�一个�×(磷�我�你�一个我-磷哦你��我��)
从 FRC 开始,吸气需要增加跨肺压,这可以通过减少胸膜P或增加气道P来实现。在自然呼吸期间,随着呼吸肌扩张胸腔,将空气吸入肺部,胸膜P减少。 NPV 通过降低胸部(使用胸甲)或整个身体(使用铁肺)的外部压力来模仿这一过程。或者,PPV 通过抬高P气道来增加肺容量。然而,随着肺容量的增加,胸廓容量也必须增加,从而提高胸壁的跨壁压力。由于PPV 期间外部P保持恒定,因此P胸膜上升(变得不那么负甚至正)。这是自然吸气(或使用周围负压吸气)和 PPV 之间的主要区别:P胸膜向相反方向变化。
除了对胸膜液层的影响之外,高P胸膜的一个重要后果是,当肺容量变化时,胸膜会经历更多的摩擦和剪切应力,特别是当P胸膜为正时,胸膜会被压在一起。因此,气胸的可能性可能受到胸膜压和肺运动程度(即潮气量)的影响。
在肺顺应性降低的情况下,必须增加驱动压力以达到相同的潮气量。然而,如果胸壁顺应性保持不变,则跨胸压和P胸膜压也将保持不变,只有跨肺压增加。额外的驱动压力完全用于补偿肺顺应性的降低。
为了优化急性呼吸窘迫综合征 (ARDS) 患者机械通气期间的呼气末正压 (PEEP),研究人员测量了P胸膜,以考虑实际的个体肺和胸壁顺应性。与理论预测相反,测量的胸膜P值通常呈阳性且显着升高。这种差异可能是由肺顺应性降低以外的因素引起的。在这种情况下,只有一部分肺参与通气,其他部分塌陷或充满水肿,这种情况通常被称为“婴儿肺”。尽管如此,气道驱动压力必须远高于测量的胸膜压力,因为即使气流为零,跨肺压也必须克服肺弹性。高P胸膜与胸腔和肺容量增加相关,增加了通气肺泡过度拉伸的风险。因此,限制潮气量对于最大限度地降低这种风险至关重要。
肺不张和气道闭合
1963 年,本迪克森等人。 ( 5 ) 证明机械通气全身麻醉会导致术前肺功能正常的患者术中氧合和依从性恶化。布里斯玛等人。 ( 6 )表明这些恶化与肺组织密度有关,可通过计算机断层扫描检测到。肺不张会直接损害氧合,并可能导致进一步的肺部损伤,例如肺炎。肺不张的发生与周围气道关闭密切相关 ( 7 , 8 )。
周围气道闭合 ( 9 , 10 ) 是肺部的一个重要特性,可以防止肺泡塌陷。气道在比肺泡塌陷更高的跨壁压力下关闭。这意味着当局部跨肺泡压力较低时,肺泡已达到其最小体积,但仍含有空气。当所有气道关闭时,肺内剩余的空气量称为残余容量(RC)。
随着局部跨肺压降低,气道关闭的过程在 PV 关系的下部拐点曲线中很明显:在深呼气期间,顺应性逐渐降低。在PV关系的线性部分,当所有肺泡都参与通气时,顺应性最大并且等于PV曲线的直线部分的斜率。随着更多的肺泡关闭,顺应性降低,当所有喂养气道都关闭时,顺应性在 RC 处达到零。
当跨肺压下降时,气道就会关闭,这在肥胖患者中很常见(11)。在仰卧位时,腹部对隔膜的压力往往会增加胸膜压力并减少肺容量。该压力可能非常高,以至于观察到肺部完全闭合,从而阻止任何气流进入肺部,除非P气道超过气道开放压力。解决这个问题的标准程序包括将患者置于反特伦德伦伯卧位并应用 PEEP。
机械通气和气道闭合之间的相互作用
机械通气期间气道闭合所起的作用尚未完全了解。 Hedenstierna ( 12 ) 表明,手术室中 50% 的标准患者会在 FRC 水平以上经历气道闭合,而 Dollfuss ( 8 ) 的实验表明,在深呼气时,气道闭合开始于 FRC 以下。 Hedenstierna 的研究小组 ( 6 ) 还表明,PEEP 可以防止气道闭合,并强调 ( 13 ) 高氧含量导致吸收性肺不张的风险。 Milic-Emili ( 9 ) 解释说,PV 关系所包围的表面积是气道闭合的衡量标准。
最近的文献提供了气道闭合的临床影响的两个例子。 Ventinova Evone ( 14 ) 呼吸机记录的 PV 曲线特别窄,可能是由于吸气和呼气期间气流受到控制,这有助于防止气道关闭。类似地,流量控制呼气 (FLEX) 技术 ( 15 ) 通过调节呼气流量来改善通气/灌注比。
PPV 还可导致周围气道的循环关闭和重新开放。吸入的空气首先会使近端肺泡膨胀。肺/胸腔体积的增加使整个肺的胸膜压力升高。一些依赖气道将因跨肺泡压力降低而关闭,但在吸气流停止后,空气从近端肺泡重新分配到远端肺泡时重新打开。众所周知,气道的周期性关闭和开放会导致呼吸机引起的肺损伤(VILI)。
VILI、ARDS、气胸和机械通气
正压机械通气用于治疗急症患者已有数十年历史。虽然临床医生认识到其挽救生命的潜力,但追溯到 20 世纪 60 年代和 70 年代的研究强调了它的一些潜在缺点和并发症。 Pingleton 的一篇最新评论 ( 16 ) 详细讨论了这些并发症。多年来,VILI 一直是临床气压伤的代名词。 1979 年,约翰逊等人。 ( 17 ) 报告称,放射线检测是接受 PEEP 治疗严重呼吸衰竭的患者潜在进一步并发症的关键指标。在 17 名出现间质气体的患者中,9 名进一步发展为气压伤、纵隔气肿、气胸和胸外夹层。在放射学上,间质气体表现为囊泡稀疏(囊性变化)、沿支气管和血管的线性条纹、血管周围的气体晕以及胸膜下气体。 1944 年,Macklin 和 Macklin ( 18 ) 提出了自发性气胸的类似机制,表明其发生之前通常会出现间质性肺气肿。慢性阻塞性肺病 (COPD) 患者的实质囊性空腔损伤和炎症变化是众所周知的气胸风险增加的原因。皮丘罗夫等人。 ( 19 )调查了82例气胸患者,其中14例为COPD患者,证实所有患者均表现为间质性肺气肿。
Amato ( 20 ) 和 Miller ( 21 ) 证明,平均气道压力和峰值气道压力的降低以及潮气量的限制可导致气胸数量和人工通气相关死亡率的显着减少。他们提出的肺保护策略(LPS)已被全世界接受。
在新冠病毒大流行期间,据观察,气胸和其他漏气的发生率异常高 ( 22 , 23 )。然而,NPV 期间很少出现气胸(24)。这进一步支持了通气正压是气胸发生的关键因素的观点,“无创”BiPAP 通气期间气胸的发生证实了这一点 ( 25 , 26 )。
对此的一个合理的解释在于两个胸膜叶片之间的摩擦力以及 PPV 过程中两个叶片压在一起的力引起的实质剪切应力。在自然呼吸中,或在负压通气(如铁肺)中,整个呼吸周期中两个胸膜叶片之间保持负压。肺部的弹性不断地将脏层胸膜拉离壁层胸膜。此外,负P胸膜与毛细管力配合,有助于在肺部周围维持一层薄薄的胸膜液。这种胸膜液起到润滑剂的作用,在体积变化期间有效吸收并促进胸膜的相互运动。
然而,在 PPV 期间,尤其是 ARDS 患者,P胸膜被证明非常高且呈阳性 ( 27 - 29 )。这种增加的压力以相当大的力迫使胸膜聚集在一起,使它们的运动复杂化并导致摩擦和剪切应力。这种剪切应力会损伤肺实质,通常导致间质性肺气肿,这已被证明先于气胸 ( 17 , 30 )。实质对脏层胸膜失去支撑会导致气胸的发生。
PPV 经P胸膜的副作用总结
自然呼吸和 PPV 之间的主要区别在于P胸膜的行为。
-
气道正压通气增加胸膜压力。
-
PPV 期间胸膜P升高可导致气道部分、重复和循环闭合。
-
P胸膜呈阳性会导致肺部被推向胸壁,而在自然呼吸期间,当P胸膜在整个周期中呈阴性时,肺部会被拉离胸壁。
-
当肺容量变化时,正P胸膜会增加两个胸膜之间的摩擦,导致实质上的剪切应力和损伤。
-
正P胸膜破坏了负P胸膜与维持肺部周围胸膜液润滑层的毛细血管力之间的平衡。这种破坏减少了胸膜之间的距离,增加了附着在胸膜上的微绒毛受损的风险。
因此,任何限制P胸膜的措施都可以帮助减轻 VILI 的影响。实际措施包括允许并同步患者的努力、膈神经刺激和俯卧位以及应用 PEEP 和肺复张操作。
结论
PPV 虽然在重症监护环境中可以挽救生命,但也带来了一些挑战和风险,主要是由于其对P胸膜的影响。与自然呼吸不同的是,自然呼吸在整个呼吸周期中P胸膜始终为负值,PPV 会升高P胸膜,从而导致一些潜在的并发症。
-
P胸膜和肺力学:气道正压引起的P胸膜升高导致肺被推向胸壁,这与自然负压呼吸期间肺被拉开形成对比。这种变化增加了胸膜之间的摩擦,导致剪切应力和对肺实质的潜在损伤。
-
气道关闭和肺不张:胸膜阳性可导致循环气道关闭,特别是在肺部的依赖区域,导致肺不张。这种气道关闭不仅会损害氧合,还会导致随后的肺损伤,包括肺炎的风险。
-
对胸膜液动力学的影响:向正P胸膜的转变破坏了负P胸膜和毛细血管力维持的微妙平衡,这种平衡通常在肺部周围保持一层薄薄的胸膜液润滑层。这种破坏会降低胸膜液作为间隔物和润滑剂的有效性,增加胸膜微绒毛受损的可能性。
-
临床意义和保护策略:与 PPV 相关的 VILI 风险增加凸显了尽量减少P胸膜的策略的重要性。这些策略包括与患者的努力同步、俯卧位以及仔细使用 PEEP 和肺复张操作。这些方法旨在限制胸膜P升高的有害影响并改善患者预后。
总之,了解自然呼吸和 PPV 之间P胸膜行为的差异对于管理和减轻与机械通气相关的不利影响至关重要。通过采用肺保护策略,临床医生可以减少气胸、肺不张和 VILI 等并发症的发生率,最终改善危重情况下的患者护理。由于 NPV 本质上会降低胸膜压,因此可能有助于避免之前讨论的许多不良副作用。因此,在现代背景下重新考虑和重新引入净现值值得认真探索。