摘要:目的探讨血管超声在单侧大脑中动脉(MCA)闭塞行颞浅动脉-大脑中动脉(STA-MCA)血管旁路移植术后的脑血流动力学动态评估中的应用。方法回顾性连续纳入苏州大学附属第一医院神经外科经DSA确诊为单侧MCA闭塞且行STA-MCA血管旁路移植术患者109例。入院24h内完成患者临床资料收集,包括年龄、性别、体质量指数和卒中高危因素(包括高血压病、高脂血症、糖尿病、吸烟和饮酒史、心房颤动)、临床表现[近6个月内;非特异性症状(头晕、记忆力减退、反应迟钝等)、短暂性脑缺血发作、卒中]、血生化指标(低密度脂蛋白胆固醇、高密度脂蛋白胆固醇、三酰甘油、总胆固醇、空腹血糖、超敏C反应蛋白)、入院时美国国立卫生研究院卒中量表(NIHSS)评分。运用彩色多普勒超声(CDU)和经颅彩色多普勒超声(TCCD)在患者术前及术后不同时间段(术后4~7d及术后1、3、6、12个月)评估STA的血流动力学参数,分析桥血管的血流通畅性以及颅内血流动力学改变,并对术后12个月CDU和DSA检查桥血管通畅情况的结果行一致性检验。根据术后12个月DSA检查结果将患者分为桥血管通畅组和非通畅组(狭窄或闭塞),比较两组各时间段STA主干即桥血管颅外段、入颅段和颅内段内径(D)及血流动力学参数包括收缩期峰值流速(PSV)、舒张期末流速(EDV)、阻力指数(RI)、搏动指数(PI)、时间平均流速(TAMV)和时间峰值流速(TAPV)并计算STA主干时间平均流量(TAMV flow)、时间平均峰值流量(TAPV flow)。于术前1~3d及术后12、18个月分别行头部CT、主动脉弓上CT血管成像及全脑CT灌注(CTP)检查以观察患者脑灌注改变情况,术后1~2d行头部CT观察术区有无新发出血及缺血灶。分别比较桥血管通畅组和非通畅组术后12、18个月与术前1~3d的CTP参数,以及两组之间CTP参数的差异。术后12、18个月门诊复诊时,采用改良Rankin量表(mRS)评估患者神经功能预后情况,其中mRS评分≤2分为预后良好,mRS评分≥3分为预后不良。记录患者术后7d及12、18个月NIHSS评分。结果(1)CDU和DSA一致性分析:术后12个月,两者评估桥血管通畅的一致性极佳,Kappa值为0.94(95% CI:0.81 ~ 1.00,P<0.01); DSA诊断桥血管通畅组101例(92.7%),狭窄组为8例(7.3%;未发现桥血管闭塞),桥血管出现狭窄的部位均位于入颅段。(2)血流动力学参数:与术前比较,术后4~7d及术后1、3、6、12个月桥血管通畅组颅外段的D增粗(Waldχ2=30.438),血流动力学参数包括血流速度(PSV、EDV、TAMV和TAPV;Waldχ2值分别为12.117、29.310、31.075和17.525)、血流量(TAMV flow和TAPV flow;Waldχ2值分别为54.503、34.986)均增加,而RI、PI均降低(Waldχ2值分别为112.568、103.629),差异均有统计学意义(均P<0.05);但狭窄组术后12个月D及血流动力学参数与术前比较,差异均无统计学意义(均P>0.05)。与术后4~7d相比较,术后12个月狭窄组入颅段PSV[252.0(206.8,315.3)cm/s比102.5 (84.0,119.0)cm/s]、EDV[119.5(106.3, 159.8)cm/s比43.5(36.8,52.0)cm/s]均明显升高,差异均有统计学意义(均P<0.05),但RI和PI差异无统计学意义(均P>0.05)。与术后4~7d相比较,术后12个月狭窄组STA颅内段血流参数包括PSV[29.4(24.8, 41.4)cm/s比111.5 (63.3,120.0)cm/s]、EDV[19.7(15.2, 22.2)cm/s比58.5(28.3,70.0)cm/s]和PI[0.55(0.42,0.63)比0.83(0.61, 0.90)]均明显降低(均P<0.05)。(3)CTP参数:术后1~2d头部CT显示,手术区未见新发出血及缺血灶。与术前相比,术后12、18个月桥血管通畅组的CTP参数相对脑血流量(rCBF)均升高,而相对脑血容量(rCBV)、相对达峰时间(rTTP)和相对平均通过时间(rMTT)均下降,差异均有统计学意义(均P<0.05);而与术前相比,术后12、18个月桥血管狭窄组rCBF均升高,rMTT均降低,差异均有统计学意义(均P<0.05),但rCBV、rTTP与术前相比差异均无统计学意义(均P>0.05)。术后12、18个月通畅组rTTP低于狭窄组[术后12个月:1.14(1.06,1.15)比1.20(1.14,1.28), P=0.024;术后18个月:1.14(1.06,1.15)比1.20(1.14,1.28), P=0.023],但术后其他CTP参数组间比较差异均无统计学意义(均P>0.05)。(4)NIHSS评分及预后:术后18个月临床随访结果显示,随访期间患者均无新发卒中。桥血管通畅组和狭窄组术后7d及12、18个月的NIHSS评分与入院时比较均降低[通畅组:2(0,4)、1(0,2)、0(0,2)分比3(0,6)分;狭窄组:3(1,5)、3(1,6)、2(1,6)分比4(1,7)分],差异均有统计学意义(均P<0.05);但术后12、18个月桥血管通畅组NIHSS评分明显低于狭窄组,且通畅组预后良好的患者比例高于狭窄组[术后12个月:87.1%(88/101)比4/8,P=0.039;术后18个月:90.1%(91/101)比4/8,P= 0.025]。结论血管超声能够量化评估STA-MCA血管旁路移植术后桥血管的血流动力学改变,可应用于血管旁路移植术后长期的动态随访。
大脑中动脉(MCA)闭塞是导致缺血性卒中的重要原因之一,当颅内侧支循环代偿不足时,患者可因颅内低灌注出现反复发作的短暂性脑缺血发作(TIA),甚至卒中。近年来关于脑血运重建手术的研究结果显示,通过严格筛选手术适应证的患者,颞浅动脉(superficial temporal artery, STA)-MCA血管旁路移植术可有效改善症状性颈内动脉(ICA)或MCA闭塞患者神经功能障碍,增加其脑血流量,降低卒中复发风险。
STA-MCA血管旁路移植术后,评估供体动脉即桥血管血流通畅情况以及量化评估桥血管血流量的动态变化至关重要,但目前对于MCA闭塞性病变行STA-MCA血管旁路移植术后长期随访中出现桥血管狭窄的研究仍鲜见相关报道。尽管DSA是评估STA-MCA血管旁路移植术后桥血管通畅与否的“金标准”,但因其价格昂贵且为有创性检查,不宜作为动态随访的首选检查方法。彩色多普勒超声(color Doppler ultrasonography, CDU)能够实时动态显示桥血管即STA的二维形态学、血流充盈情况及血流动力学改变,经颅彩色多普勒超声(transcranial color coded Doppler, TCCD)能够直接观察颅内STA-MCA血运重建区域血管的血流动力学改变。因此,本研究拟通过CDU和TCCD评估单侧MCA闭塞患者接受STA-MCA血管旁路移植术后12个月内颅内外尤其是桥血管的血流动力学改变,评估桥血管的通畅率,为患者疗效的动态随访提供依据。
1 对象与方法
1.1 对象
回顾性连续纳入2018年1月至2023年3月于苏州大学附属第一医院神经外科经DSA确诊为单侧MCA闭塞并接受STA-MCA血管旁路移植术且术后临床随访18个月资料完整的患者109例,其中男72例,女37例,年龄27~74岁,平均(54±10)岁。根据术后12个月DSA评估桥血管STA通畅情况分为桥血管通畅组和非通畅组。本研究方案经苏州大学附属第一医院伦理委员会审核批准[审批号:(2024)伦研批第348号],所有患者或家属已签署诊疗知情同意书。
纳入标准:(1)术前及术后12个月及以上随访时均行头部CT、CT血管造影(CTA)、CT灌注(CT perfusion,CTP)和DSA检查;(2)术前经DSA诊断为单侧MCA闭塞;(3)手术前6个月内伴有因MCA闭塞引起的头晕、反复TIA或卒中等临床表现,经内科规范化药物治疗无效且手术时间距最后1次发病超过3周;(4)术前CTP证实闭塞侧MCA供血区域存在缺血灌注异常;(5)影像学及临床资料完整。
排除标准:(1)烟雾病、ICA闭塞性疾病行STA-MCA血管旁路移植术;(2)手术对侧存在ICA、MCA重度狭窄(狭窄率为70%~99%)或闭塞者;(3)闭塞侧MCA供血区域存在大面积脑梗死,即Alberta卒中项目早期CT评分(Alberta stroke program early CT score, ASPECTS)≤5分;(4)合并脑肿瘤、颅内动脉瘤以及脑血管畸形等其他神经系统疾病;(5)存在手术禁忌证,包括有严重的出血倾向、心功能和肾功能障碍等;(6)临床随访时间<18个月。
1.2 资料收集
患者入院24h内完成临床资料收集,包括年龄、性别、体质量指数和卒中高危因素(包括高血压病、高脂血症、糖尿病、吸烟和饮酒史、心房颤动)以及血生化指标,包括低密度脂蛋白胆固醇、高密度脂蛋白胆固醇、三酰甘油、总胆固醇、空腹血糖、超敏C反应蛋白;根据患者就诊时的神经系统体格检查,将其临床表现(近6个月内)分为头晕、记忆力减退、反应迟钝等非特异性症状及TIA、卒中;应用美国国立卫生研究院卒中量表(NIHSS)于患者入院时和术后7d评估患者神经功能,并记录NIHSS评分。
1.3 血管超声评估
采用荷兰PHILIPS公司的CX50 CDU诊断仪,选择3~12MHz宽频线阵探头和1~5MHz相控阵探头,检查方法和诊断标准参考《中国脑卒中血管超声检查指导规范》。于术前1~3d、术后4~7d及术后1、3、6、12个月分别进行血管超声检查,由两名具有10年以上工作经验的高年资超声科医师操作完成。
STA主干位于耳廓前方,通常位置固定,走行也相对直。术前,将CDU的线阵探头轻置于耳缘前方,记录STA主干血流动力学参数包括:内径(diameter,D)、收缩期峰值流速(PSV)、舒张期末流速(EDV)、阻力指数(resistance index,RI)、搏动指数(PI)、时间平均流速(time-averaged mean velocity, TAMV)和时间峰值流速(time-averaged peak velocity, TAPV);测量STA主干D值,系统自动计算时间平均流量(TAMV flow;ml/min)= π×(D/2)2×TAMV和时间平均峰值流量(TAPV flow; ml/min)=π × (D/2)2 × TAPV。
术后复查时,CDU对于桥血管的检测从STA主干即颅外段开始,通过二维灰阶和彩色多普勒血流显像沿着桥血管走行连续动态追踪至颅骨缺损处即其入颅段,观察管腔形态和血流充盈情况,并在其颅外段和入颅段分别记录血流频谱,分析血流动力学参数。于开颅处应用TCCD观察血管旁路移植区域颅内血管的血流充盈情况、血流方向和血流频谱形态。
1.4 一站式CT
采用德国SIEMENS第二代双源CT(SOMATOM Definition Flash)于术前1~3d及术后12、18个月分别行头部CT、主动脉弓上CTA及全脑CTP检查以观察患者脑灌注改变情况,术后1~2d行头部CT观察术区有无新发出血及缺血灶,扫描参数同本中心既往研究。图像传至后处理工作站SYNGO.VIA,应用软件CT Neuro Perfusion对图像进行后处理。避开血管、梗死灶、钙化等位置手工勾画感兴趣区(region of interest,ROI),软件自动生成镜像对称部位。获取手术前后半卵圆中心、基底节区及颞叶ROI的灌注参数并取其平均值作为最终结果,计算相对CTP参数即患侧与健侧ROI比值,包括相对脑血流量(relative cerebral blood flow, rCBF)、相对脑血容量(relative cerebral blood volume, rCBV)、相对达峰时间(relative time to peak, rTTP)和相对平均通过时间(relative mean transit time,rMTT)。由具有10年以上工作经验的放射科医师进行操作和解读。分别比较桥血管通畅组和非通畅组术后12、18个月与术前1~3d的CTP参数,以及两组之间CTP参数的差异。
1.5 DSA评估
采用德国Siemens Neurostar plus/ Top对患者行主动脉弓以上全脑血管选择性造影。所有患者于术前1~3d及术后12个月行DSA检查。术前1~3d主要观察MCA闭塞侧颅内血管侧支代偿情况,包括无侧支、大脑前动脉(ACA)区域脑膜支开放、大脑后动脉(PCA)区域脑膜支开放、ACA+PCA脑膜支开放;术后12个月对术侧颈外动脉进行正位与侧位造影,观察STA形态尤其是桥血管入颅段以及STA-MCA血管旁路移植吻合口的通畅情况、手术区域血供情况等,并根据DSA结果将患者分为桥血管通畅组和非通畅组(狭窄或闭塞)。选择性颈外动脉或STA造影后若桥血管不显影,则为闭塞;桥血管任何节段管腔变细,则为狭窄;桥血管及其吻合口周围血管显影良好则为通畅。以上操作由两名10年及以上工作经验的介入科医师进行。以DSA为“金标准”,将术后12个月CDU评估的STA通畅情况与术后12个月的DSA检查结果进行一致性检验。
1.6 手术方式
全部患者均采用STA-MCA血管旁路移植+硬脑膜翻转并颞肌贴敷的联合血运重建术式。术中选择STA顶支或额支作为供体血管,并将血管旁路移植时间控制在30min内,避免长时间阻断血管引起缺血事件的发生,并应用微型多普勒超声和吲哚氰绿荧光造影判断桥血管吻合通畅性。在颞肌贴敷后,关颅时咬除部分骨瓣,作为桥血管入颅的通道以防止其受压,并实时应用微型多普勒超声判断桥血管通畅性,发现异常及时微调以确保手术成功。
1.7 随访
患者术后12、18个月门诊复诊时,临床医师采用改良Rankin量表(mRS)评估患者神经功能预后情况,其中mRS评分≤2分为预后良好,mRS评分≥3分为预后不良,同时记录患者NIHSS评分。
1.8 统计学分析
应用SPSS19.0软件对数据进行统计学分析。对CDU和DSA检查桥血管通畅情况的结果行一致性检验,Kappa值≤0.20代表一致性较差,>0.20~0.40代表一致性一般,>0.40~0.60代表一致性中等,>0.60~0.80代表一致性良好,>0.80代表一致性极好。采用Kolmogorov-Smirnov方法对计量资料进行正态性检验,符合正态分布的连续性变量以x-±s表示,两组比较采用独立样本t检验;不符合正态分布的连续性变量以中位数和四分位数[M(P25,P75)]表示,组间比较采用Wilcoxon秩和检验。分类变量以例数表示,两组比较采用χ2检验或Fisher确切概率法。两组组间和组内手术前后不同时间点的STA血流参数、NIHSS评分、mRS评分和CTP参数的比较,符合正态分布的计量资料采用重复测量方差分析,不符合正态分布的计量资料和计数资料采用广义估计方程。以P<0.05为差异有统计学意义。
2 结果
2.1 CDU与DSA结果的一致性检验及两组患者临床资料比较
STA-MCA血管旁路移植术后12个月,CDU检查结果显示桥血管通畅者100例,桥血管狭窄者9例(未发现闭塞)。与DSA检查结果进行一致性检验,结果显示,二者一致性极佳,Kappa值为0.94(95%CI:0.81~1.00,P<0.01);仅有1例患者CDU显示桥血管入颅段呈“五彩镶嵌”血流频谱,血流速包括PSV和EDV升高,考虑局部管腔狭窄,而DSA显示为桥血管走形扭曲,管腔显影良好。见表1。
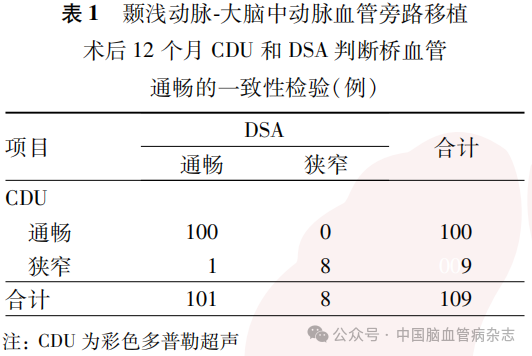
根据术后DSA结果将所有患者分为桥血管通畅组和狭窄组的对比结果显示,狭窄组患者吸烟、饮酒的比例和低密度脂蛋白胆固醇水平均高于通畅组,差异均有统计学意义(均P<0.05)。见表2。

2.2 术后桥血管STA血流动力学改变
桥血管STA通畅率:术后4~7d,CDU显示桥血管通畅率为98.2%(107/109),术后1、3、6和12个月,CDU显示桥血管的通畅率分别为98.2%(107/109)、97.2%(106/109)、95.4%(104/109)、92.7%(101/109),桥血管出现狭窄的部位均位于入颅段。
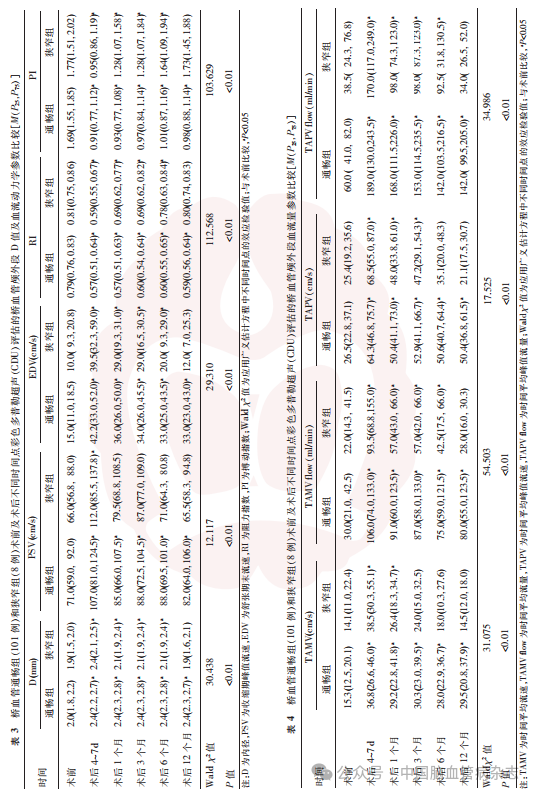
桥血管STA主干即桥血管颅外段血流动力学参数:与术前比较,术后4~7d及术后1、3、6、12个月桥血管通畅组的D增粗(Wald χ2=30.438),血流动力学参数包括血流速度(PSV、EDV、TAMV和TAPV;Wald χ2值分别为12.117、29.310、31.075、17.525)、血流量(TAMV flow和TAPV flow;Wald χ2值分别为54.503、34.986)均增加,而RI、PI均降低(Wald χ2值分别为112.568、103.629),差异均有统计学意义(均P<0.05);但狭窄组术后12个月D及血流动力学参数与术前比较,差异均无统计学意义(均P>0.05)。见表3,表4。
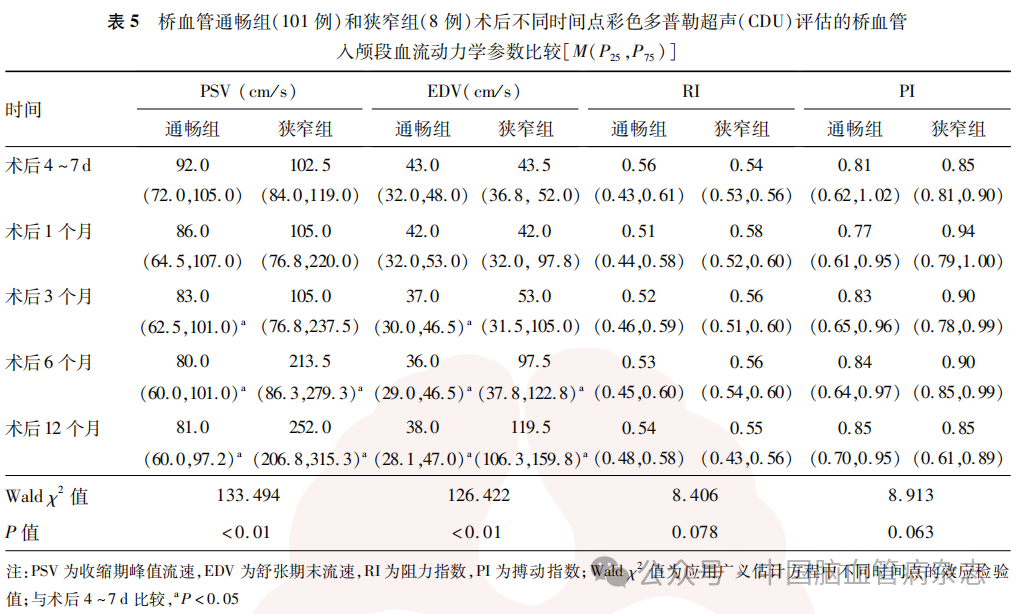
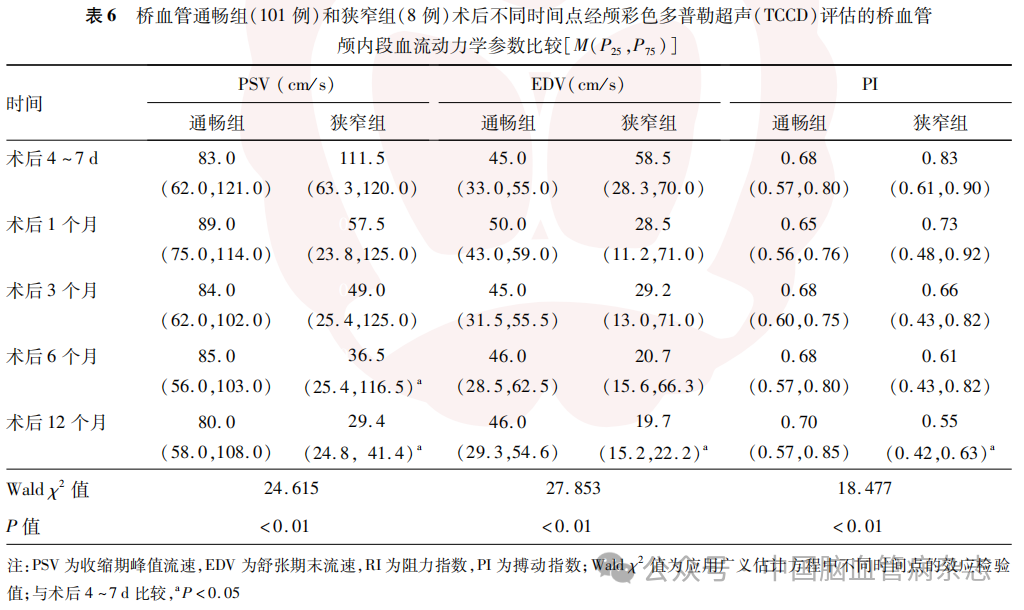
术后桥血管STA入颅段及颅内段的血流动力学参数:与术后4~7d相比较,术后12个月狭窄组入颅段PSV、EDV均明显升高,差异均有统计学意义(均P<0.05),但RI和PI与术后4~7d比较差异无统计学意义(均P>0.05)。见表5。与术后4~7d相比较,术后12个月狭窄组STA颅内段血流参数包括PSV、EDV和PI值均明显降低(均P<0.05)。见表6。
2.3 一站式CT结果分析
术后1~2d头部CT显示,手术区未见新发出血及缺血灶。与术前相比,术后12、18个月桥血管通畅组的CTP参数rCBF均升高,而rCBV、rTTP和rMTT均下降,差异均有统计学意义(均P<0.05);而与术前相比,术后12、18个月桥血管狭窄组rCBF均升高,rMTT均降低,差异均有统计学意义(均P<0.05),但rCBV、rTTP与术前相比差异均无统计学意义(均P>0.05)。术后12、18个月通畅组rTTP低于狭窄组(均P<0.05),但术后其他CTP参数组间比较差异均无统计学意义。见表7。
2.4 DSA结果分析
术前MCA闭塞侧颅内侧支代偿情况见表2。术后12个月的DSA显示,桥血管通畅组患者比例为92.7%(101/109),狭窄组为7.3%(8/109),未发现桥血管闭塞。
2.5 神经功能改善情况
术后18个月临床随访结果显示,随访期间患者均无新发卒中。桥血管通畅组和狭窄组术后7d及术后12、18个月的NIHSS评分与入院时比较均降低(均P<0.05),尤其术前伴有肢体乏力、感觉障碍、言语不清等神经功能障碍者在术后表现为症状减轻或消失。术后12、18个月,通畅组NIHSS评分明显低于狭窄组,且通畅组预后良好患者的比例高于狭窄组,差异均有统计学意义(均P<0.05)。见表2。
典型病例
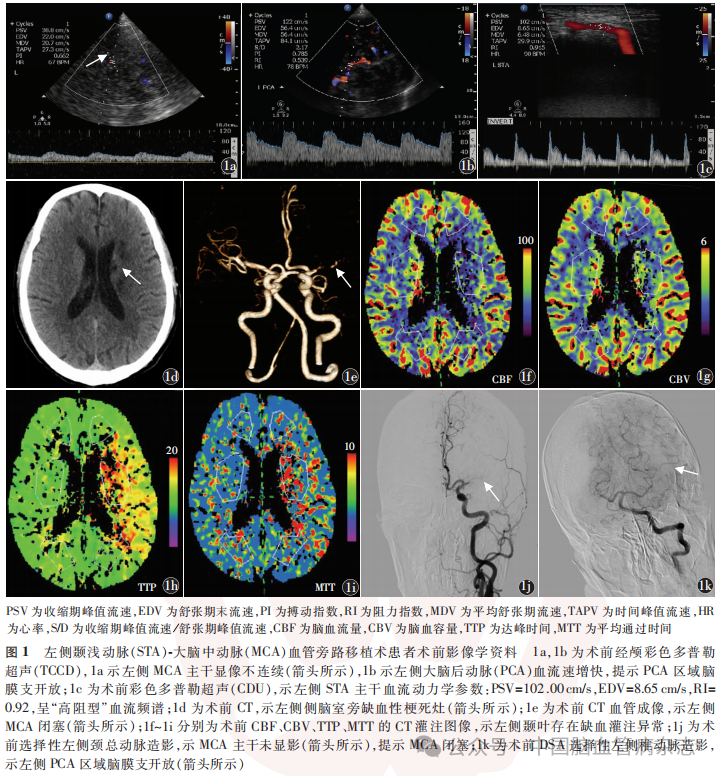
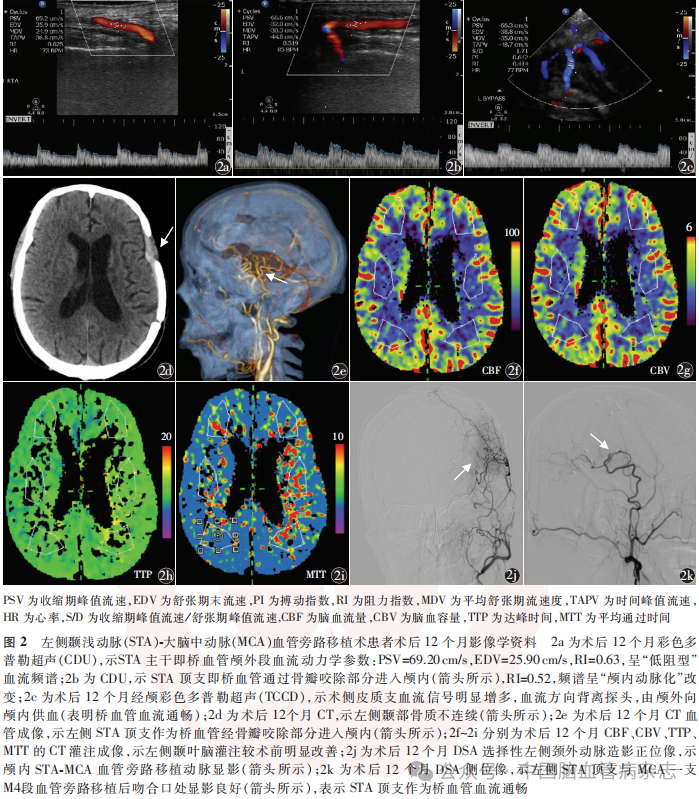
男,56岁,因“右侧肢体麻木3月余”于2022年3月23日入住苏州大学附属第一医院神经外科治疗,入院NIHSS评分2分,mRS评分2分。入院血压136/78mmHg,空腹血糖5.1mmol/L(正常值范围:3.9 ~ 6.1mmol/L),总胆固醇、低密度脂蛋白胆固醇、高密度脂蛋白胆固醇、三酰甘油均未见异常,超敏C反应蛋白4.0mg/L(正常值范围:0~3.0mg/L)。既往高脂血症10余年,服药控制;无高血压病及糖尿病史。2022年3月24日行TCCD示左侧MCA主干显像不连续(图1a),左侧PCA血流速增快,提示PCA区域脑膜支开放(图1b),术前CDU示左侧STA主干血流动力学参数:PSV=102.00cm/s,EDV=8.65cm/s,RI=0.92,呈“高阻型”血流频谱(图1c);CT示左侧侧脑室旁缺血性梗死灶(图1d),CTA示左侧MCA闭塞(图1e),CTP示左侧颞叶缺血灌注异常(图1f~1i);2022年3月25日术前DSA选择性左侧颈总动脉造影示MCA主干未显影,提示MCA闭塞(图1j),DSA选择性左侧椎动脉造影后,左侧PCA区域脑膜支开放(图1k);2022年3月26日行左侧STA-MCA血管旁路移植术+硬脑膜翻转并颞肌贴敷的联合血运重建术。术后12个月(2023年3月29日)CDU示左侧STA顶支即桥血管通过骨瓣咬除部分进入颅内(图2a,2b);TCCD示桥血管颅内段显像良好(图2c);CTA示桥血管吻合通畅,CTP示左侧颞叶灌注改善(图2d~2i);2023年3月30日DSA示左侧桥血管血流通畅(图2j,2k)。术后12、18个月门诊随访NIHSS评分均为1分,mRS评分均为1分。
3 讨论
通过STA-MCA血管旁路移植+硬脑膜翻转并颞肌贴敷的联合脑血运重建手术主要应用于治疗烟雾病及ICA或MCA慢性闭塞性病变,对于改善脑灌注,预防卒中复发,提升患者生存质量有显著效果。但由我国发起的颅外-颅内动脉血管旁路移植术治疗症状性ICA和MCA闭塞(carotid and middle cerebral artery occlusion surgery study,CMOSS)的多中心研究结果却显示,在过去1年内因ICA或MCA闭塞和血流动力学功能不全导致的TIA或非致残性缺血性卒中患者中,距末次发生TIA或卒中超过3周并接受STA-MCA血管旁路移植术(随机分组后7d内进行手术)联合药物治疗的患者与单独接受药物治疗的患者的主要结局(随机分组后30d内卒中或死亡、或30d以上至2年内同侧缺血性卒中;8.6%比12.3%;OR=0.71,95% CI:0.33~1.54,P= 0.39)差异无统计学意义。然而,这并不能完全否定STA-MCA血管旁路移植术对症状性ICA或MCA闭塞患者的治疗价值,而是预示着其临床应用还需进一步深入研究。
本研究显示,在STA-MCA血管旁路移植术后,应用CDU与DSA判断桥血管通畅与否的一致性极好,Kappa值为0.94;且术后随访过程中应用CDU可动态观察桥血管尤其是其入颅段的走行,能直观判断桥血管是否通过骨瓣缺口处进入颅内,且桥血管通畅组STA主干即桥血管颅外段的RI、PI值与术前相比明显减低,是频谱“颅内动脉化”的直接体现,与既往研究结果相符。此外,骨瓣缺损为血运重建术后TCCD的应用提供了良好的骨窗条件,而TCCD亦能够通过骨质不连续的位置确定桥血管是否显像并进入颅内(若血流方向发生逆转,则表明由颅外的STA向颅内供血)从而可综合评估血管旁路移植手术的有效性。本研究结果还显示,单侧MCA闭塞患者行STA-MCA血管旁路移植后,术后4~7d CDU显示,2例患者桥血管入颅段发生狭窄,考虑是受术区颞肌水肿、骨瓣压迫所致,CDU显示术后12个月桥血管出现狭窄的部位均位于入颅段,但未发现桥血管闭塞者,提示对血管旁路移植术后的患者进行动态随访、建立规范的复查时间轴非常重要。本研究狭窄组患者吸烟、饮酒的比例和低密度脂蛋白胆固醇水平均高于通畅组,提示临床医师在术后应进一步联合药物治疗控制卒中高危因素以预防桥血管狭窄,但由于术后12个月狭窄组病例较少,故本研究中未进一步行多因素Logistic回归分析以探索影响桥血管狭窄的可能因素。
Morton等对应用桡动脉或大隐静脉作为桥血管进行高流量血管旁路移植的36例患者进行>3个月的随访,结果显示,桥血管的TAMV flow范围为65~200ml/min,平均值为130ml/min,但CDU显示TAMV flow<65ml/min的5例患者的CTA证实其桥血管均出现狭窄(血管扭曲或血栓形成所致),且其中3例发生TIA,提示CDU对血管旁路移植术后患者进一步行血管内治疗或开放修复桥血管具有参考意义。本研究中CDU检测结果显示,通畅组术后12个月桥血管的TAMV flow中位数为80.0(55.0, 123.5)ml/min,而非通畅组桥血管的TAMV flow中位数为28.0(16.0, 30.0)ml/min,表明当桥血管出现狭窄时能够显著影响其向术区提供血流量,通过CDU检测的TAMV flow可为STA-MCA血管旁路移植术患者的术后桥血管随访提供依据。国内有研究者应用CDU在38例患者(41个大脑半球)行STA-MCA血管旁路移植术后1周和术后6、12个月进行动态随访,结果显示,3个复查时间点STA流量逐步减低(F=3.861,P<0.05),但STAD值、PSV差异无统计学意义(F值分别为1.663、2.044,均P>0.05)。在本研究的动态随访过程中,通畅组桥血管的D值基本维持稳定,且血流速度和流量也未完全呈现下降趋势;但STA狭窄组患者术后12个月桥血管入颅段出现明显狭窄后,其颅外段的内径变细,血流量亦随之降低。Ning等研究显示,将ICA颅内段以及MCA重度狭窄或闭塞患者根据手术意愿分为STA-MCA血管旁路移植术组和单纯药物治疗组,结果显示,术前CTP示患侧脑灌注缺血越严重的患者,接受血管旁路移植术后半年其脑血流动力学改善越明显,且STA-MCA血管旁路移植手术组年卒中发生率低于单纯药物治疗组(6.7%比25.6%,P<0.05),提示筛选可从血管旁路移植术中获益的患者的关键之一为选择有缺血灌注异常的患者,术前存在脑灌注缺血异常是严格筛选手术适应证的重要依据之一。rTTP是CTP参数中评估脑灌注状态较为敏感的半定量指标,本研究中,术后12、18个月通畅组CTP参数中rTTP低于狭窄组(均P<0.05),表明通畅组术后脑灌注改善情况较狭窄组更明显;但术后12、18个月桥血管通畅组和狭窄组CTP参数中的rCBF增加、rMTT下降,但差异均无统计学意义(均P>0.05),提示两组患者脑灌注均得到改善。
本研究显示,术后12、18个月桥血管通畅组NIHSS评分较术前明显减低,提示STA-MCA血管旁路移植术有效改善了患者的临床症状和生存质量。而桥血管狭窄组NIHSS评分亦较术前减低,一方面因桥血管即使出现狭窄,但仍有少量血流经桥血管进入颅内,另一方面考虑与本研究采用直接STA-MCA血管旁路移植+硬脑膜翻转并颞肌贴敷的联合脑血运重建术式有关,即间接血运重建随时间推移可建立一定的血流补偿。此外,术后12、18个月桥血管通畅组NIHSS评分明显低于狭窄组,且患者临床预后良好的比例也明显更高,提示当桥血管出现狭窄尤其是重度狭窄后,其向颅内提供的血流受限,同时也表明对于行联合脑血运重建术式的患者,对脑灌注及神经功能改善发挥主要作用的血供仍为直接血管旁路移植的桥血管。值得注意的是,即使桥血管发生狭窄患者在随访期间也未发生缺血性卒中,这与Murai等研究结果相一致,可能与间接血运重建、颅内侧支循环建立有关。同时也表明,患者在接受STA-MCA血管旁路移植术后,仍应结合药物治疗对卒中高危因素进行干预,防止桥血管出现狭窄甚至闭塞。
综上所述,基于CDU、TCCD的超声影像学检查能够评估STA-MCA血管旁路移植术后桥血管的血流动力学动态改变,判断其通畅性,可为其临床疗效评估提供参考依据。但本研究尚存在不足之处:纳入样本量偏少,特别是术后12个月复查CDU时桥血管发生再狭窄的病例数较少,导致两组之间病例数不均衡,故未进一步行多因素Logistic回归分析影响桥血管狭窄的可能因素。另外,本研究仅纳入患者术前及术后18个月内随访资料,今后应积累大量STA-MCA血管旁路移植术后患者,对桥血管颅外段和颅内血流状态的改变趋势进行长期动态监测和总结。