obe-cel
Obecabtagene autoeucel (obe-cel)是一种自体41BB-ζ抗CD19 CAR-T细胞疗法,使用中间亲和力CAR来减少毒性作用并提高持久性。Obe-cel已于2024年11月8日获得美国 FDA 批准,是 FDA 批准的首个无需 REMS 计划(风险评估缓解策略)的 CAR-T 疗法,其独特的快速靶标结合解离设计使其与现有疗法区分开来,CAR与CD19结合后具有较快的解离速度,避免了T细胞过度激活,不易发生T细胞耗竭,从而提高了CAR-T疗法的持久性,理论上能在不牺牲疗效的情况下,显著降低治疗中细胞因子释放综合征等严重不良反应的风险。此外,区别于其他CAR-T产品的单次回输,Obe-cel采用清淋化疗后分次剂量输注的方式给药;清淋预处理也有些许差别。
Obe-cel的获批是基于一项1b/2期多中心FELIX研究(美国、西班牙、英国34家中心参研),近日新英格兰医学杂志发表了该研究结果。

研究结果
该研究纳入复发或难治性CD19阳性B细胞急性淋巴细胞白血病(R/R B-ALL)成人(≥18岁)患者153例,其中127例(83.0%)接受了输注。1b期和2期部分均有A和B队列,2期部分还有C队列;主要队列为2A队列(n=94),包括有形态学疾病的患者(骨髓原始细胞≥5%),队列2B的患者有可测量残留病(骨髓原始细胞<5%);队列2C为孤立性髓外病变患者。

患者中位47岁,既往中位2线治疗,52.0%对末线治疗难治;41.7%接受过贝林妥欧单抗,31.5%接受过奥加伊妥珠单抗,16.5%接受过两者;44.1%接受过异基因移植;22.8%存在髓外病变。92.9%的患者接受了桥接治疗,主要是化疗。
Obe-cel在清淋预处理后以骨髓负荷调整的分割剂量给药,在清淋前要求进行骨髓评估以指导剂量,第二次给药是在没有严重或未解决的毒性作用的情况下。127例患者中共有120例(94.5%)接受了两次的计划给药,7例(5.5%)仅接受第一次给药。队列2A有94%接受了两次给药。
队列2A输注患者中位随访20.3个月,总缓解率为77%,完全缓解率为55%,完全缓解伴血液学不完全恢复率为21%;中位缓解持续时间为14.1个月,中位无事件生存期为9.0个月。
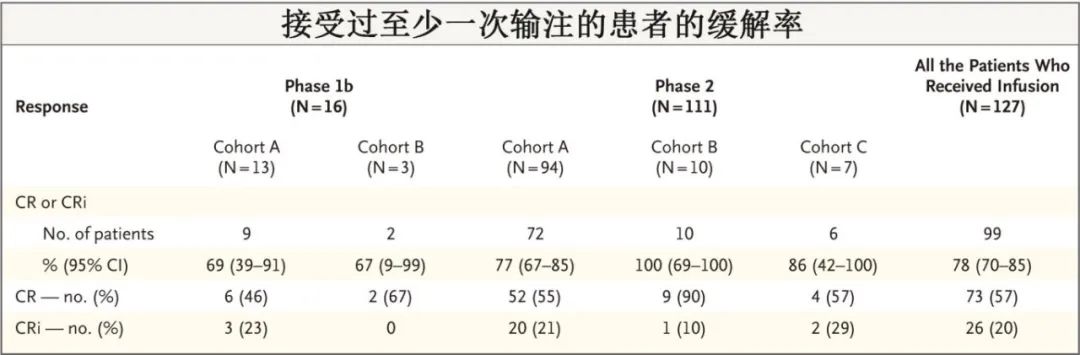
在接受至少一次Obe-cel输注的127例患者中,中位随访21.5个月,总缓解率为78%,完全缓解率为57%,完全缓解伴血液学不完全恢复率为20%。中位缓解持续时间为21.2个月,中位无事件生存期为11.9个月,6个月和12个月无事件生存率分别为65.4%和49.5%,清淋前骨髓负荷影响无事件生存期,骨髓原始细胞<5%、5-75%和>75%的患者中12个月无事件生存率分别为68%、55%和25%。中位总生存期为15.6个月,6个月和12个月总生存率分别为80.3%和61.1%,清淋前骨髓负荷影响总生存期,骨髓原始细胞<5%、5-75%和>75%的患者中12个月总生存率分别为72%、59%和55%。
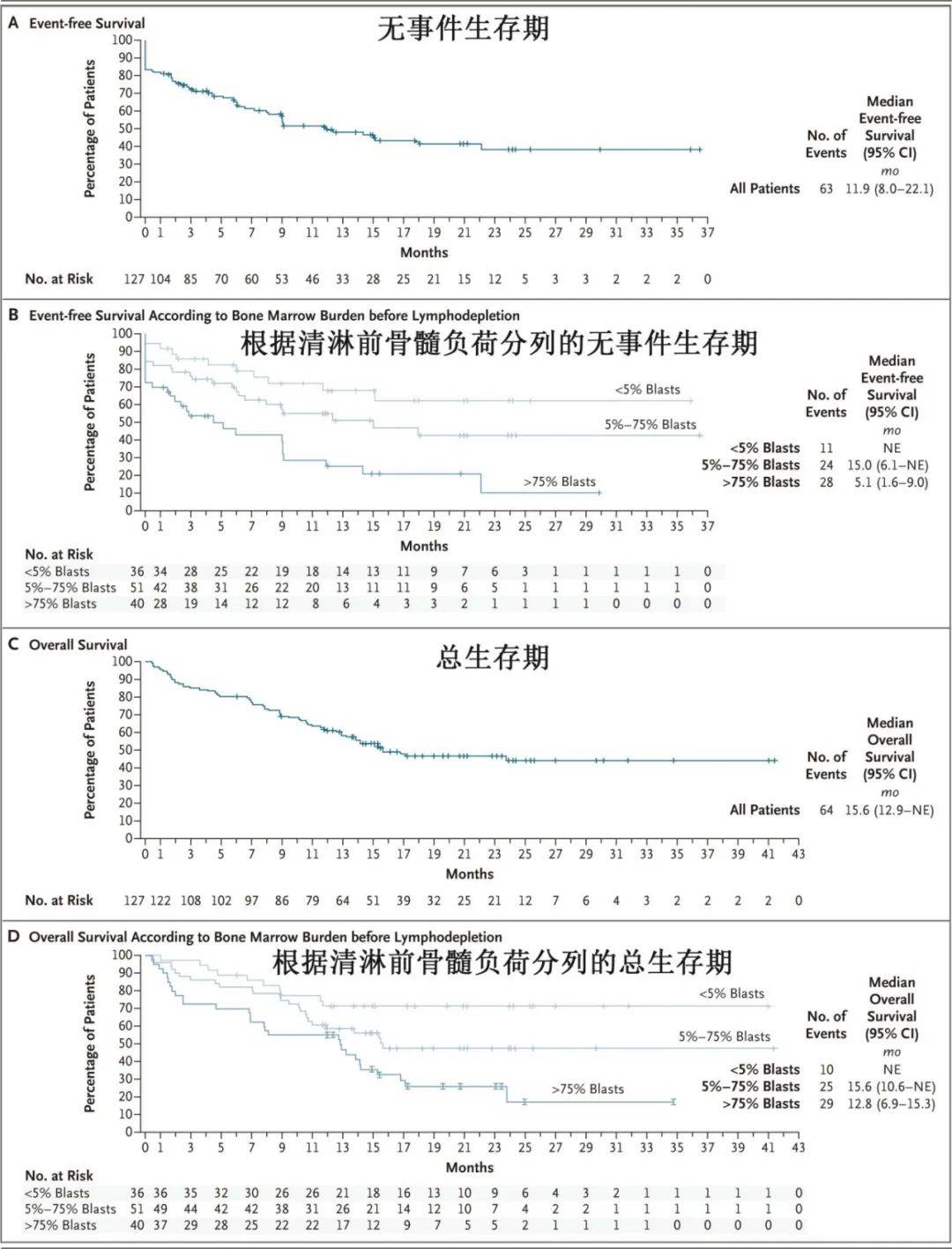
此外18%的患者在输注Obe-cel后接受了异基因移植,移植和未移植患者的无事件生存期和总生存期无显著差异。
末次随访时31%的患者形态学复发,清淋时骨髓负荷影响复发率:骨髓原始细胞<5%、5-75%和>75%的患者中复发率分别为19%、29%和50%。
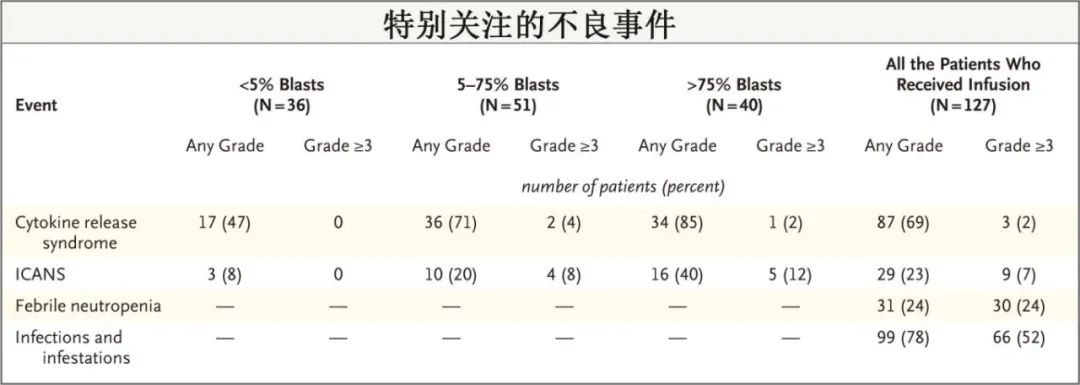
2.4%的患者出现≥3级细胞因子释放综合征,7.1%的患者出现≥3级免疫效应细胞相关神经毒性综合征,24.4%的患者发生粒缺性发热,5例死于感染。此外在发生≥3级免疫效应细胞相关神经毒性综合征的9例患者中,5例(56%)在清淋前骨髓原始细胞>75%,4例(44%)为5-75%;<5%的患者中为无≥3级免疫效应细胞相关神经毒性综合征。
总结
在复发或难治性B细胞成人ALL患者中,Obe-cel具有高持续缓解率(尤其是骨髓负荷低-中的患者),且≥3级免疫相关毒性发生率较低。
参考文献
Roddie C, et al. Obecabtagene Autoleucel in Adults with B-Cell Acute Lymphoblastic Leukemia.N Engl J Med . 2024 Nov 27. doi: 10.1056/NEJMoa2406526.