外阴硬化性苔藓(vulvar lichen sclerosus,VLS)是一种以女性外生殖器瘙痒疼痛及皮肤黏膜色素减退为主要特征的慢性非瘤样皮肤疾病。有研究表明,北美洲女性VLS的发病率约为1.7%,且在青春期少女和绝经期妇女中出现高峰。
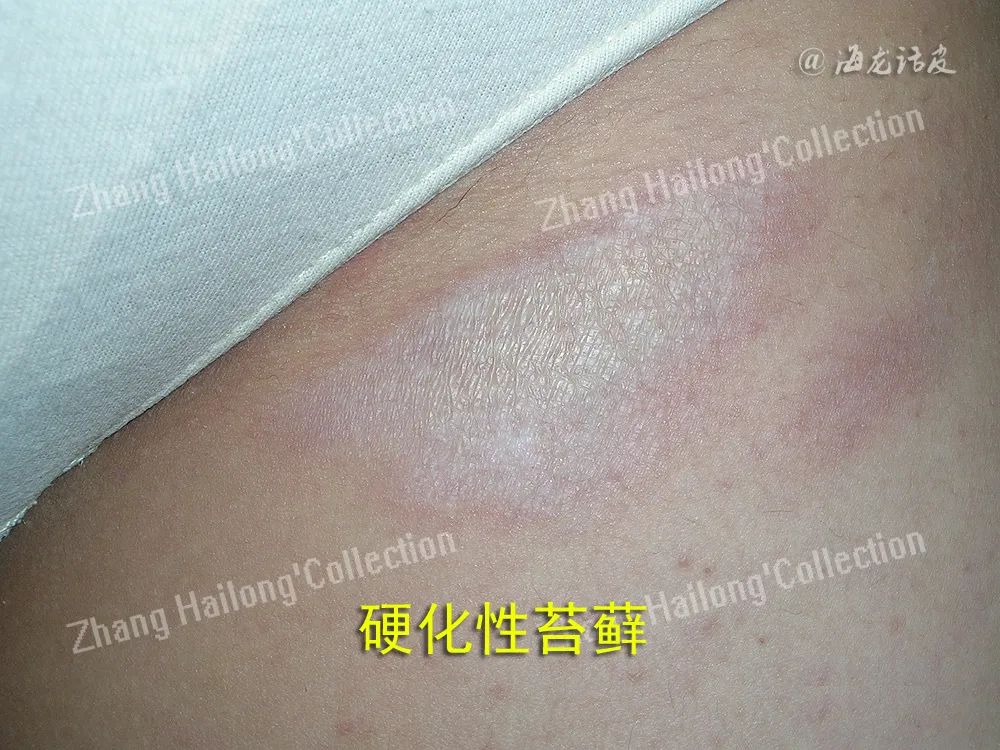
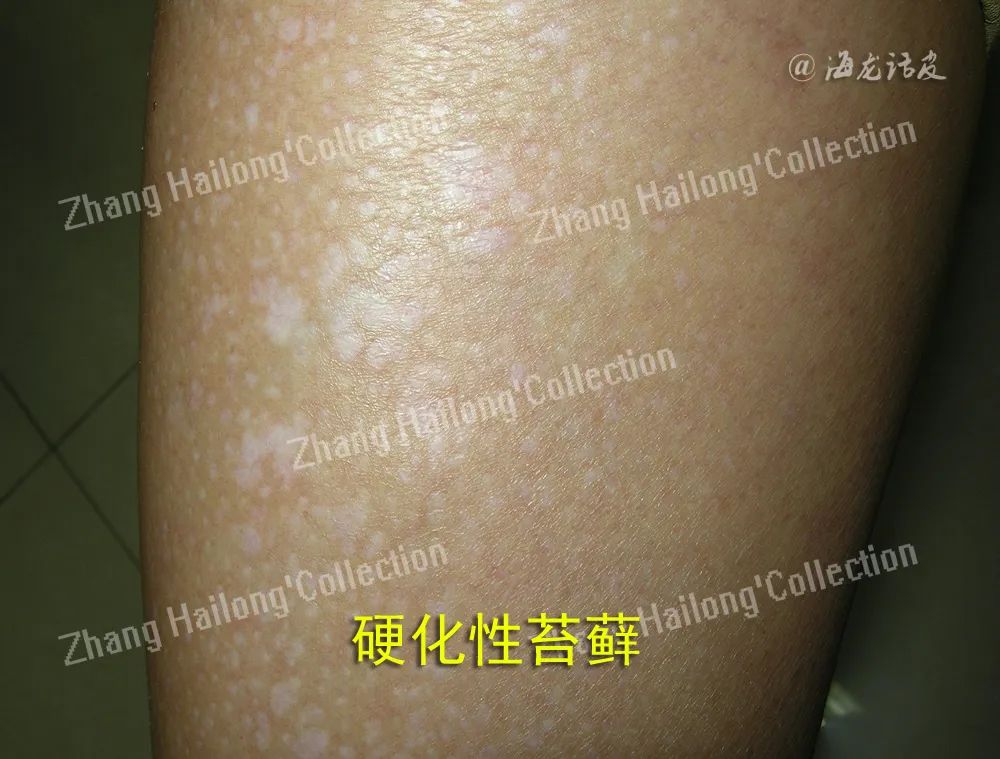
它主要影响女性大小阴唇及肛周,表现为病损处皮肤和黏膜色素减退,出现白色斑块或丘疹,表皮粗糙肥厚、增生角化,起褶皱,进而发展成外阴粘连、阴蒂融合,导致排尿困难、性功能受损等。若病变未经有效的干预治疗,最终可进展为不可逆的外阴解剖结构改变以及恶性肿瘤,严重危害患者的心理和生理健康
病因及发病机制
VLS的病因尚不明确,目前认为VLS的发病可能与机体自身免疫异常、性激素调节失衡、家族遗传、代谢异常以及局部刺激等因素有关。
1、自身免疫异常:
有研究发现VLS患者常合并桥本甲状腺炎、白癜风、恶性贫血和银屑病等自身免疫性疾病。VLS可通过促进辅助性T细胞1(helper T cell 1,Th1)分化及过表达来抑制机体T细胞的平衡调节,破坏机体的自我耐受,促进炎症的发生,进而产生活性氧(reactive oxygen species,ROS)物质成为氧化应激扳机点,引起DNA、蛋白质等大分子的结构变化,导致自身免疫性疾病的发生。此外,ROS氧化应激的过程还会引起真皮血管的收缩和损伤,造成局部组织缺血缺氧,从而出现营养不良、组织硬化、瘢痕形成和肿瘤发生,加速VLS的进展和恶化。这些结论提示VLS的发病可能与机体自身免疫异常有关。
2、性激素调节失衡:
VLS的发病率在青春期少女(12~16岁)和绝经期妇女(40~60岁)中呈双峰分布,可能与性激素作用有关。青春期少女卵巢尚未发育成熟,绝经期妇女卵巢功能开始下降,这两种情况都可能导致体内性激素水平紊乱、分泌减少。性激素水平较低可能影响女性器官发育,导致外阴皮肤缺乏营养、弹性降低。局部外用睾酮替代治疗后,患者外阴瘙痒明显减轻,但复发率较高。由此可见,性激素在抑制VLS病情进展方面具有一定作用,且其在体内的含量与该病的严重程度密切相关。
3、遗传因素:
有研究显示,5%~12%的VLS患者的直系亲属(如父母及兄弟姐妹)也被诊断为VLS。这提示VLS的发病可能与家族遗传有关。Haefner等通过全外显子组测序将有VLS家族史的家庭与无VLS家族史的家庭进行比较,结果发现,有VLS家族史的家庭基因组谱中可能存在抑制蛋白质功能的变异基因,比如LATS2、CD177、CD200和ANKRD18A。此外,Tran等通过免疫组织化学分析发现VLS的遗传倾向与调节人类白细胞抗原(human leukocyte antigen,HLA)Ⅱ类抗原的基因表达水平呈正相关。此外,该研究还发现VLS患者中有50%的成年女性和66%的青春期前女性出现了HLA-DQ7,这提示HLA-DQ7可能在VLS的易感性中发挥作用。
4、代谢异常:
成纤维细胞生长、胶原合成异常、硬化组织形成可能参与了VLS的发生、发展。研究结果发现,VLS患者体内的微小RNA-155(microRNA-155,miR-155)基因出现过表达,降低了抑癌基因 FOXO3和CDKN1B在体内的表达和活性,加快了成纤维细胞的增殖,促进了硬化组织的形成。另外,胶原蛋白的合成减少促进了真皮层成纤维细胞的产生,抑制了弹性纤维的生成,最终导致皮肤弹性降低。
5、局部刺激:
会阴部闭塞潮湿的环境、内裤的质地、运动时的摩擦及分娩时的组织损伤等因素都会不断刺激女性外生殖器。这些刺激因素作用于神经纤维和神经末梢,使外阴部皮肤和黏膜出现角化异常、增厚、粗糙、变硬等,进而发生局部神经和血管的营养失调,导致局部色素减退或消失。
诊断
VLS的病因尚不明确,目前认为VLS的发病可能与机体自身免疫异常、性激素调节失衡、家族遗传、代谢异常以及局部刺激等因素有关。
1、临床表现:
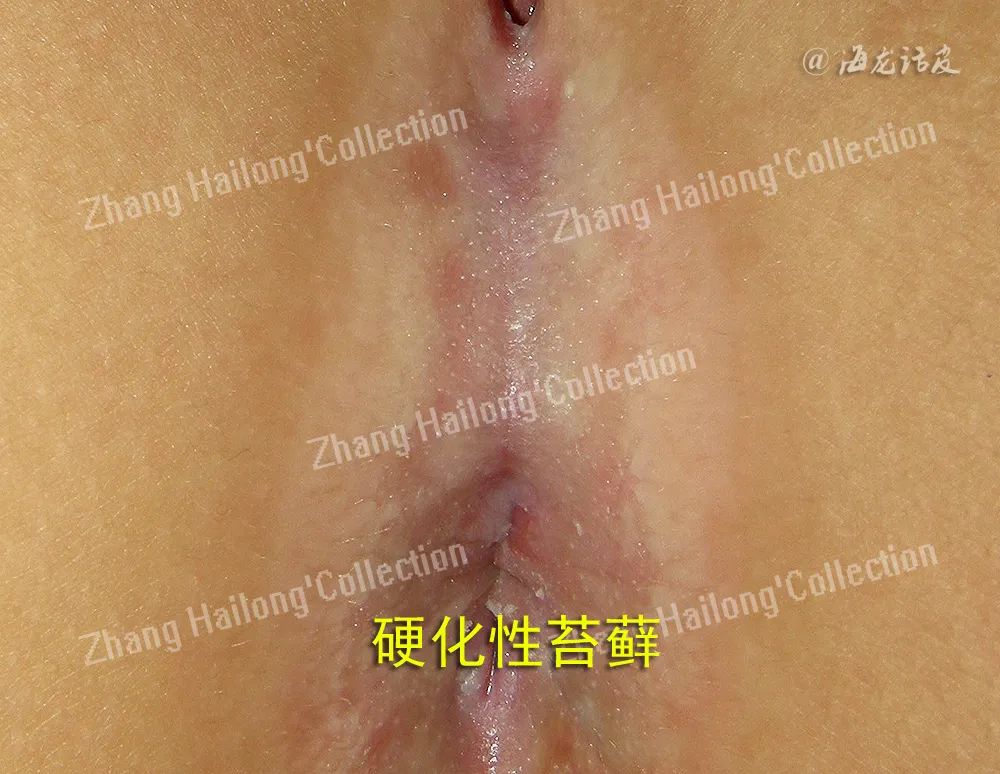
成人VLS最主要的症状是外阴瘙痒,尤以夜间为甚,部分患者由于疾病的持续进展还可能出现外阴烧灼痛、排尿困难或性交不适。该病难鉴别、易漏诊,疾病晚期病损区皮肤会变薄,起褶皱(牛皮纸样外观),出现白色斑块和丘疹,继而进展形成会阴粘连,导致小阴唇融合、阴道口狭窄、阴蒂埋没。若病变延伸至肛周,可形成经典的“8字形”外观。
VLS在儿童或青少年时期发生发展被称为青少年外阴硬化性苔藓(juvenile vulvar lichen sclerosus,JVLS)。与成人一样,JVLS的临床表现也有持续的生殖器症状,包括外阴瘙痒、刺激疼痛、皮肤裂隙出血和便秘。此外,患儿还可能因排尿困难、害怕排尿、憋尿产生更严重的尿路症状,如溢流性尿失禁。同样地,若JVLS持续发展可以出现病变区域变白、皮肤褶皱、局部解剖结构变化、阴道开口狭窄以及癌变等风险。
2、组织病理学诊断:
对于临床情况较复杂的患者,常需进行组织活检来确诊(取皲裂、溃疡处皮肤行多点活检),组织病理学检查是诊断VLS的金标准。显微镜下可见真皮水肿,浅层的胶原纤维变性,伴大量淋巴细胞浸润,此外还可以出现基底层细胞水肿、棘细胞层萎缩以及表皮层黑色素细胞减少。可疑恶变的VLS还会有组织鳞状上皮增生伴角化不全或角化过度。需要注意的是,对于儿童VLS,通常不取活检确诊。这是因为活检可能会对她们造成心理和身体的创伤,只有当病变加重而对应治疗无效时才使用该方法。
治疗
当前,临床上针对VLS的治疗方案有多种,但大多数治疗结果不能让人满意,这可能是由于VLS的发病机制尚不清楚,未能找到其确切的病因。该病治疗的主要目的和原则是缓解瘙痒疼痛症状、延缓病变进展以及预防远期并发症,并最终提高患者生活质量。
1、一般治疗:
VLS可由局部刺激所致,因此减少刺激因素可以有效缓解VLS的临床症状。例如,保持会阴及肛周皮肤干燥清洁,少吃辛辣油腻等刺激性食物,选择舒适透气的内裤,避免药物或洗涤剂清洗会阴,保持心情愉悦以及进行适当的体育锻炼等。针对少数紧张焦虑的VLS患者,可以适量应用镇静催眠药物辅助治疗。
2、药物治疗:
皮质类固醇激素:目前公认的VLS一线治疗仍然是局部外用皮质类固醇,它可通过影响炎症介质、炎症细胞和溶酶体酶来发挥对抗炎症、抑制免疫及调节胶原纤维合成的作用。Chin等发现局部皮质类固醇治疗可降低VLS进展为恶性肿瘤的概率,但是长期使用可能造成外阴皮肤黏膜萎缩及毛细血管扩张,且停药后容易复发。
主要用法为:患处涂抹0.05%丙酸氯倍他索软膏,2次/d,持续1个月,然后更改用药频率为1次/d,持续2个月,最后调整为每周使用2次,持续3个月,共用药6个月。虽然VLS是慢性进展性疾病,但通过药物的维持治疗,疾病仍然可以得 到有效控制。
性激素替代疗法:VLS的发生可能与体内性激素的缺失有关,因此可以考虑利用人工补充性激 素的方式进行替代治疗。性激素可以增加蛋白质的合成,使萎缩变性的皮肤黏膜得到营养进而恢复正常。成年女性中,因为缺少雌激素而出现VLS症状如阴道干燥和性交困难时,大多可使用8%孕酮软膏缓解。对于外阴皮肤缺少雄激素受体的VLS患者,常采用丙酸睾酮霜治疗。
主要用法为:患处涂抹2%丙酸睾酮霜,3次/d,持续1个月,然后更改用药频率为1次/d,持续3周。该药需要长期涂抹,不良反应主要表现为阴蒂增大及毛发旺盛,此时应立即停药或根据情况更改为其他药物。对于儿童VLS患者,随着年龄的增长,其卵巢功能逐渐成熟,性激素分泌增多,后期大多可自愈,因此通常不建议使用雄激素药物治疗,防止出现男性化特征。
免疫抑制剂:免疫抑制剂可以通过调控炎性介质及免疫调节因子的产生和释放,发挥抗炎和免 疫调节作用。有文献证明,钙调磷酸酶抑制剂(如他克莫司)通过抑制T细胞内钙依赖性信号传导途径,抑制T细胞的活化和增殖,从而减少白细胞介素-2(interleukin-2,IL-2)等细胞因子的生成,达到调节自身免疫的作用。
使用方法:局部使用他克莫司乳膏2次/d,持续8周。长期应用皮质类固醇激素治疗活动性VLS出现较严重的不良反应后,钙调磷酸酶抑制剂是其有效的替代品。在VLS的维持治疗阶段使用他克莫司软膏,可以有效地缓解疾病症状和预防远期并发症。临床医生应当提前告知患者,最初使用时患处可能会出现短暂轻微的烧灼痛,这是正常现象。
富血小板血浆(platelet-rich plasma,PRP):治疗近年Tedesco等的一项研究发现,PRP治疗可以通过脂肪间充质干细胞重构细胞外基质、抑制纤维化以及促进受损组织再生,来减轻VLS患者的组织病理学炎症反应。此外,因其富含血小板,可释放高浓度的生长因子和其他生物活性分子,有效对抗炎症、提高间充质细胞的增殖能力、修复病变损伤组织以及促进血管再生,从而缓解患者的病情。
3、物理治疗:
CO2激光治疗:近年来,激光作为一种微创治疗手段已经被广泛应用于各种阴道和外阴疾病。多项研究证明,激光具有改变组织特性的作用。这些发现让激光在临床上被用于非黏膜瘢痕和皱纹组织的重建。其主要机制是:激光作用于黏膜后产生热效应,使局部温度迅速升高,进而病变组织出现汽化、水肿和表皮剥脱,促进新血管、新胶原生成及胶原小梁结构的恢复,以此达到改善微循环及重建深层组织的效果。
与未接受任何治疗的VLS患者相比,经激光治疗1个月后的VLS患者活组织镜检可见上皮增厚伴表皮浅层脱落,毛细血管拉长,上皮细胞中糖原及成细胞活性增加。这些现象都表明经激光治疗后,胶原蛋白和细胞基质等能改善VLS症状的物质会增加。另外,该治疗方法还能明显减少VLS患者机体内的血清炎性因子,进而降低炎症反应,缓解临床症状,达到抗炎、止痒、止痛的作用,有效改善了患者的生活质量。与其他物理治疗相比,CO2激光治疗复发率较低,不良反应较轻,安全性更高,疗效更确切。
聚焦超声治疗:聚焦超声治疗利用超声波穿透表皮组织,将能量聚集在皮肤黏膜真皮层,使真皮层血管得到激活再生,血管内皮细胞的通透性增强,从而改善了病变处的营养状况,促进了组织修复及再生,有效阻止了皮肤黏膜的变性和萎缩。但是,经过长期的随访发现,长期接受聚焦超声治疗会导致照射部位局部神经末梢的敏感性增加,患处早期可出现不同程度的水肿及疼痛。若在治疗的同时给予局部冷敷处理,症状会逐渐减轻,患者的依从性也得以提高。
盐酸氨酮戊酸光动力疗法(ALA-PDT):研究发现,经过ALA-PDT治疗后,VLS患者的临床体征 (如病变大小和色素减退程度)和主观症状(如患处瘙痒和烧灼痛)均得到明显改善。光敏药物5-氨基酮戊酸局部外敷于病损部位,经过光动力治疗仪的适当波长激活,可转化为光敏代谢产物原卟啉以及发生光化学反应,诱导ROS和细胞毒性物质的产生,导致淋巴细胞和角质形成细胞凋亡,从而起到抗炎、抗角质形成和调控局部免疫功能的作用,有效阻止真皮硬化。此外,该方法还能增强基质金属蛋白酶(matrix metalloproteinase,MMP)中胶原酶(collagenase)的活性,抑制胶原合成,恢复皮肤弹性,达到治疗VLS的目的。
自体脂肪移植:自体脂肪移植是一种能减少皮肤纤维化、改善皮肤质量的新型再生疗法。因易于获得且生物相容性好,在各种开创性研究中均发现其可以用于VLS的治疗。少数患者移植后可出现恢复部位不对称、脂肪坏死或水肿红斑等不良反应。由于缺乏广泛的数据支持,自体脂肪移植的实际并发症尚不明确,该方法对VLS的实际治疗效果仍需要大量的随机对照试验来进一步证实。
4、手术治疗:
若VLS患者的病情出现进一步加重、经保守治疗无效或病损处有不典型增生等可疑恶变的情况时,可考虑手术治疗。主要术式为外阴表浅切除术或外阴粘连松解术。近年来,微创手术正逐渐兴起。研究发现,微创手术(如外阴瘢痕组织剥离术)能有效改善女性外阴粘连所致的性交困难或排尿障碍。然而,手术治疗并不能完全治愈VLS,且切除后复发率较高,仍然需要长期用药辅助治疗,因此临床上应用较少。
预后随访
多项研究发现,2%~5%的VLS可能进展为恶性外阴鳞状细胞癌(vulvar squamous cell carcinoma,VSCC)或分化型上皮内瘤变(differentiated vulvar intraepithelial neoplasia,DVIN)。因而,关于该病的治疗,除了选择合适的方式,其出院后的长期随访也尤为重要。临床医生应该密切监测VLS患者的预后,以便及时发现任何可疑的不良变化。常规提倡于治疗后的第3、6、12个月随访,之后每半年至一年进行1次随访。患者应当谨遵医嘱,积极规范化治疗,不可随意停药。只有这样,才能使该病的临床恢复达到效果最大化,才能更有效地阻止VLS进展为恶性肿瘤。
结语
VLS作为一种难鉴别、易漏诊的疾病,大众对其认知仍十分有限。VLS难治性的外阴瘙痒症状不仅会造成患者生理上的困扰,同时,还可能使她们失去自信、变得焦虑,显著影响其心理健康。适度的体育锻炼、良好的生活习惯等也对改善VLS患者的症状具有一定的作用。由于VLS可严重影响患者的生活质量和性活动,并可能发生恶性转化,因此需要进行大量的临床和实验室研究,明确该病发生发展的关键要素,从而针对病因制定更合理有效的治疗方案,最终实现从源头上阻断VLS病情的进展和恶化。
参考文献:
1.程诗语,石洁,李艳丽等.外阴硬化性苔藓的临床研究进展[J].国际生殖健康/计划生育杂志 ,2024,43(3):260-264.
2.宋静卉,邢丽媛,王思思等.外阴硬化性苔藓患者的生活质量及影响因素:基于198例成年女性问卷调查[J].皮肤性病诊疗学杂志,2022,29(4):311-316.
3.De Luca DA,Pa para C,Vorobyev A,et al.Lichen sclerosus:The 2023 update[J]. Front Med(Lausanne),2023,10:1106318.
4.其他文献略。