1、晚期胃癌的精准治疗现状
好的生物标志物是精准医学的基石
个体可分为不同的亚群,他们对特定疾病或特定治疗反应的敏感性不同;
生物标志物检测可通过确定患者肿瘤接受哪种治疗最有可能缓解或耐药来实现个体化治疗。
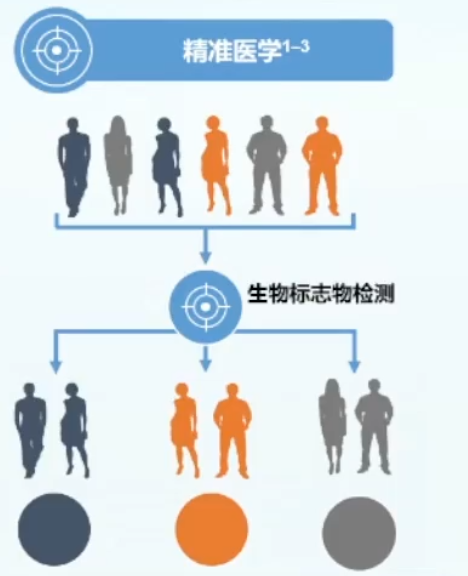
生物标志物检测使肿瘤个体化治疗成为可能:
正确的患者,在正确的时间,得到正确的治疗
精准医学的优势:
患者接受最有可能获得缓解的干预措施
患者不会接受不必要的干预
可能预测哪些患者更有可能发生不良事件,进而可避免特定治疗
更有效利用医疗资源
精准医学的劣势:
检测方法可能无法标准化
可能较昂贵
目前在实践中作用有限
胃癌的异质性强,精准分子驱动指导晚期胃癌显示临床获益
2、晚期胃癌的精准治疗生物标志物
靶向和免疫药物:仅HER2、VEGFR、PD-1取得阳性结果。
胃癌分子靶点:
-
HER2:胃癌中表达阳性的比例高达22%
-
PD-L1:表达率随不同测试结果不同
CPS≥1 67-73%
CPS>5 29-31%
CPS>10 16-18%
-
FGFR:30.2%的晚期胃癌显示FGFR2b阳性,FGFR2b的表达和较差预后有关
-
CLDN18.2:36%的晚期胃癌CLDN18.2高表达(高表达:≥75%的肿瘤细胞中 2+/3+ IHC染色)
-
MET:50%胃癌蛋白质水平上表现过表达(IHC),3-4%出现基因扩增
胃癌免疫治疗的疗效预测标志物
MSI、PDL1、TMB、EBV、CNA、GEP
MSI-H/dMMR在胃癌中的应用
-
MSI-H/dMMR可见于约8-37%的胃癌患者
-
在胃癌中,MSI-H/dMMR状态的出现主要源自MLH1基因启动子的超甲基化导致的表观遗传学基因沉默
-
MSI-H/dMMR状态是胃癌患者预后较好的预后相关生物标志
-
在胃癌中,MSI-H/dMMR状态可能作为抗PD-1/PD-L1药物的预测性生物标志:一些FDA批准的适应症包括MSH-H/dMMR状态
-
美国NCCN指南推荐一旦确认或怀疑转移性恶性肿瘤,即可进行MSI-H/dMMR检测
EBV在胃癌中的应用
特点:
-
领域内较新的一类生物标志物
-
目前临床通过原位杂交法(ISH)检测EBER判定
-
前期韩国小样本研究数据具有前景,但其他报导结果并未如此理想
不足:
-
胃癌患者中EBV+比例极低
-
缺乏前瞻性研究验证
MSI-H、EBV阳性、PD-L1阳性是Pembro治疗有效的标志物。
3、胃癌肿瘤微环境与未来研究方向
肿瘤微环境(tumor microenvironment,TME):
细胞成分:包括肿瘤细胞、免疫细胞、内皮细胞、基质细胞以及与肿瘤相关成纤维细胞等;
非细胞成分:包括细胞因子、趋化因子、细胞外基质等;
普遍特征:缺氧、酸性、血管增生异常、免疫抑制
TCGA胃癌分子分型
2014年,从TGGA数据库调取295名患者的临床数据
蛋白水平聚类分析主要分为四类:EBV;MSI;CIN;GS
不同分子亚型的胃癌对免疫治疗疗效有显著差异
-
MSI-H和EBV(+)胃癌与MSS/EBV(-)对免疫治疗应答患者较高的免疫激活状态
胃癌不同分子分型有着不同的肿瘤免疫微环境(TME)
-
基因组稳定型(genomically stability,GS):肿瘤具有更多巨噬/B细胞,约50%具有三级淋巴结构,适合接受免疫治疗;
-
染色体不稳定型(chromosomal instability,ClN):肿瘤大部分为“冷肿瘤”,表现为T细胞耗竭和肿瘤相关巨噬细胞TAM浸润,可能与MYC和细胞周期通路富集有关
TME评分高的患者更能从免疫治疗中获益
4、总结
-
精准治疗为晚期胃癌治疗带来新希望,好的生物标志物是精准医学的基石,胃癌的异质性强,精准分子驱动指导显示出临床获益;
-
胃癌分子分型与精准治疗疗效相关,需根据不同生物标记物特征对患者进行更精准的分层,筛选出对于靶向或者免疫治疗获益人群;
-
胃癌分子分型与免疫治疗疗效相关,不同分子分型有不同的微环境特征,需尝试根据不同微环境特征对患者进行更精准的分层,筛选出对免疫治疗获益人群。