肥胖是一种激增的公共健康风险,经常与致命的疾病有关,包括糖尿病、中风和心肌梗死。常见的肥胖治疗方法包括饮食控制、减肥药和减肥手术,但这些方法往往无效或不安全。在此,唐本忠院士、王东教授团队报道了一种微创和有效的方法,通过利用红外/近红外发射和脂滴靶向聚集诱导的发光物质(AIEgens),即TTMN和MeTTMN,对脂肪细胞中的大颗粒脂滴进行特异性靶向和光诱导过氧化反应。已报道的AIEgens能够以高信噪比跟踪和监测前脂肪细胞形成脂肪细胞的过程。此外,所提出的AIEgens作为I型光敏剂,在白光下产生高活性的羟基自由基和超氧化物,通过脂质过氧化的连锁反应消除成熟脂肪细胞,即使在低氧供应下也是如此。还展示了在体内光动力疗法(PDT)中使用AIEgens进行皮下减脂治疗。这项工作证明了AIEgens作为一种双重成像和I型光敏剂用于光动力疗法来诱导脂肪细胞凋亡,涉及到一种简单的制造和治疗过程。建议的体内光动力肥胖治疗方法对非靶向正常组织的毒性可以忽略不计,为未来有效和相对安全的肥胖治疗提供了一种替代方法。该研究以题为“Adipocyte-Targeting Type I AIE Photosensitizer for Obesity Treatment via Photodynamic Lipid Peroxidation”的论文发表在ACS Nano上。
在此,报道了两种具有很强的I型PDT能力的红外/近红外抗原(TTMN和MeTTMN)用于选择性靶向分化的脂肪细胞和通过光动力脂质过氧化治疗肥胖(图1)。MeTTMN的扩展供体−受体结构导致长波吸收和荧光发射,这有利于深部组织成像和光动力学治疗,光散射效应和自体荧光信号影响较小。3T3-L1细胞是研究肥胖代谢机制和成脂分子机制的一种广泛应用的脂肪细胞分化细胞模型。在体外研究中,3T3-L1细胞通过改良的方法向成熟脂肪细胞分化为成熟脂肪细胞。AIEgens优先定位并聚集在成熟3T3-L1脂肪细胞中较大尺寸的脂滴中,而不是较少和较小的未分化细胞。在白光照射下,MeTTMN通过I型反应途径光敏化产生高活性的羟基自由基,通过光动力脂质过氧化有效地清除成熟的3T3-L1脂肪细胞。由于MeTTMN在3T3-L1前脂肪细胞中的浓度较低,因此对这些未成熟脂肪细胞的毒性可以忽略不计。证实了由MeTTMN产生的ROS可以在脂肪细胞的大脂滴中启动脂质过氧化的连锁反应,诱导类似铁死亡的细胞程序性死亡过程,从而实现成熟的脂肪细胞死亡。本工作为开发高效产生ROS的I型AIE光敏剂提供了有价值的结果,以及它们作为一种有效和相对安全的图像引导光动力疗法治疗肥胖的潜力。
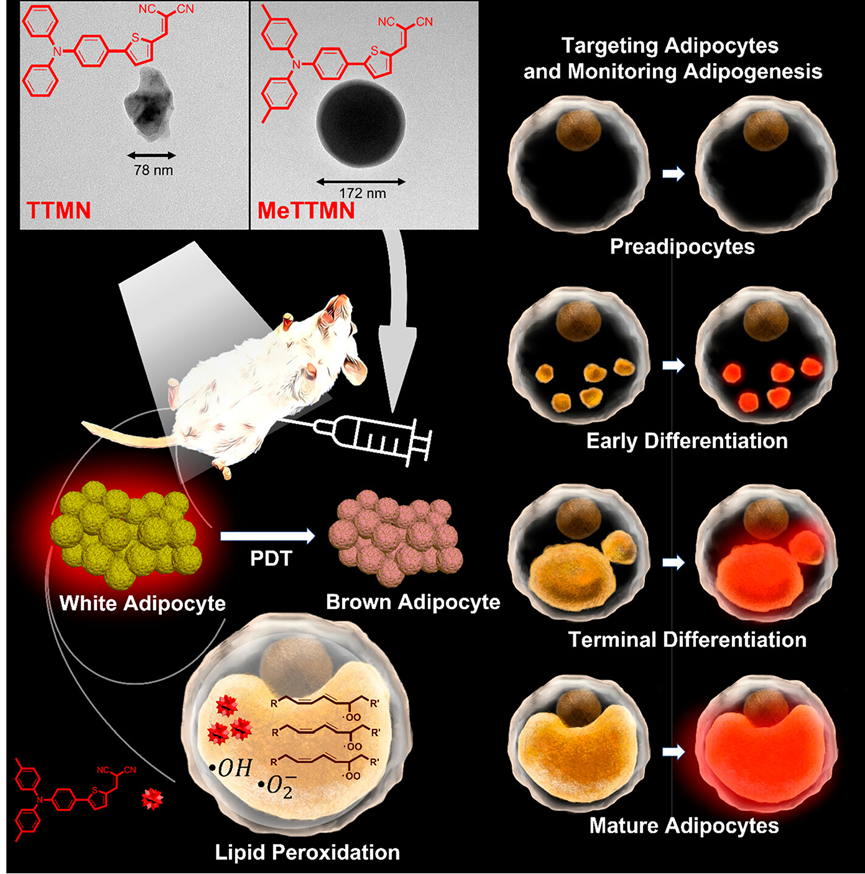
图1.脂肪细胞靶向的I型AIE光敏剂通过脂质过氧化治疗光动力性肥胖的示意图
【TTMN和MeTTMN的光物理性质】
3T3-L1前脂肪细胞和正常细胞,包括C2C12细胞(小鼠成肌细胞系)和RAW264.7细胞(巨噬细胞系),几乎不被2 μM的AIEgens染色。相反,两种AIEgens都成功地染色了5天分化的3T3-L1脂肪细胞,并在共聚焦成像下观察到明亮的红色发射。为了确定TTMN和MeTTMN的染色位置,将市售的BODIPY493/503脂滴与2 μM TTMN或2 μM MeTMN共同孵育。AIEgens和BODIPY信号完全融合,表明TTMN和MeTTMN对3T3-L1脂肪细胞中的脂滴具有特异性靶向。脂滴的特异性归因于TTMN和MeTTMN的高度疏水性,这导致了抗原与脂滴中丰富的甘油三酯和脂肪酸之间的疏水−疏水相互作用。
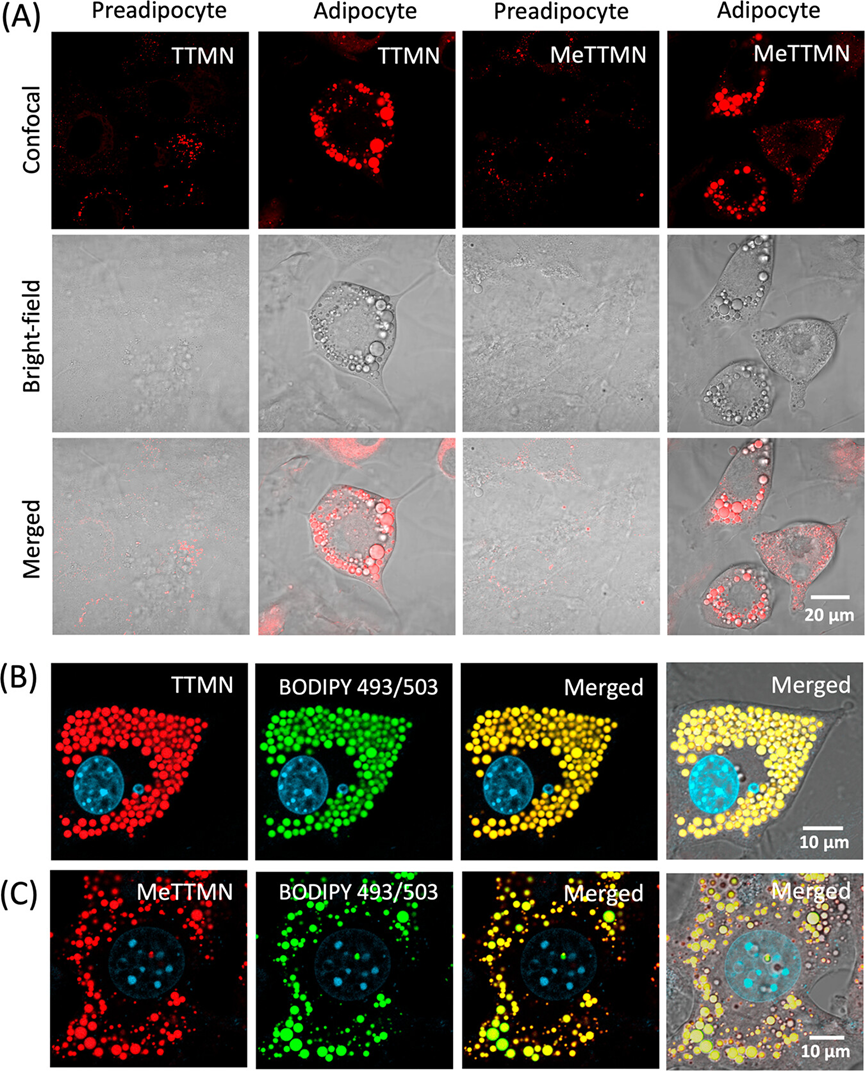
图2.TTMN和MeTTMN的光物理性质
【脂肪生成监测】
在确认了TTMN和MeTTMN的特异性脂肪细胞靶向性后,进一步研究了AIEgens监控脂肪细胞分化过程的能力。测试了TTMN和MeTTMN分别与不同阶段分化的3T3-L1细胞孵育的结果。分化后10d,TTMN和MeTTMN在20倍倍镜下可见淡红色荧光。在40倍倍镜下,由于3T3-L1细胞中含有部分脂滴的比例很小,红色信号来自于小部分细胞中的大脂滴,这表明成功地诱导了脂肪生成。相反,在细胞分化过程20天后,在放大20倍的情况下,TTMN和MeTTMN实验都观察到了密集的红色发射信号,所有的红色信号都来自于大多数3T3-L1细胞中密集的脂滴聚集。这表明大多数3T3-L1细胞已经成功地进行了脂肪生成以形成脂肪细胞。因此,基于发射信号的差异,AIEgens不仅可以通过有效识别和监测细胞的分化过程来促进脂肪形成和脂肪细胞分化,而且还可以通过流式细胞仪的细胞分选将3T3-L1脂肪细胞从未分化的细胞中分离出来。
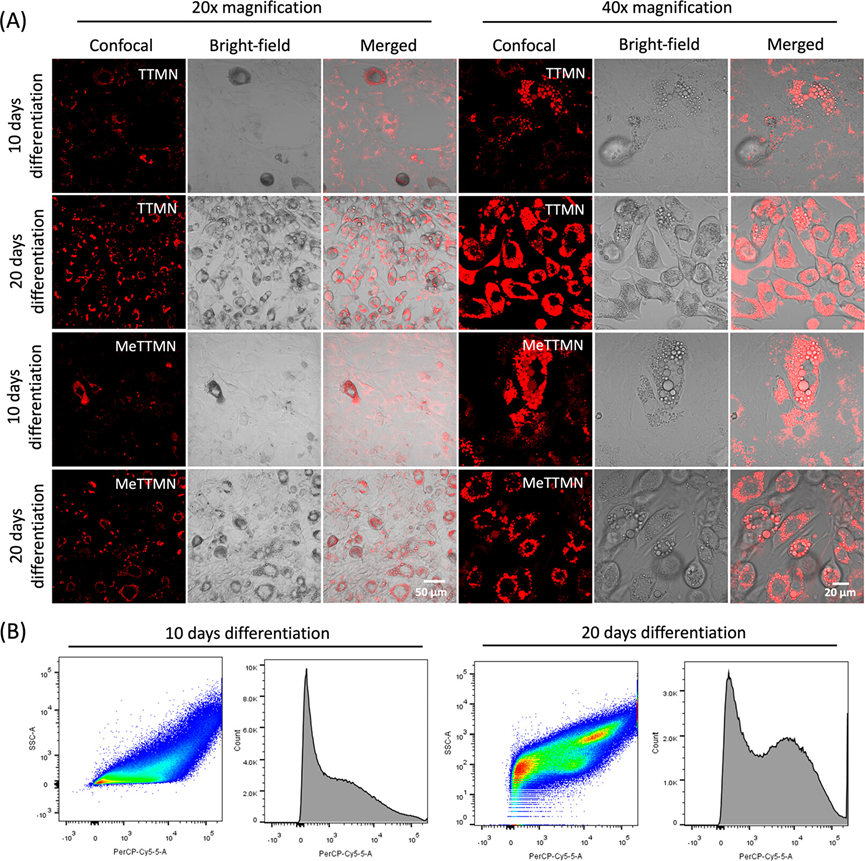
图3.脂肪生成监测
【AIE光敏剂高效产生I型ROS】
研究了TTMN和MeTTMN的脂肪细胞生物成像能力后,考察了它们在白光照射下产生ROS的能力。发现在最佳光照条件下,MeTTMN产生的ROS量最高,远远高于TTMN和Ce6。一般来说,ROS可以通过第一类(电子转移)和第二类(能量转移)反应过程产生。结果显示在三种受试光敏剂中,在Ce6存在的情况下,ABDA吸收的分解率最高(最高可达23%)。在TTMN存在下,只有约10%的ABDA被分解,而在MeTTMN的存在下,ABDA的分解可以忽略不计。这些结果表明,AIEgens产生的大部分ROS是通过I型途径而不是II型途径产生的。TTMN和MeTMMN都以稳定的速度产生羟基自由基。此外,TTMN和MeTTMN在90 s光照时间内产生了强烈的超氧化物。在相同的条件下,MeTTMN比TTMN产生更多的超氧化物。与已报道的含阳离子吡啶的AIE光敏剂不同,所研究的AIEgens产生的ROS大多为羟基和超氧化物,因此TTMN和MeTTMN可被归类为I型AIE光敏剂。由于I型光敏剂在ROS的产生中对氧的依赖性较低,它们可以克服II型光敏剂在PDT中遇到的一些限制,特别是对于低氧条件下的脂肪细胞。
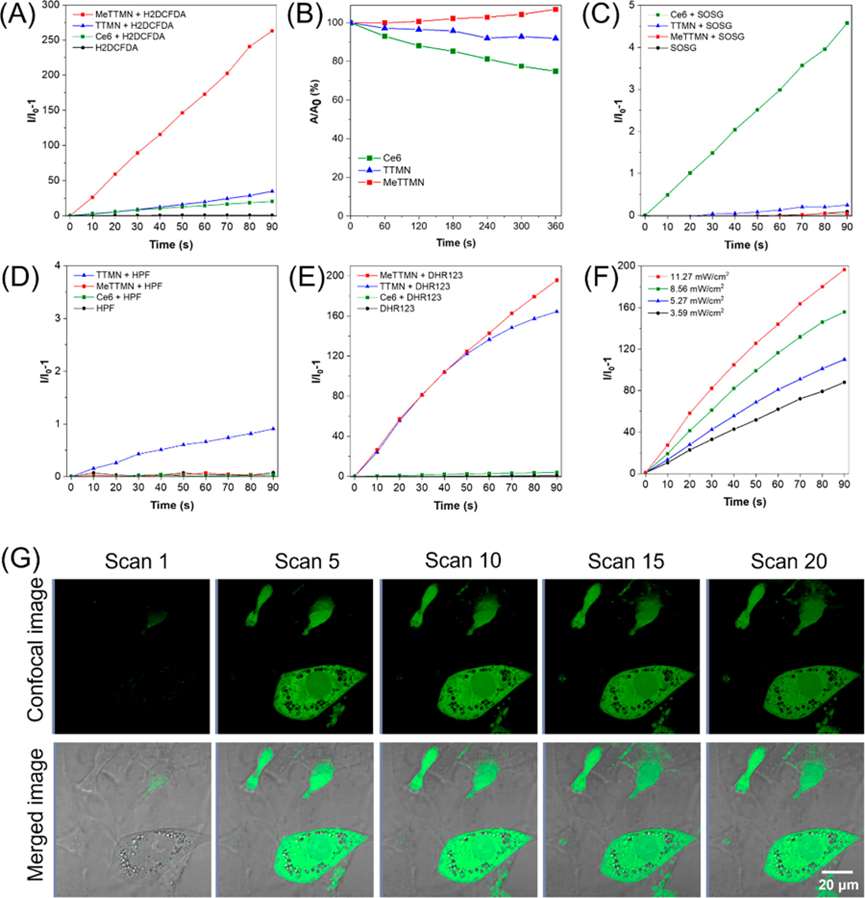
图4.AIE光敏剂高效产生I型ROS
【体外PDT对脂肪细胞的作用】
接下来,以H2DCFDA为指示剂,研究了光照射下3T3-L1细胞中AIEgens的一般ROS生成。AIEgens孵育15 min后,细胞内H2DCFDA的绿色荧光信号随着光照时间的延长而增强,表明AIEgens能在3T3-L1细胞内产生ROS。为了进一步证实所提AIEgen可以在脂肪细胞内产生羟基自由基,使用HPF作为羟基自由基指示剂来处理细胞并监测体外ROS的产生。在与AIEgens孵育15 min后,随着光照时间的增加,观察到中等的HPF发射信号。相反,由于前脂肪细胞中的脂滴较少,3T3-L1前脂肪细胞的HPF信号可忽略不计。因此,在3T3-L1细胞中,羟基自由基水平与聚集的AIEgen的数量成正比。这种产生的羟基自由基的浓度差异可以用来特异性地损伤富含脂滴的脂肪细胞。
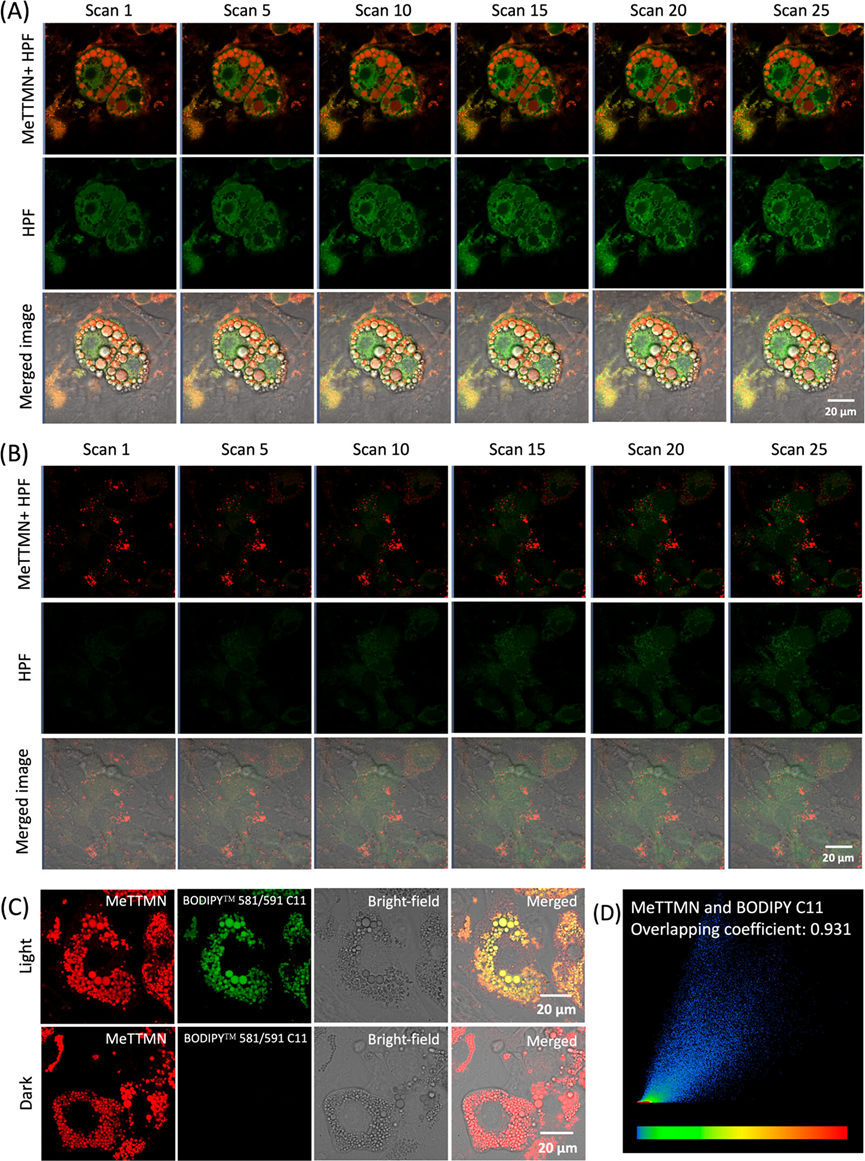
图5.体外PDT对脂肪细胞的作用
在阐明TTMN和MeTMN能够特异性靶向富含脂滴的脂肪细胞,以及在脂肪细胞的脂滴中有效地产生ROS和诱导脂质过氧化的能力之后,进一步评价了TTMN对脂肪细胞的光动力消融效率。3T3-L1前脂肪细胞和3T3-L1脂肪细胞与AIEgens孵育15 min,然后光照30 min,孵育4 h。光照射后的前脂肪细胞大部分是活的,这表明AIEgens对非靶向前脂肪细胞的毒性很低。
在暗培养过程中,TTMN处理组和MeTMN处理组的细胞毒性分别为50%和70%以上。特别是,MeTTMN显示出比TTMN更有效的脂肪细胞杀伤能力,这是因为它具有高ROS生成能力,导致MeTTMN产生更多有效的超氧化物。因此,MeTTMN是一种有效的、特异的脂肪细胞靶向和杀伤双探针。
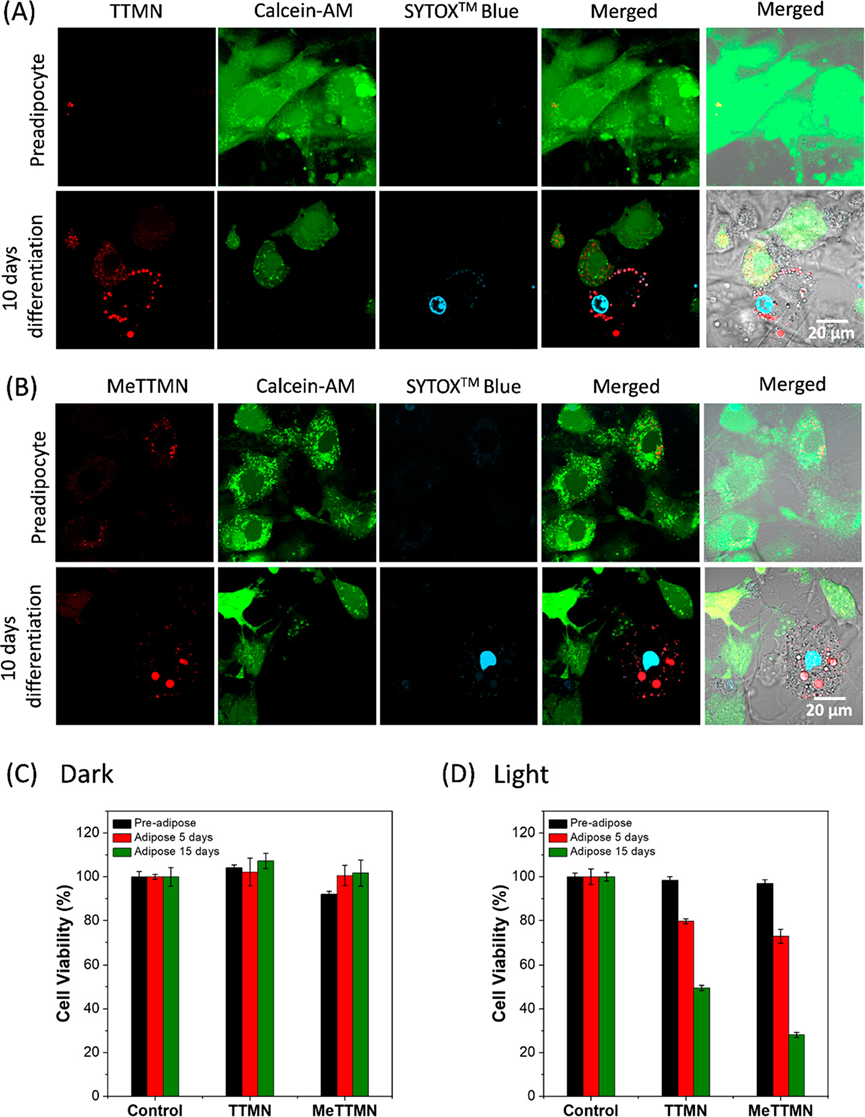
图6.前脂肪细胞或10天分化脂肪细胞染色的共聚焦图像
【在体内进行减脂治疗】
利用雄性肥胖小鼠模型进一步研究了光动力脂肪消融的性能。将小鼠分为四组,即(1)注射MeTTMN后再接受白光照射的组,(2)仅接受MeTTMN排斥反应的组,(3)仅接受光照射治疗的组,(4)对照组。肥瘦小鼠被喂食高能量食物22天以诱导肥胖, 在喂食高能量食物的日子里,持续监测小鼠的体重增加。在15天的肥胖治疗期间,不同组的小鼠的体重被监测,其中接受完全MeTTMN注射+光照射治疗的小鼠组显示出显著的体重控制。相比之下,对照组小鼠在15天的治疗中仍然表现出体重增加。此外,对照组、MeTTMN组和仅接受光照射治疗组肥胖小鼠的体型呈圆形,而MeTTMN+光照射治疗组小鼠的体型明显变瘦。在4组小鼠中,MeTTMN+光照射治疗组小鼠血糖水平恢复正常的速度最快,MeTTMN+光治疗组小鼠表现出较少的糖尿病倾向。究其原因,AIE光敏剂在光照射治疗过程中对脂肪细胞的消融作用是导致小鼠体重减轻和腰围减少的主要原因。并且所制备的MeTTMN具有可忽略的光毒性和良好的体内生物相容性。
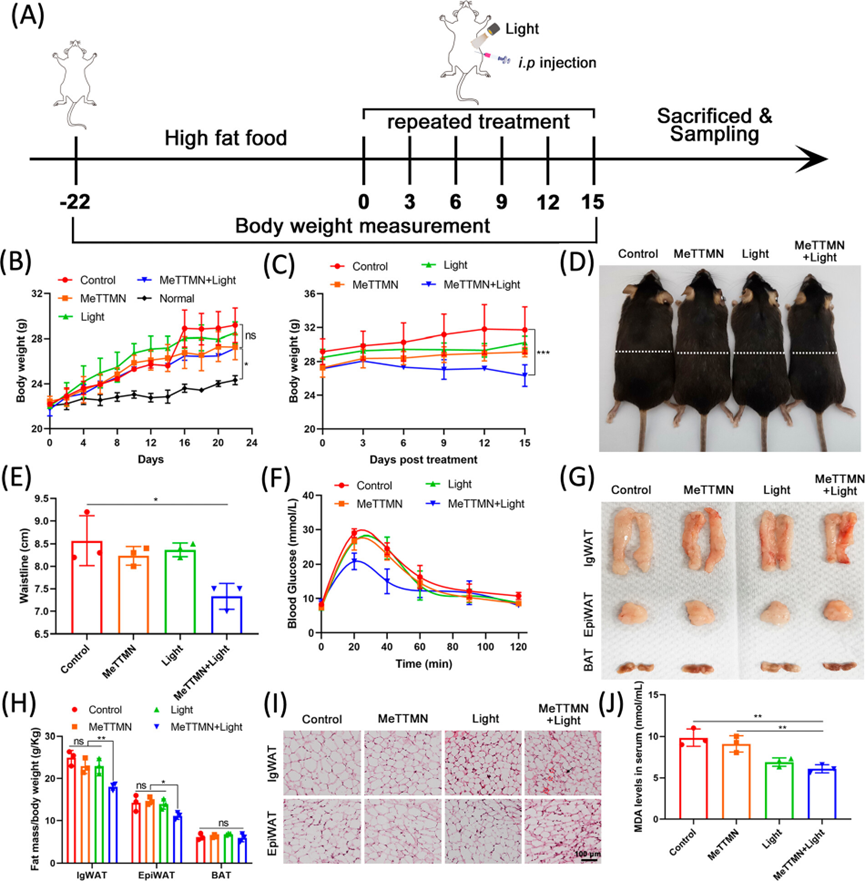
图7.使用MeTTMN作为光敏剂的体内光动力肥胖治疗
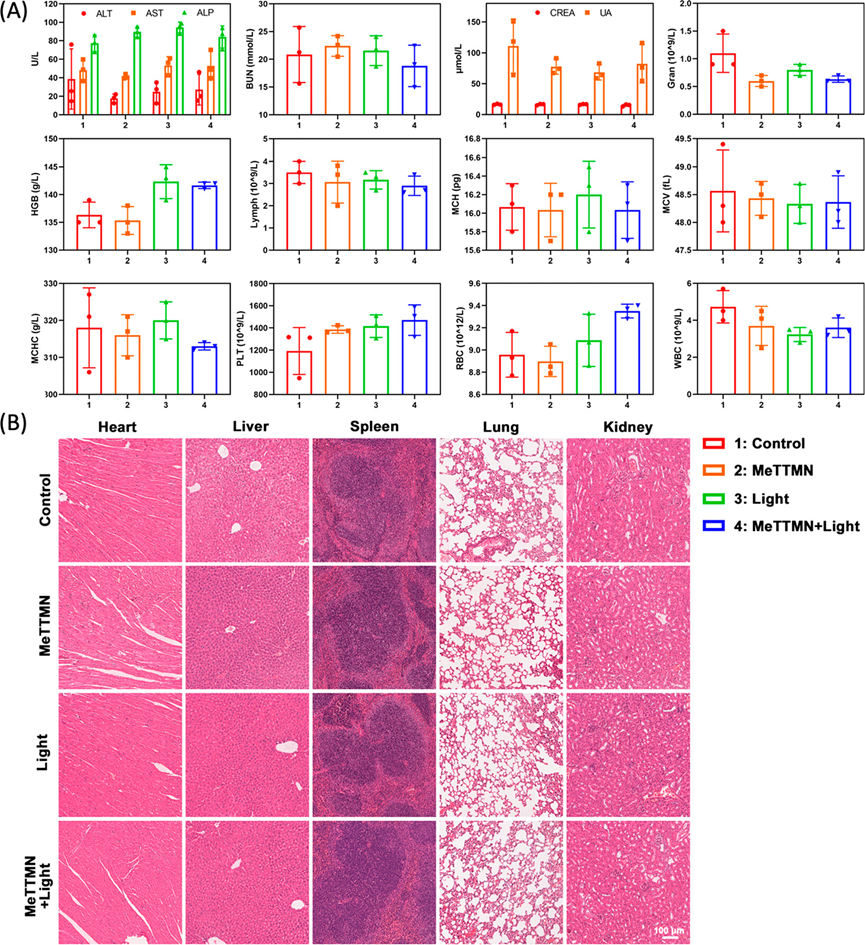
图8.光动力肥胖治疗的体内毒性分析
【小结】
该研究证明了疏水性AIEgens,TTMN和MeTTMN,可以特异性地靶向并聚集在脂肪细胞内,数量丰富,脂滴较大。TTMN和MeTTMN具有良好的AIE特性,能够在脂滴中触发强烈的红色发射,能够有效地识别成熟脂肪细胞和前脂肪细胞,并提供方便的活细胞跟踪和监测脂肪形成过程。此外,所提出的I型AIE光敏剂产生羟基自由基和超氧化物,适用于对氧依赖性较小的过度脂肪细胞的光动力消融。TTMN和MeTTMN产生的活性氧还会引发脂质过氧化的连锁反应,从而产生协同作用,消除白色脂肪组织。体内减脂研究表明,通过微针将AIEgens原位输送到脂肪组织是一种有效的PDT方法。这种治疗促进了目标白色脂肪细胞的褐变过程,从而实现了减脂。这项工作为以最小的创伤有效地对抗肥胖提供了一种替代方法。然而,AIE光敏剂如何在光动力疗法中实现脂肪细胞消除的潜在机制仍需进一步研究。在后续工作中,将探索该疗法在消除内脏周围脂肪方面的效果。
原文链接:
https://pubs.acs.org/doi/10.1021/acsnano.3c03654