初诊多发性骨髓瘤的治疗模式在过去几十年中发生了显著变化,从传统的类固醇/烷化剂为基础的诱导方案,发展到包括免疫调节剂、蛋白酶抑制剂或单克隆抗体在内的有效组合,近期大规模研究显示,资源丰富的环境中,患者接受治疗后的整体生存期达到126个月,然而,由于目前有多种一线治疗方案可供选择,关于不同方案相对安全性和疗效的讨论仍在持续,ENDURANCE随机对照试验发现,未接受立即自体干细胞移植的患者接受KRd(卡非佐米、来那度和地塞米松)和VRd(硼替佐米、来那度胺和地塞米松)诱导治疗,无进展生存期没有显著差异,然而,后续的真实世界研究显示,初诊多发性骨髓瘤患者的治疗效果存在差异,基于卡非佐米的诱导治疗方案在一线治疗中的应用持续上升,鉴于以上情况,该研究通过系统评价和Meta分析,比较了KRd和VRd作为初诊多发性骨髓瘤诱导治疗的疗效。

方法
该研究系统性检索了PubMed、Embase和Cochrane图书馆从建库至2024年1月的相关研究,并使用Rayyan软件独立筛选检索记录,纳入随机对照试验和观察性研究,比较了KRd和VRd作为初诊多发性骨髓瘤诱导治疗的疗效,排除了以下类型的研究:(1)包括复发/难治性多发性骨髓瘤或其他浆细胞疾病患者的研究;(2)缺乏VRd或KRd组的研究;(3)未报告比较结果的研究;(4)与其他纳入研究存在重叠人群的研究。两位研究者独立提取了全文出版物的相关数据,并由第三位研究者解决分歧,两位研究者独立评估了研究偏,主要研究终点是无进展生存期,次要研究终点包括总生存期、总反应率、完全反应率和可测量残留疾病阴性率。
研究结果
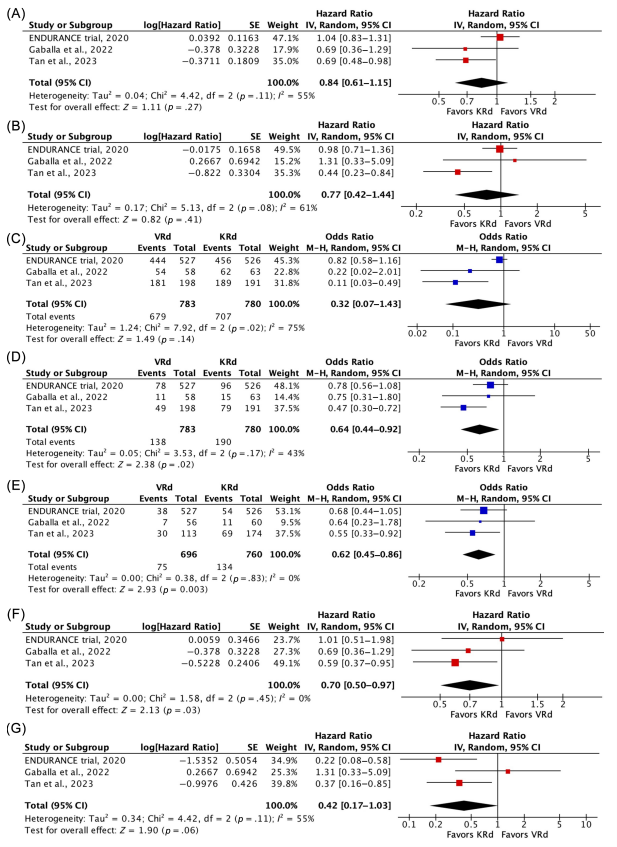
无进展生存期(PFS):KRd组和VRd组在PFS上没有显著差异(HR=0.84; 95% CI=0.61-1.15; p=0.27; I2=55%)。总生存期(OS):两组在OS上也没有显著差异(HR=0.77; 95% CI=0.42-1.44; p=0.41; I2=61%)。总反应率(ORR):两组在ORR上同样没有显著差异(OR=0.32; 95% CI=0.07-1.43; p=0.14; I2=75%)。完全反应率(CRR):与VRd组相比,KRd组有更高的CRR(OR=0.64; 95% CI=0.44-0.92; p=0.02; I2=43%)。可测量残留疾病阴性率:KRd组也有更高的MRD阴性率(OR=0.62; 95% CI=0.45-0.86; p=0.003; I2=0%)。高危险细胞遗传学特征患者亚组分析:在1137名具有细胞遗传学数据的患者中,348名(31%)被确定为高危险初诊多发性骨髓瘤。在这亚组中,与VRd相比,KRd诱导治疗与PFS的显著改善相关(HR=0.70; 95% CI=0.50-0.97; p=0.03; I2=0%)。总生存期(OS)亚组分析:尽管在KRd组中观察到OS改善的趋势,但未达到统计学显著性(HR=0.42; 95% CI=0.17-1.02; p=0.06; I2=55%)。
安全性
ENDURANCE试验中,KRd组观察到严重的心肺-肾脏毒性(16% vs 4.7%)和治疗相关死亡(2.1% vs 0.4%)的发生率高于VRd组,该研究的主要目的是比较两种方案的疗效,因此未进行患者报告的结果或安全性分析,目前实践中更常用的卡非佐米剂量方案是每周70mg/m2,但大多数患者接受的卡非佐米剂量方案是每周36mg/m2两次。文献中缺乏前瞻性/回顾性比较包含抗CD38单克隆抗体的VRd和KRd四联方案的安全性数据,因此,该研究无法对两种诱导治疗方案的安全性进行直接比较。
结论
PFS和OS:在整体人群中,KRd组和VRd组在PFS和OS上没有显著差异,这表明VRd诱导治疗仍然是无高危险细胞遗传学特征患者的标准一线选择,高危险患者:在1137名具有细胞遗传学数据的患者中,348名(31%)被确定为高危险初诊多发性骨髓瘤,在这亚组中,与VRd相比,KRd诱导治疗与PFS的显著改善相关。CRR和MRD阴性率:与VRd组相比,KRd组有更高的CRR和MRD阴性率,支持将KRd作为高危险初诊多发性骨髓瘤患者的一线诱导治疗。安全性:由于缺乏直接的安全性比较,需要更多研究以全面评估两种诱导方案的安全性特征,当前进行的比较两种诱导治疗方案的前瞻性随机对照试验将有助于完善和个体化初诊多发性骨髓瘤的治疗策略。
原始出处
Costa BA, Costa TA, Pak K, Patel A, Felix N, Mouhieddine TH, Richter J. 2024. Comparative efficacy of carfilzomib, lenalidomide, and dexamethasone (KRd) versus bortezomib, lenalidomide, and dexamethasone (VRd) in newly-diagnosed multiple myeloma: A systematic review and meta-analysis. American Journal of Hematology n/a.